FOSZFIN-FOSZFIT TÍPUSÚ KIRÁLIS LIGANDUMOK ELŐÁLLÍTÁSA ÉS ALKALMAZÁSA ENANTIOSZELEKTÍV
KATALITIKUS SZINTÉZISEKBEN
DOKTORI (PhD) ÉRTEKEZÉS
Készítette:
Farkas Gergely okleveles vegyész
Témavezető:
Dr. Bakos József
egyetemi tanár, a kémiai tudomány doktora
Kémiai és Környezettudományi Doktori Iskola
Kémia Intézet
Szerves Kémia Intézeti Tanszék Veszprém
2013
Értekezés doktori (PhD) fokozat elnyerése érdekében a Pannon Egyetem Kémiai és Környezettudományi
Doktori Iskolájához tartozóan Írta:
Farkas Gergely
Témavezető: Dr. Bakos József Elfogadásra javaslom (igen / nem)
...
(aláírás)
A jelölt a doktori szigorlaton ...%-ot ért el.
Az értekezést bírálóként elfogadásra javaslom:
Bíráló neve: …... …... igen /nem
……….
(aláírás)
Bíráló neve: …... …... igen /nem
……….
(aláírás)
Bíráló neve: …... …... igen /nem
……….
(aláírás)
A jelölt az értekezés nyilvános vitáján …...%-ot ért el.
Veszprém, ……….
a Bíráló Bizottság elnöke A doktori (PhD) oklevél minősítése…...
………
Az EDHT elnöke
TARTALMI ÖSSZEFOGLALÓ ... 9
ABSTRACT ... 11
ZUSAMMENFASSUNG ... 12
Rövidítésjegyzék ... 13
Bevezetés és célkitűzések ... 15
1. Irodalmi áttekintés ... 18
1.1. Az aszimmetrikus katalízis mérföldkövei ... 18
1.2. Foszfin-foszfit típusú ligandumok ... 22
1.3. Enantioszelektív szintézisek ... 30
1.3.1. A palládiumkatalizált aszimmetrikus allil-helyzetű szubsztitúció ... 31
1.3.2. A ródiumkatalizált aszimmetrikus hidrogénezés mechanizmusa ... 35
1.4. Foszfin-foszfit ligandumok sztereo-elektronikus tulajdonságai ... 42
1.4.1. Sztérikus sajátságok... 42
1.4.2. Elektronikus sajátságok ... 44
1.5. A kelátgyűrű szerepe az enantioszelektív szintézisekben ... 48
1.5.1. A kelátgyűrű konformációja ... 48
1.5.2. A bite angle effektus ... 53
1.6. A transz-hatás és a transz-befolyás ... 57
1.7. Egyfogú és kétfogú heterodonor ligandum-kombinációk ... 60
1.8. Foszfin-foszfit ligandumok előállítása ... 63
2. Eredmények és értékelésük ... 66
2.1. A ligandumok szintézise, ... 66
2.1.1. Foszfin-foszfit ligandumok előállítása ciklikus szulfát-észterek gyűrűnyitásával ... 67
2.1.2. Foszfin-foszfit ligandumok előállítása karbonilvegyületek nukleofil addíciós reakciójával ... 73
2.1.4. Foszfin-foszfit ligandumok előállítása ciklikus éterek gyűrűnyitásával . 77 2.1.5. Foszfin-foszfit ligandumok előállítása természetes, optikailag aktív
vegyületek felhasználásával ... 78
2.2. Szelén-származékok és átmenetifém-komplexek előállítása és spektroszkópiai vizsgálata ... 80
2.2.1. Elektronikus sajátságok ... 80
2.2.2. Ródium-komplexek ... 83
2.2.3. Palládium-komplexek ... 90
2.3. Palládium- és ródium-komplexek katalitikus alkalmazásai ... 93
2.3.1. Palládiumkatalizált aszimmetrikus allil-helyzetű szubsztitúció ... 93
2.3.1.1. Az oldószer hatásának vizsgálata ... 95
2.3.1.2. A hőmérséklet hatása ... 98
2.3.1.3. Az alkálifém-sók hatása ... 99
2.3.1.4. A ligandumok szerkezetének hatása ... 100
2.3.2. Prokirális olefinek homogénkatalitikus aszimmetrikus hidrogénezése . 104 2.3.2.1. A nyomás hatása ... 104
2.3.2.2. Az oldószer hatása ... 106
2.3.2.3. A hőmérséklet hatása ... 108
2.3.2.4. A szubsztrátum szerkezetének hatása ... 110
2.3.2.5. A ligandum szerkezetének hatása ... 112
2.3.2.6. A kelátgyűrű tagszámának hatása ... 113
2.3.2.7. A szubsztrátum-katalizátor mólarány hatása ... 120
2.4. A ligandum-kombinációs módszer vizsgálata aszimmetrikus hidrogénezési reakciókban ... 120
Összefoglalás ... 124
A disszertáció tézisei ... 126
Theses of the dissertation ... 131
3. Kísérleti rész... 136
3.1. Szintézis ... 136
Irodalomjegyzék ... 170
„Az aszimmetrikus katalízis négydimenziós kémia. A jó eredmények eléréséhez egy ideális 3D szerkezet (x, y, z) és a megfelelő kinetika (t) is szükséges.”
„Asymmetric catalysis is four-dimensional chemistry. High efficiency can be achived only by using a combination of both an ideal 3D structure (x, y, z) and suitable kinetics (t).”
Ryoji Noyori
Hálásan köszönöm témavezetőmnek, Dr. Bakos Józsefnek a PhD munkám elkészítéséhez nyújtott áldozatkész segítségét. Kezdeti problémafelvetéseimet és ötleteimet megformálta, szilárd koncepcióvá alakította. Szakmai és emberi iránymutatása nélkül e dolgozat nem valósulhatott volna meg.
Köszönettel tartozom Édes Béla vegyésztechnikusnak, aki a laboratóriumi munkában nyújtott nélkülözhetetlen segítséget. Gyakorlati tapasztalata és hozzájárulása a jó hangulatú laboratóriumi munkához nagyban hozzásegítettek eredményeim eléréséhez.
Köszönet illeti Dr. Tóth Imrét, aki hasznos szakmai tanácsaival és építő jellegű kritikájával nagyban hozzájárult eredményeim egzakt értékeléséhez.
Hálával tartozom munkatársaimnak, akik szakmai tanácsaikkal, észrevételeikkel, kritikus megjegyzéseikkel és a laboratóriumi munkához nyújtott segítségükkel hozzájárultak munkámhoz. Köszönet illeti Dr. Balogh Szabolcsot, Madarász Józsefet, Dr. Fekete Miklósné Emma Nénit, Császár Zsófiát, Tresztenyák Alízt és Nánási Balázst. Továbbá köszönöm a Szerves Kémia Intézeti Tanszék minden dolgozójának áldozatkész segítségét.
Mérhetetlen hálával tartozom családomnak, édesapámnak, édesanyámnak, nagynénémnek (Franciskának) és Dórának, hogy szeretetükkel, gondoskodásukkal és biztatásukkal támogatták munkámat. Köszönet illeti G. Tóth Mihályt és feleségét, Margit Nénit a sok hasznos tanácsért és kedvességért.
Hálát adok a Mindenható Istennek, hogy munkám elkészítéséhez erőt és egészséget adott!
A kutatás a TÁMOP 4.2.4.A/2-11-1-2012-0001 azonosító számú Nemzeti Kiválóság Program – Hazai hallgatói, illetve kutatói személyi támogatást biztosító rendszer kidolgozása és működtetése országos program című kiemelt projekt által nyújtott személyi támogatással valósult meg. A projekt az Európai Unió támogatásával, az Európai Szociális Alap társfinanszírozásával valósul meg. A
TÁMOP 4.2.4.A
Foszfin-foszfit típusú királis ligandumok előállítása és alkalmazása enantioszelektív katalitikus szintézisekben
A királis kelátképző ligandumok katalitikus alkalmazása enantioszelektív katalitikus reakciókban rendkívül hatékony módszer optikailag tiszta vegyületek előállítására. Az utóbbi néhány év folyamán kifejlesztett foszfortartalmú királis hibrid ligandumokkal – így foszfin-foszfinit, foszfin-foszfonit, foszfin-foszforamidit és foszfin-foszfit ligandumokkal – módosított átmenetifém-komplexek az aszimmetrikus reakciók rendkívül hatékony katalizátorainak bizonyultak. A kétfogú kelátképző ligandumok között, a foszfin-foszfit típusú vegyületek különleges helyet foglalnak el egyedülálló elektronikus tulajdonságaiknak és egyszerű előállításuknak köszönhetően.
Jelen dolgozatban 13 alkándiil-vázzal rendelkező, axiális kiralitású (S)-binaftil vagy (S)-oktahidrobinaftil-csoportot tartalmazó hibrid foszfin-foszfit ligandum szintézisét és ródiumkatalizált aszimmetrikus hidrogénezési, illetve palládiumkatalizált enantioszelektív allil-helyzetű szubsztitúciós reakciókban való katalitikus alkalmazását mutatom be.
A vegyületek katalitikus tulajdonságainak mélyreható tanulmányozása érdekében előállítottam, és spektroszkópiai módszerekkel vizsgáltam a ligandumok ródium- és palládiumtartalmú komplexeinek koordinációs sajátságait, illetve szeléntartalmú származékaik elektronikus jellemzőit.
A palládiumkatalizált aszimmetrikus allil-helyzetű szubsztitúciós reakciók során vizsgáltam a kelátgyűrű-méret, az oldószer illetve az alkalmazott additívok hatását. A hidrogénezési reakciókban a ligandumokkal módosított ródiumtartalmú katalizátorrendszerek aktivitásának és szelektivitásának vizsgálata érdekében az egyes katalitikus reakciókat a nyomás, a hőmérséklet, az oldószer, a szubsztrátum és a kelátgyűrű-tagszám változásának függvényében tanulmányoztam.
A vizsgálatok során egyértelmű összefüggést figyeltem meg a kelátgyűrű tagszáma, illetve a katalizátorok aktivitása és szelektivitása között. Az előállított
reakciók termékét.
asymmetric catalytic reactions
The use of chiral chelating ligands has become a powerful strategy in catalyst design for enantioselective catalytic reactions. In recent years, new series of bidentate hybrid ligands such as phosphine-phosphinite, phosphine-phosphonite, phosphine- phosphoramidite and phosphine-phosphite have been shown to have high efficiency in asymmetric catalysis. Among bifunctional ligands, chiral phosphine-phosphites are a particularly interesting class of compounds due to their easy synthesis and unique electronic properties.
The present work focuses on the synthesis of a new class of chiral phosphine- phosphite ligands containing axially chiral (S)-binaphthyl or (S)-octahydrobinaphthyl moiety and their catalytic application in palladium-catalyzed enantioselective allylic alkylation and rhodium-catalyzed asymmetric hydrogenation reactions.
In order to gain a penetrating insight into the catalytic behaviour of the developed 13 novel ligands, rhodium- and palladium-complexes and selenium containing derivatives were synthesized and evaluated by using spectroscopic methods.
In palladium-catalyzed asymmetric allylic alkylation reactions the role of the structure of the ligands and the effect of the solvents and additives were evaluated. In hydrogenation reactions, pressure-, temperature-, solvent-, substrate- and chelate ring size-dependence of the new rhodium complexes were investigated for the determination of their catalytic activity and enantioselectivity.
Surprisingly, a special effect was found between the ligands structure and the catalyst activity and selectivity. Furthermore, excellent enantioselectivities and activities could be achieved in the catalytic reactions by using the novel phosphine- phosphite type ligands.
katalytischen asymmetrischen Synthesen
Die Anwendung der chiralen bifunktionellen Liganden ist eine wirkungsvolle Strategie in Katalysator-Design für die enantioselektiven katalytischen Reaktionen geworden. In den letzten Jahren haben neue Serien der zweizähnigen Hybridliganden, wie Phosphin-Phosphinite, Phosphin-Phosphonite, Phosphin-Phosphoramidite und Phosphin-Phosphite, hohe Effizienz bei der asymmetrischen Katalyse gezeigt. Unter bifunktionellen Liganden sind chirale Phosphin-Phosphite eine besonders interessante Klasse der Verbindungen wegen ihrer einfachen Synthesen und einzigartigen elektronischen Eigenschaften.
Die vorliegende Arbeit konzentriert sich auf die Synthese einer neuen Klasse der chiralen Phosphin-Phosphit Liganden mit axial chiralen (S)-Binaphthol- oder (S)- Octahydrobinaphtholeinheiten und ihre katalytische Anwendung in palladiumkatalysierte enantioselektive allylische Alkylierung und rhodiumkatalysierte asymmetrische Hydrierung.
Um einen Einblick in das katalytische Verhalten der neuen Verbindungen zu gewinnen, wurden Rhodium- und Palladium-Komplexverbindungen und selenenthaltende Derivate synthetisiert, und unter Verwendung spektroskopischer Methoden ausgewertet.
In der palladiumkatalysierten asymmetrischen allylischen Alkylierung wurde die Rolle der Ligandenstruktur und die Bedeutung der Lösungsmitteln und Additiven ausgewertet. Zur Bestimmung der katalytischen Aktivität und Selektivität der neuen Rhodium-Komplexverbindungen wurde die Abhängigkeit von Druck, Temperatur, Lösungsmittel, Substrat und Chelatringgröße untersucht.
Überraschenderweise wurde ein Spezialeffekt zwischen der Größe der Chelatringe und der Katalysatoraktivität und Selektivität gefunden. Durch die Verwendung der neuen Phosphin-Phosphit Liganden wurden exzellente Enantioselektivitäten und Aktivitäten in den katalytischen Reaktionen erreicht.
Rövidítésjegyzék
L-DOPA: L-3,4-dihidroxi-fenilalanin
DIOP: 2,2-dimetil-4,5-((difenilfoszfino)dimetil)dioxolán Dipamp:bisz((2-metoxifenil)fenilfoszfino)etán
Chiraphos: 2,3-bisz(difenilfoszfino)bután Prophos: 1,2-bisz(difenilfoszfino)propán
Norphos: 2,3-bisz(difenilfoszfino)biciklo[2.2.1]hept-5-én
BPPM: terc-butil-4-(difenilfoszfino)-2-((difenilfoszfino)metil)pirrolidin-1-karboxilát BDPP: 2,4-bisz(difenilfoszfino)pentán
BINAP: 2,2’-bisz(difenilfoszfino)-1,1’-binaftil Duphos: 1,2-bisz(2,5-dimetilfoszfolan-1-il)benzol DIMPC: 1,2-bisz((difenilfoszfino)metil)ciklohexán
Contergan: (rac)-2-(2,6-dioxopiperidin-3-il)-1H-izoindol-1,3(2H)-dion
(R,S)-Binaphos: (11bR)-4-((S)-2’-(difenilfoszfino)-1,1’-binaft-2-iloxi)dinafto[2,1- d:1’,2’-f][1,3,2]dioxafoszfepin
Cycphos: 1,2-bisz(difenilfoszfino)-1-ciklohexil-etán TOF: átalakítási frekvencia (angol turnover frequency) COA: ciklooktán
COE: ciklooktén
COD: (Z,Z)-ciklookta-1,5-dién BSA: N,O-bisz(trimetilszilil)acetamid
PC: (rac)-propilén-karbonát (4-metil-1,3-dioxolán-2-on) EC: etilén-karbonát (1,3-dioxolán-2-on)
EtOAc: etil-acetát THF: tetrahidrofurán
DN: donorszám (angol donor number)
NBD: norbornadién (biciklo[2.2.1]hepta-2,5-dién) DMIT: dimetil-itakonát
AFMe: (Z)-α-acetamido-fahéjsav-metil-észter AKMe: α -acetamido-akrilsav-metil-észter
H0-Binol: 1,1’-bi-2-naftol
H8-Binol: 5,5’,6,6’,7,7’,8,8’-oktahidro-1,1’-bi-2-naftol TADDOL: tetraaril-1,3-dioxolán-4,5-dimetanol
Bevezetés és célkitűzések
A természetben előforduló szerves anyagok egy részét optikailag aktív molekulák alkotják, melyek különleges jelentőségűek az élővilágban. Az enantiomerek egymással tükörképi viszonyban lévő szerkezetek, melyek akirális hatásokkal szemben egyformán, királis hatásokkal szemben viszont eltérő módon viselkednek. Ez utóbbi tény jelentősen megnehezíti a szintetikusan előállítható racém származékok biológiai felhasználását.
Számos optikailag aktív vegyület állítható elő a természetben található, olcsó királis anyagokból kiindulva. A módszer hátránya az, hogy ezen vegyületek száma korlátozott, illetve gyakran csak az egyik enantiomer fordul elő.
A sztöchiometrikus és katalitikus aszimmetrikus szintéziseknél optikailag inaktív vegyületekből kiindulva, valamely királis segédanyag (pl. reagens, katalizátor vagy oldószer) felhasználásával nyerhetünk optikailag aktív vegyületeket. Az átmenetifém-katalizált homogénkatalitikus aszimmetrikus szintézis királis ligandumot tartalmazó katalizátorral valósítható meg. Az optikailag aktív módosító anyag kis mennyisége királis információt hordoz és visz át a katalitikus folyamatban a képződő termék nagy mennyiségére. Ily módon akár az enzimatikus rendszereket megközelítő katalitikus aktivitást és szelektivitást is elérhetünk (gyógyszer-, növényvédőszer-, illatszer-, élelmiszeripar). Ezen előnyös tulajdonságai miatt a homogénkatalitikus aszimmetrikus szintézis az elmúlt négy évtizedben rendkívül látványos fejlődésen ment keresztül, és ma már ipari jelentőségű.
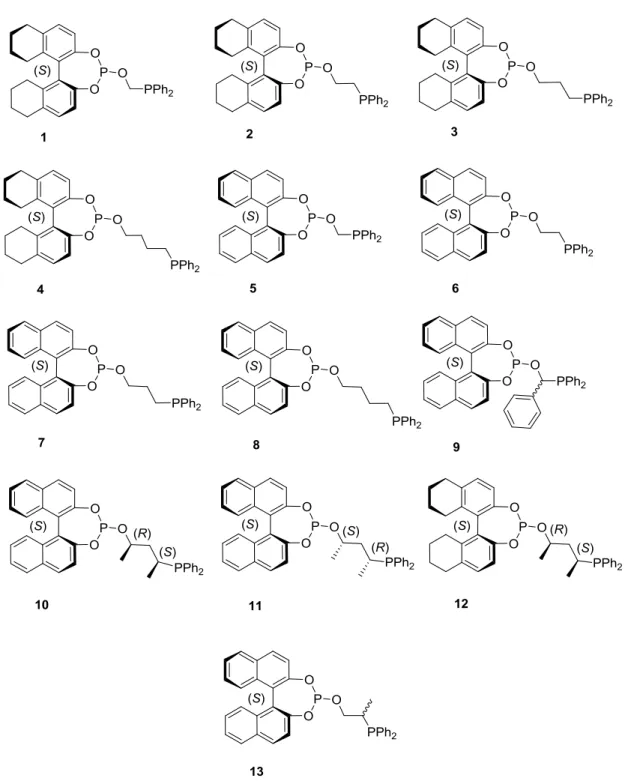
Munkám során célom volt alifás alkándiil-vázzal rendelkező, axiális kiralitású binaftil- vagy oktahidrobinaftil-csoportot tartalmazó hibrid foszfin-foszfit típusú katalizátor-módosító ligandumok előállítása (1. ábra), és ezek palládium- és ródiumtartalmú komplexeinek katalitikus vizsgálata aszimmetrikus allil-helyzetű szubsztitúciós reakciókban illetve enantioszelektív hidrogénezésben.
Tekintettel a vizsgált foszfin-foszfit ligandumok szerkezeti sokféleségére, munkám során többféle szintézisút segítségével sikerült előállítani a kívánt szerkezetű vegyületeket. Az egyes ligandumokkal módosított átmenetifém-
komplexek katalitikus jellemzőinek vizsgálata során tanulmányoztam a különböző ligandumoknak a reakció optikai hozamára és aktivitására gyakorolt hatását, majd ezen keresztül vizsgáltam a katalizátorok szerkezete és katalitikus tulajdonságai közötti összefüggést. A ligandumok koordinációs sajátságait ródium- és palládium- komplexeik illetve szeléntartalmú származékaik spektroszkópiai vizsgálata segítségével jellemeztem.
1. ábra Az előállított foszfin-foszfit ligandumok
1. Irodalmi áttekintés
1.1. Az aszimmetrikus katalízis mérföldkövei
Az optikai aktivitás jelenségét először Arago (1811) figyelte meg hemiéderes kvarckristályok vizsgálata során. Ezek a kristályok a síkban poláros fény síkját elforgatják. A kristályoknak kétféle formája létezik, melyek azonos szögben ugyan, de ellentétes irányokban forgatják a fényt.
Később Biot kísérletei nyomán kiderült, hogy bizonyos vegyületek (pl. a borkősav) oldatai is rendelkezhetnek optikai aktivitással. 1848 és 1853 között Pasteur igazolta, hogy az optikai aktivitás kapcsolatban áll a molekulák aszimmetriájával. A XIX. század végén Kekulé, Le Bel és van’t Hoff munkássága révén bebizonyosodott, hogy a Pasteur által említett aszimmetria leginkább a szénatom tetraéderes térorientációjával magyarázható.
Ezek az elméleti megfontolások nélkülözhetetlenek voltak a kiralitás fogalmának megértéséhez és ezen keresztül a királis vegyületek szintézisének tervezéséhez, megvalósításához.
Az optikailag aktív vegyületek szintézisére általánosan három lehetőség adódik:
(a) racemátokból: ekkor a keletkező racém elegyet alkotó komponensek három lehetséges módon különíthetők el: preferált kristályosítás, kinetikai rezolválás1 vagy diasztereomer kristályosítás segítségével;
(b) optikailag inaktív szubsztrátumból: aszimmetrikus szintézis segítségével, biokatalitikus vagy kemokatalitikus úton;
(c) természetes, optikailag tiszta kiindulási anyagokból, szintézissel.
A természetes, optikailag tiszta vegyületek, mint azt már a bevezetőben említettem, csak korlátozott mennyiségben állnak rendelkezésre, így a (c) módszerrel történő szintézis nagyobb méretekben ritkán kivitelezhető.
Az (a) és (b) módszer közötti határozott különbség az, hogy, míg a klasszikus megoldásnál egy mol királis segédanyaggal legjobb esetben egy mol optikailag tiszta végterméket lehet kinyerni, addig enantioszelektív katalízissel kis mennyiségű királis
katalizátorral, nagy mennyiségű királis végtermék állítható elő. Emellett a racém elegyek elválasztásakor a nem kívánt enantiomer általában elvész, így az értékes enantiomer szintézisének hozama, az adott elválasztási lépést tekintve, legfeljebb 50, enantioszelektív szintézisek során ez az érték megközelítheti a 100-ot is.
A biológiailag aktív vegyületek (gyógyszerek, növényvédőszerek, stb.) jelentős része optikailag is aktív. Az enantiomerek eltérő biológiai hatást mutathatnak, sőt a kívánt biológiai aktivitás gyakran csak az egyik enantiomerhez kötődik. Az egyik izomer tehát igen gyakran szennyezőanyag, amely nemkívánatos mellékhatásokat eredményezhet, feleslegesen terhelheti a szervezetet és a környezetet. Az 1960-as évek tragikus Contergan-története hívta fel a figyelmet a sztereokémia és az enantioszelektív szintézisek jelentőségére.2 Mindamellett az optikailag tiszta anyag hatékonysága többszöröse lehet a racemát hatékonyságának, ezért alkalmazása a racemáttal szemben jelentős profitot eredményezhet.
Az átmenetifém-katalizált aszimmetrikus szintézisek közös sajátossága, hogy valamilyen fémorganikus komplex koordinációs övezetében játszódnak le. Ezen tudományág fejlődésének kulcslépése volt az ún. „wilkinsoni-komplex”
([Rh(PPh3)3Cl]) felfedezése, mely sokféle vegyület atmoszférikus nyomáson történő hidrogénezését tette lehetővé.3 Számos szerves kémiai reakcióban mutatott katalitikus aktivitást, így izomerizációban, karbonilezésben, oligomerizációban, stb. Emellett segítségével tisztázni tudták a katalitikus ciklus alapvető összefüggéseit is.4
Rendelkezésre állt tehát egy kiváló homogén katalizátor, amelyet Horner és Knowles – egymástól függetlenül – módosítottak. Optikailag inaktív trifenil-foszfin helyett királis foszfint – (S)-fenil-metil-propil-foszfint alkalmazva -etil-sztirol hidrogénezési reakciójában, szerény mértékű aszimmetrikus indukciót értek el.5 Később felismerték azt is, hogy a katalitikusan aktív ródium-komplex in situ, tehát a reakcióelegyben is előállítható [Rh(dién)Cl]2 komplex és a megfelelő foszfin reakciójával. Ezután a kutatás Schrock és Osborn munkájával folytatódott, akik [Rh(dién)(PR3)2]+ típusú komplexeket állítottak elő és alkalmaztak hidrogénező katalizátorokként.6
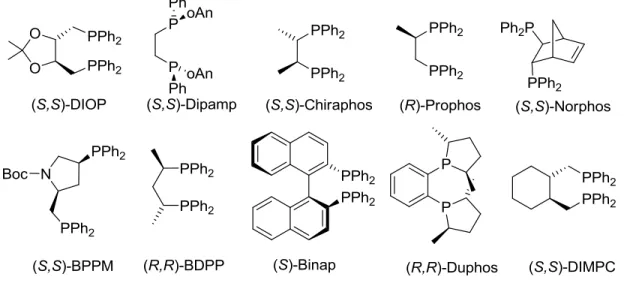
A foszfortartalmú katalizátorok fejlődésének következő állomásaként említhető a Kagan és munkatársai által előállított és a katalizátor módosítására elsőként alkalmazott királis ditertcier foszfin, a DIOP (2. ábra), mellyel prokirális dehidroaminosavak hidrogénezésében 74%-os enantioszelektivitást értek el.7 Később a Knowles által kidolgozott, ugyancsak kelátképző tulajdonságú difoszfint, a Dipamp-ot (2. ábra),8 már ipari méretekben is alkalmazták. A ligandum segítségével a Parkinson-kór gyógyítására alkalmazott L-DOPA 94%-os enantioszelektivtással állítható elő.9 Az egyfogú foszfortartalmú ligandumok mellett tehát megjelentek a több koordinatív kötés kialakítására is képes kelátképző ligandumok. A kétfogú ligandumok alkalmazása során, a képződő kelátkomplexek konformációs merevségének köszönhetően ugyanis jelentős mértékben csökkenhet a katalitikus ciklusban keletkező konformerek száma, mely növelheti a reakció szelektivitását. E felismerés révén a katalizátor-módosító ligandumok egy újabb generációja született meg. Prokirális olefinek aszimmetrikus hidrogénezési reakciójában rendkívül jó enantioszelektivitást biztosító katalitikus rendszereket állítottak elő kelátképző királis ditercier foszfin ligandumok alkalmazásával (2. ábra).
2. ábra Kelátképző királis ditercier foszfinok
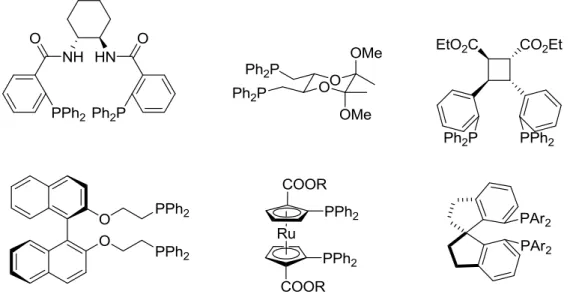
A kelátképző ditercier foszfin ligandumok alkalmazása a dolgozat egyik témájaként választott palládiumkatalizált aszimmetrikus allil-helyzetű szubsztitúciós reakciókban ugyancsak elterjedt (3. ábra).10 E reakcióban a már említett vegyületek11 mellett, gyakran alkalmazott ditercier foszfin-típusú ligandumok a 3. ábrán láthatók.12 Az allil-helyzetű szubsztitúciós reakciókban kiváló eredményeket értek el továbbá azaszemikorrin (95% ee),13 bisz-oxazolin14 (97% ee) és diaziridin15 (>99%) ligandumokkal módosított palládium-katalizátorokkal. Emellett a kiemelkedő szelektivitást és aktivitást biztosító foszfinooxazolin16 ligandumok alkalmazása ugyancsak elterjedt az aszimmetrikus allilezési reakciókban.17
3. ábra Aszimmetrikus allil-helyzetű szubsztitúciós reakciókban alkalmazott királis ditercier foszfin típusú katalizátor-módosító ligandumok
Az elmúlt években a foszfortartalmú katalizátorrendszereknek újabb típusai jelentek meg, melyek aktivitása és szelektivitása bizonyos reakciókban felülmúlja a korábban alkalmazott rendszerek katalitikus teljesítményét. Az utóbbi időben rendkívül nagy hangsúlyt kapott a C1-szimmetriájú, kétfogú katalizátor-módosító ligandumok alkalmazása.18 Az ilyen L-L’ típusú vegyületek koordinálódó donoratomjainak eltérő sztereo-elektronikus sajátságai révén tovább csökkenhet a katalitikus reakcióban megjelenő izomerek száma, amely a folyamatban a
sztereokémiai kontroll egyértelmű növekedését eredményezi.19 Mindamellett – például hidrogénezési reakciókban – a prokirális szubsztrátummolekula koordinációját is jelentős mértékben befolyásolhatja a donoratomok eltérő sztereo- elektronikus sajátsága.19a Mindezek eredményeként számos kétfogú, L-L’ típusú ligandumot állítottak elő – így például P-N,20 P-O,21 P-S22 vagy P-P’ típusú ligandumokat – és alkalmaztak különböző katalitikus szintézisekben. Ilyen új katalizátor-módosító vegyületként említhetők a P-P’ típusú, C1-szimmetriájú foszfin- foszfinit,23 foszfin-foszfonit24, foszfin-foszforamidit25 és foszfin-foszfit ligandumok.
Fontos továbbá megjegyezni, hogy az elmúlt években bizonyos egyfogú királis foszfinit,26 foszfonit,27 foszforamidit,28 illetve foszfit29 ligandumok felhasználásával is sikerült nagy hatékonyságú és szelektivitású homogén és heterogén katalizátorrendszereket előállítani.
1.2. Foszfin-foszfit típusú ligandumok
Királis foszfin-foszfitot katalizátor-módosító ligandumként először Takaya és Nozaki alkalmaztak sztirol enantioszelektív hidroformilezési reakciójában. Az axiális kiralitású Binaphos-szal (4. ábra; a) módosított ródiumtartalmú katalizátorral rendkívül jó regio- és enantioszelektivitást értek el (88% elágazó láncú termék, 94%
ee).30
4. ábra Az első foszfin-foszfit ligandumok
Később a királis foszfin-foszfit típusú ligandumok katalitikus alkalmazása kiterjedt számos más reakciótípusra is, így például hidrogénezésre,31,30c,d,e,f
hidroborálásra,32 aszimmetrikus allil-helyzetű szubsztitúcióra,33 enantioszelektív hidrocianálásra,34 gyűrűnyitásos metatézis polimerizációs reakciókra,35 alternáló szén-monoxid-alkén kopolimerizációra,36 konjugált addíciós reakciókra37, illetve palládiumkatalizált hidrofoszforilálásra.38
A foszfin-foszfit típusú ligandumok két, eltérő koordinációs sajátságú foszforatommal rendelkeznek: a foszfinocsoportban lévő foszforatom jó σ-donor, míg a foszfit egységben lévő jó π-akceptor jelleggel bír. Természetesen a két foszforatom környezetének sztérikus jellemzői is nagyban különbözhetnek. Az utóbbi időben széles körben elterjedt a foszfin-foszfit ligandumok alkalmazása enantioszelektív hidrogénezési reakciókban. Számos prokirális szubsztrátummolekula aszimmetrikus redukcióját valósították meg kiemelkedően jó szelektivitással és aktivitással. Az elért ígéretes eredmények ellenére alkalmazásuk kevésbé elterjedt aszimmetrikus allil- helyzetű szubsztitúciós reakciókban. Lényeges megemlíteni továbbá, hogy a foszfin- foszfit típusú ligandumok többnyire egyszerűen előállíthatók könnyen hozzáférhető, olcsó kiindulási vegyületekből.
Zhang és munkatársai dehidroaminosav-észterek aszimmetrikus hidrogénezésében alkalmazták a katalizátor módosítására a Binaphos egyik származékát (4. ábra; b). A katalizátort in situ állították elő a ligandum és [Rh(COD)2]PF6 komplex felhasználásával, mellyel α-acetamido-akrilátok és különböző dehidrofenilalanin-származékok hidrogénezési reakcióiban több mint 99%-os enantioszelektivitást értek el.39
Később Chan és Yeung ferrocén alapú foszfin-foszfit ligandumot (5. ábra) állítottak elő, melyet dehidroaminosavak aszimmetrikus hidrogénezésében alkalmaztak.40 A katalizátort in situ készítették [Rh(COD)2]BF4 prekurzorból királis ligandummal. A reakció szelektivitása ebben az esetben nem mondható kiemelkedőnek, hiszen az elért legjobb optikai hozam is csak 89% volt, ugyanakkor enamidok aszimmetrikus hidrogénezése során, 87,5%-os enantioszelektivitással sikerült N-(1-feniletil)acetamidot előállítani.
5. ábra Ferrocén-vázas foszfin-foszfit ligandum
Monoszacharid alapú foszfin-foszfit ligandumokat (6. ábra) állítottak elő Claver és munkatársai.41,30c Az in situ képzett ródium-komplexeik (pl.
[Rh(COD)2]BF4-ból kiindulva) dehidroaminosavak aszimmetrikus hidrogénezési reakcióinak kiváló katalizátoraiként említhetők. Segítségükkel α-acetamido-akrilsav- metil-észter és (Z)-α-acetamido-fahéjsav-metil-észter aszimmetrikus hidrogénezése több mint 99%-os enantioszelektivitással valósítható meg.
6. ábra Monoszacharid-vázas ligandumok
Pizzano és kutatócsoportja fenilén- és etilén-vázas foszfin-foszfit ligandumokat (7. ábra) állítottak elő, melyek ródium-komplexeivel rendkívül jó enantioszelektivitást (több mint 99%-os) értek el (Z)-α-acetamido-fahéjsav-metil- észter aszimmetrikus hidrogénezése során.42,30g A ligandumok [IrCl(COD)2] prekurzorral képzett komplexei pedig iminek aszimmetrikus hidrogénezési reakciójában szolgáltattak jó eredményeket (72-85% ee).43 A vegyületek továbbá
kiváló eredményeket nyújtottak α,β-telítetlen enolészter foszfonátok (91-98%
ee),44,30f és 2-metil-kinolin (73% ee)45 aszimmetrikus hidrogénezési reakcióiban.
7. ábra Fenilén- és etilén-vázas foszfin-foszfit ligandumok
Van Leeuwen és munkatársai királis 1,3-propilén-vázzal rendelkező ligandumokat állítottak elő (8. ábra).30d Az új ligandumok között szerepeltek sztereogén foszforatomot tartalmazó vegyületek is. (Z)--Acetamido-fahéjsav-metil- észter és acetamido-akrilsav-metil-észter aszimmetrikus hidrogénezése során jó enantioszelektivitással (általánosan 90-99%) nyújtották a kívánt terméket. A tanulmány érdekes megállapítása, hogy a sztereogén foszforatom szerepe a reakció optikai hozamára csekély, alapvetően a vázban lévő sztereogén elem befolyásolja a reakció szelektivitását. Fontos megjegyezni, hogy, amennyiben a ligandum egynél több sztereogén elemmel rendelkezik, döntő jelentőségű lehet azok együttes, eredő hatása a reakció optikai hozamára.
A ligandum-család emelett jó szelektivitást nyújtott aszimmetrikus allil- helyzetű szubsztitúciós reakciókban is (83% ee).33
8. ábra Királis 1,3-propilén híddal rendelkező foszfin-foszfit ligandumok
Sztereogén elemekkel rendelkező, 1,2-diszubsztituált etilén-vázas foszfin- foszfit ligandumokat állított elő Vidal-Ferran és csoportja (9. ábra).46 Az új ligandumkönyvtár segítségével kiemelkedő aktivitással és enantioszelektivitással hidrogéneztek különböző dehidroaminosav-észtereket (99% ee), itakonsav- származékokat (99% ee), α,β-telítetlen enolészter foszfonátokat (92% ee)47 és 2- metilkinolint (93% ee).48 Kiváló példaként említhető, hogy a 3,4-bisz(acetoxi)-(Z)-- acetamido-fahéjsav-metil-észter (L-DOPA prekurzor) aszimmetrikus hidrogénezése 99%-os enantioszelektivitással valósítható meg.49 A diciklohexil-foszfino-csoporttal rendelkező ligandummal bizonyos szubsztrátumok (pl. telítetlen enolészter- foszfonátok) esetében jobb enantioszelektivitást értek el, mint difenil-foszfino- csoportot tartalmazó analógjával (9. ábra).50 A ligandumokkal módosított palládium- komplexek kielégítő enantioszelektivitással adták a (E)-1,3-difenilallil-acetát és dimetil-malonát aszimmetrikus allilezési reakciójának termékét (81% ee).51
9. ábra Királis etilén-vázas foszfortartalmú ligandumok
Börner és munkatársai tetrahidrofurán-vázas ligandumokat állítottak elő és vizsgáltak allil-acetát hidroformilezési reakciójában.52 A ródiumkatalizált folyamat során a legjobb regioszelektivitást (76/24 az elágazó láncú izomer javára) az a ligandummal, a legjobb enantioszelektivitást (44%) pedig a b vegyülettel érték el (10.
ábra).
10. ábra Tetrahidrofurán-vázas ligandumok
Bakos és kutatócsoportja különböző méretű kelátgyűrűk kialakítására képes foszfin-foszfit ligandumok platina-komplexeinek koordinációs sajátságait vizsgálta.53 Meglepő módon, az a ligandum (11. ábra) egy ekvivalens [Pt(CH3CN)2Cl2] komplexszel transz-[Pt(P-OP)2]Cl2 összetételű komplexet ad, mely vegyület körülbelül 25 óra alatt, szobahőmérsékleten rendeződik át cisz-[Pt(P-OP)Cl2] összetételű komplexxé. A folyamatban elsőként képződő termék tehát a kinetikai kontroll eredménye, mely később a nagyobb termodinamikai stabilitású vegyületté rendeződik át. A b ligandum esetében hasonló jelenséget nem tapasztaltak: az egyetlen képződő termék a cisz-[Pt(P-OP)Cl2] komplex volt (11. ábra). A kialakuló kelátgyűrű mérete tehát jelentős mértékben befolyásolhatja a ligandum koordinációs tulajdonságait.
11. ábra Különböző méretű kelátgyűrűk kialakítására képes foszfin-foszfit ligandumok
Breit és kutatócsoportja foszfabarralén-vázzal rendelkező katalizátor- módosító ligandumokat állított elő (12. ábra).54 A vegyületeket dehidroaminosavak ródium-katalizált aszimmetrikus hidrogénezési reakcióiban vizsgálták. A hidrogénezett termék jó hozammal és kielégítő enantioszelektivitással (88%) képződött.
12. ábra Foszfabarralén-vázas vegyületek
Müller és munkatársai foszfabenzol-alapú ligandumokat állítottak elő (13.
ábra).55 A vegyületeket (Z)-α-acetamido-fahéjsav-metil-észter és dimetil-itakonát ródiumkatalizált aszimmetrikus hidrogénezési reakciójában tesztelték. Az elért legjobb optikai hozamok elmaradnak más foszfin-foszfit típusú ligandumokkal elért eredményektől (rendre 62 és 78% ee).
13. ábra Foszfabenzol-alapú ligandumok
A ligandumok szintézisének egyik lényeges eleme a szerkezet tudatos és precíz megtervezése. A vegyületek modularitása nagyszámú új molekula előállítását teszi lehetővé, melyek közül azonban gyakran csak néhány bizonyul katalitikus szempontból megfelelőnek. A szintézis ugyanakkor az esetek többségében igencsak időigényes. A fenti nehézségekre kínál megoldást a Schmalz és kutatócsoportja által kidolgozott eljárás, mellyel – a kombinatorikus kémia lehetőségeit megragadva – nagyszámú értékes foszfin-foszfit típusú vegyület állítható elő (14. ábra).56 A vegyületek szintézisére kidolgozott eljárást később tökéletesítették.57 Az új ligandumok segítségével sztirol hidroborálási reakciójában 91%-os enantioszelektivitással állítottak elő 1-feniletanolt (14. ábra, a).32 A b ligandum felhasználásával Schmalz kiemelkedően jó szelektivitással állított elő egy antiszeptikus hatású vegyületet.58 Az elért enantioszelektivitás jobb volt, mint a vegyület szintéziséhez általánosan alkalmazott BINAP nyújtotta optikai hozam.
Fontos megemlíteni, hogy a TADDOL-egységet tartalmazó ligandumok általában jobb szelektivitással szolgáltatták a hidroborálási reakciók termékét, mint a binaftilcsoporttal rendelkező vegyületek.
14. ábra TADDOL-egységet tartalmazó ligandumok
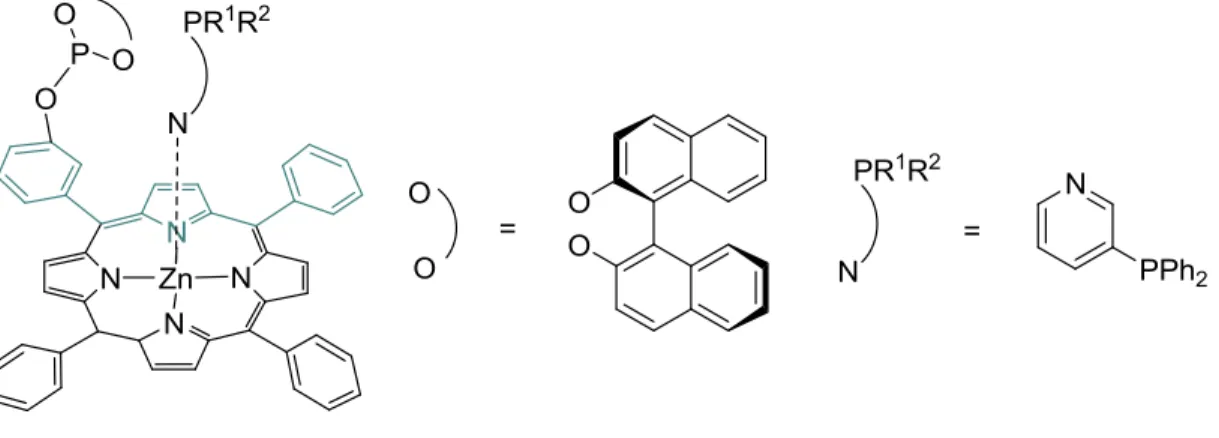
Van Leeuwen és Reek szupramolekuláris stratégiával előállított foszfin-foszfit ligandumokat (SUPRAPhos ligandumok) vizsgáltak difenilallil-acetát aszimmetrikus allil-helyzetű szubsztitúciós reakciójában (15. ábra).59 Az alkalmazott katalitikus rendszer 24 órás reakcióidő mellett teljes konverzióval és legfeljebb 70%-os
enantioszelektivitással adta a kívánt terméket. Az elért eredmények alapján bizonyították, hogy a koordinálódó donoratomok közötti híd hosszának rendkívüli hatása van a reakció szelektivitására. A ligandumok ugyanakkor rendkívül jó szelektivitást biztosítottak ciklohexenil-acetát kinetikai rezolválása során.60
15. ábra Szupramolekuláris stratégiával előállított foszfin-foszfit típusú ligandumok
1.3. Enantioszelektív szintézisek
Az enantioszelektív katalitikus szintézisekben a katalizátornak királis információt kell hordoznia. A királis információt hordozó katalizátor lehet fémet nem tartalmazó szerves molekula (organokatalízis), vagy átmenetifém-tartalmú vegyület (fémorganikus katalízis). Ez utóbbi esetben, a királis információ forrása lehet egy királis ligandumokkal módosított átmenetifém vagy akár egy királis ellenion (16.
ábra).
16. ábra Királis információt hordozó átmenetifém-komplexek
Érdekes megemlíteni továbbá a királis oldószer (pl. etil-(S)-laktát) használatát, hiszen az oldószer királis közegként befolyásolhatja a reakció sztereoszelektivitását.
Aszimmetrikus szintézisek során tehát a katalizátor által hordozott királis információ adódik át a szubsztrátummolekulának. Azt a folyamatot, melynek során a katalizátor királis információt ad át, aszimmetrikus indukciónak nevezzük.
1.3.1. A palládiumkatalizált aszimmetrikus allil-helyzetű szubsztitúció
Az aszimmetrikus allil-helyzetű szubsztitúció (Trost-féle AAA reakció) olyan szerves kémiai reakció, mely alkalmas szén-szén és szén-hetroatom (leggyakrabban O, N, S és P) σ-kötés enantioszelektív kialakítására. Az első enantioszelektív allil- helyzetű szubsztitúciós reakció Barry M. Trost nevéhez fűződik.61 Trost királis difoszfinnal módosított Pd(0)-komplexet alkalmazva kismértékű enantiomerikus dúsulást ért el. Az újabb és újabb katalizátor-módosító ligandumok megjelenésével és a reakció mechanizmusának beható tanulmányozásával a Pd-katalizált aszimmetrikus allil-helyzetű szubsztitúció egy intenzíven művelt kutatási területté vált. A Pd- katalizált reakció jelentőségét tovább növeli az a tény, hogy a katalitikus ciklus intermedierjei spektroszkópiai módszerekkel könnyen vizsgálhatók, a katalitikus ciklus jól ismert. (Más átmenetifém-katalizált (Rh, Mo, Ir, Cu, Ni, W stb.) allil- helyzetű szubsztitúciós reakciók esetében az intermedierek vizsgálata nehézkes, a ciklus lépései sok esetben még nem teljesen tisztázottak.) A folyamat további előnye, hogy sokkal enyhébb körülmények között megvalósítható, mint egy „hagyományos”
alifás SN1 vagy SN2 reakció.
A katalitikus ciklusban megjelenő intermedierek számát, és így a reakció mechanizmusát is meghatározzák az alkalmazott ligandum és szubsztrátum szimmetriaviszonyai. A továbbiakban a C1-szimmetriájú ligandummal és a C1 és C3 szénatomon azonos szubsztituenst tartalmazó „allil-szubsztrátummal” végrehajtott reakció mechanizmusát mutatom be (17. ábra).
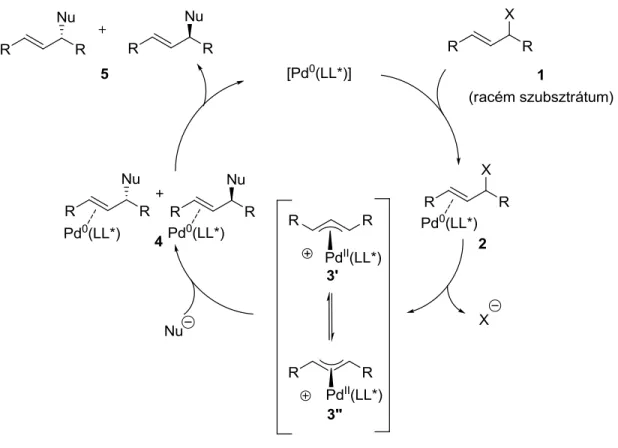
17. ábra Palládiumkatalizált aszimmetrikus allil-helyzetű szubsztitúciós reakció mechanizmusa (LL*: C1-szimmetriájú kétfogú ligandum)
A reakcióban elsőként az allilcsoportot tartalmazó szubsztrátummolekula koordinálódik a királis ligandumokkal rendelkező Pd0 központi atomhoz, melynek hatására izomer η2-π-allil-Pd0 komplexek (2) jönnek létre.62 A szubsztrátummolekula rendelkezik egy allil-helyzetű távozó csoporttal, ami legtöbbször acetát- vagy karbonátcsoport. A következő, oxidatív addíciós lépésben, a távozó csoport lehasad és két síknégyzetes szerkezetű η3-π-allil-PdII komplex (3) jön létre, melyek egymással egyensúlyban vannak. Amennyiben azonban az alkalmazott királis ligandum nem aszimmetrikus, hanem pl. C2-szimmetriával rendelkezik, akkor a kialakuló η3- komplexek között nincs különbség, azok teljesen azonosak.
Ezt követően az intermedierben az elektrofil PdII központi ion aktiválja az allilcsoport terminális helyzetű C-atomjait a nukleofil támadásával szemben. A nukleofil támadó ágens koordinálódik valamelyik terminális helyzetű, egymással
diasztereotóp viszonyban lévő C1- vagy C3-szénatomhoz, melynek eredményeként, reduktív eliminációval ismét kialakul egy η2-π-allil-Pd0 (4) komplex, amelyből eljuthatunk a termékhez (5).
Mind az oxidatív addíció, mind pedig a reduktív elimináció sztereoszelektíven, SN2 mechanizmus szerint, inverzióval játszódik le a megfelelő szénatomon, így, amennyiben izomerizációs folyamat jelenlétével nem kell számolni, a bruttó reakciót tekintve retencióról beszélhetünk. A nukleofil támadó ágens tehát az allilcsoport (3) által meghatározott sík ugyanazon oldalán lép be, ahonnan az X távozó csoport kilépett. Az aszimmetrikus allil-helyzetű szubsztitúció egyik érdekes sajátsága, hogy a reakció során – 4 disszociációjának kivételével – minden lépés felelőssé tehető az enantioszelekcióért az alkalmazott reakciókörülményektől függően. Amennyiben feltételezzük, hogy a reakció sebességmegatározó lépése a nukleofil ágens támadása, és eltekintünk egyéb izomerizációs jelenségektől, akkor a reakció enantioszelektivitása három momentum függvénye: (i) az intermedier η3-π- allil-PdII komplex (3) egyensúlyi összetételének (3’ és 3”), (ii) ezek reaktivitása közötti különbségnek, illetve (iii) a nukleofil támadás regioszelektivitásának.
A katalitikus ciklus során számolni kell bizonyos izomerizációs folyamatokkal is. Ezek közül a 3 intermedier egyensúlyát lehetővé tevő ún.
látszólagos allil-rotáció jelentőségét már említettem. Jelenlétével kizárólag különböző donoratomokat tartalmazó katalizátorrendszerek esetében kell számolni. A folyamat mechanizmusára többféle modell ismeretes.63 Ezek közül egy π-σ-π izomerizációval járó reakcióutat mutat be a 18. ábra.63a A látszólagos allil-rotáció – mely tényleg látszólagos, hiszen az allilcsoport „elcsavarodása” energetikailag nem kedvezményezett – ebben az esetben a σ-komplexben létrejövő Pd-C rotáció következménye.
18. ábra A látszólagos allil-rotáció egy feltételezett mechanizmusa
A fenti mechanizmushoz hasonló elv alapján játszódik le az ún. π-σ-π- izomerizáció.64 Lényeges eltérés azonban, hogy ez esetben nem a Pd-C kötés mentén történő rotáció, hanem a C1-C2 tengely körüli elfordulás okozza az izomer termékek (syn- és anti-izomerek: az R-csoport a C2-atomhoz kapcsolódó hidrogénnel rendre cisz- és transz-helyzetben van) megjelenését (19. ábra).
19. ábra A π-σ-π-izomerizáció mechanizmusa
Mindez azt is jelenti, hogy a π-σ-π-izomerizáció nem csak a végtermék optikai tisztaságát, hanem annak geometriai izomériáját is befolyásolhatja.
Jelenlétével persze csak abban az esetben kell számolni, ha az R-csoport elegendően kicsiny sztérikus igénnyel rendelkezik ahhoz, hogy az anti-izomer kialakulása bekövetkezzen (pl. metilcsoport). Természetesen az izomeregyensúly nagyban függ az alkalmazott ligandumtól is.
További izomerizációs lehetőségként említhető a Pd(0)-katalizált allil- kicserélődés.65 A folyamat során egy allilcsoportot nem tartalmazó, koordinatíve telítetlen Pd(0)-atom koordinálódik egy η3-π-allil-PdII intermedier megfelelő oldalához, melynek hatására – inverzióval – új Pd(II)-komplex képződik (20. ábra). A reakció bekövetkezésének esélye a katalizátor-komplex alacsony koncentrációjának köszönhetően kicsi.
20. ábra A Pd(0)-katalizált allil-kicserélődés mechanizmusa
1.3.2. A ródiumkatalizált aszimmetrikus hidrogénezés mechanizmusa
Aszimmetrikus hidrogénezéskor a szubsztrátum legtöbbször ún. prokirális alkén. A prokirális alkének olyan telítetlen molekulák, melyekből egy molekula hidrogén addíciójával királis termék keletkezik. A prokirális jelleg természetesen relatív tulajdonság, hiszen attól, hogy egy molekula például hidroformilezésre nézve prokirális, nem biztos, hogy a hidrogénezés tekintetében is az.
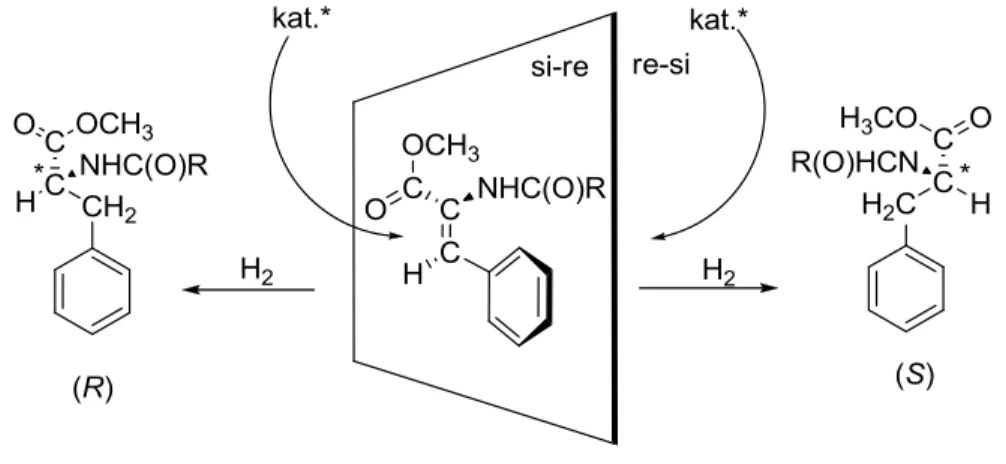
Enantioszelektív hidrogénezés során gyakran alkalmazott prokirális modellmolekula a (Z)-N-acetil--amino-fahéjsav-metil-észter (vagy (Z)--acetamido- fahéjsav-metil-észter). A molekulában lévő alkénes kettős kötés gátolja a C2-C3- rotációt, így az kétféle módon koordinálódhat a katalizátor-komplexhez. A molekula két oldalát, a Cahn-Ingold-Prelog-konvenció alapján, illethetjük a si-re és re-si jelzőkkel (21. ábra).
21. ábra A dihidrogén addíciója a prokirális alkén két oldalára
Az aszimmetrikus hidrogénezés alapja tehát első közelítésben az, hogy a katalizátor különbséget tesz a szubsztrátummolekula két oldala között. A szubsztrátum-katalizátor-komplex „két formában” létezik, amelyek egymással diasztereomer viszonyban vannak, így különböző sebességgel keletkezhetnek vagy különböző sebességgel reagálhatnak a hidrogénnel, mely eredményeként különböző mennyiségben keletkeznek a termékek. Mindez azt eredményezi, hogy a reakció kisebb-nagyobb mértékben enantioszelektív lesz.
Az irodalmi adatok alapján megállapítható, hogy a reakciók optikai hozama sőt maga a reakció mechanizmusa is függ a királis katalizátor-módosító ligandum minőségétől, de talán még ennél is döntőbb jelentőségű a hidrogénezendő olefin szerkezete. Az egyszerű poláris funkcióscsoportot nem tartalmazó olefinek hidrogénezésének optikai hozama például általában csekély. A reakció szelektivitását növeli, ha a telítetlen vegyület -szénatomján elektronakceptor csoport van, különösen karboxilcsoportok esetében, de a legkiválóbb modellvegyületek azok (például az -acil-amino-fahéjsav-származékok), amelyek a ródiummal több ponton léphetnek kölcsönhatásba, kelátgyűrűt létrehozva ezzel.
Az aszimmetrikus hidrogénezés mechanizmusát elsőként Jack Halpern és John M. Brown derítette fel részleteiben.66 A Halpern-Brown-mechanizmus szerint, a katalitikus folyamat első lépéseként a katalizátor-komplexben a dién hidrogéneződik, és oldószerkomplex képződik (22. ábra). A vizsgált katalitikus reakciókban metanolt
alkalmaztak oldószerként. A következő lépésben az oldószert a kétfogú ligandumként viselkedő szubsztrátum helyettesíti (23. ábra).
22. ábra A dién „hidrogéneződése”
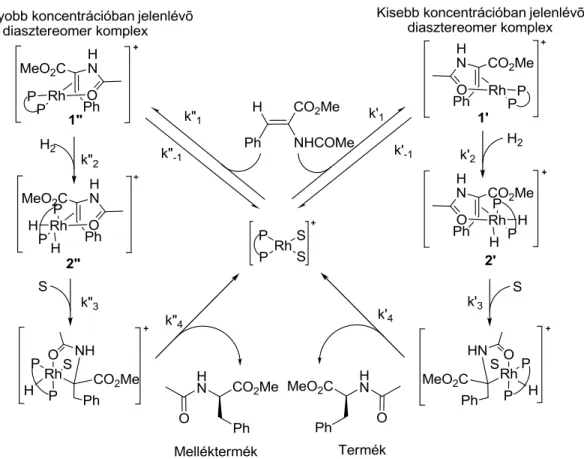
A képződött kétféle, négyzetes, planáris szerkezetű, egymással diasztereomerikus viszonyban lévő szubsztrátum komplexekre a dihidrogén cisz- addícióval addícionál, a kisebb koncentrációban jelenlevő diasztereomer azonban nagyságrendekkel gyorsabban reagál a hidrogénnel.67 A hidrogén oxidatív addícióját a hidrogén beékelődése követi, mely a β-helyzetű szénatomot érinti, míg az α- szénatom a ródiumhoz kapcsolódik. Az így keletkező monohidrido-ródium- komplexből reduktív eliminációval képződik a két enantiomer. Ez a lépés új utat nyit a következő katalitikus ciklus számára (23. ábra).
A mechanizmus alapfeltevései szerint – melyek kísérletileg is igazolhatók – (i) a hidrogén oxidatív addíciója irreverzibilis folyamat, illetve (ii) a hidrogén endo- helyzetben reagál cisz-addícióval a szubsztrátum molekulával. Mindezek alapján könnyen belátható, hogy a szubsztrátum koordinációja során képződő diasztereomerek, illetve a keletkező termékek (enantiomerek) sztereokémiája között közvetlen kapcsolat áll fenn. Halpern két esetben közvetlen mérési módszerekkel (NMR spektroszkópia és röntgendiffrakció segítségével) is bizonyította a vázolt mechanizmus érvényességét. Lényeges azonban megemlíteni, hogy a legtöbb esetben a katalitikus rendszer direkt módszerekkel történő tanulmányozása rendkívül bonyolult. A bemutatott mechanizmus segítségével azonban további következtetések vonhatók le, melyek kísérleti igazolása indirekt módon támaszthatja alá a mechanizmus érvényességét. Ilyen indirekt módszerként említhető a nyomás és a hőmérséklet hatásának vizsgálata.
Megfelelően nagy hidrogénnyomás mellett (k2[H2][szubsztrátumkomplex] >>
k-1[szubsztrátumkomplex]) a folyamat sztereoszelektivitását a k’1/k”1 arány szabja meg. Mindez jól magyarázza a nyomásnövelés hatására bekövetkező enantioszelektivitás-csökkenést. A hőmérséklet hatásának vizsgálatához lényeges megemlíteni, hogy – miként az már kiderült – a reakció nagy szelektivitása a diasztareomer viszonyban lévő katalizátor-szubsztrátum komplexek (hidrogénnel való reakciójuk sebességéhez viszonyított) gyors egyensúlyának következménye.
Mivel ez az egyensúlyi átalakulás általában nagyobb aktiválási entalpiájú, mint a komplex hidrogénnel történő reakciója, így a folyamat megfelelően alacsony hőmérsékleten „befagyasztható”. Feltéve, hogy a nagyobb koncentrációban jelenlévő, kevésbé reaktív diaszteromer reagál hidrogénnel (ami igaz, hiszen az enantioszelektivitás kisebb, mint 100%), elmondható, hogy az optikai hozam csökken a hőmérséklet csökkentésével.
23. ábra Az enantioszelektív hidrogénezés Halpern-Brown-féle mechanizmusa
Fontos megállapítás, hogy a reakció sebességmeghatározó lépése szobahőmérsékleten a hidrogén oxidatív addíciója. A reduktív elimináció aktiválási entalpiája azonban elegendően nagy ahhoz, hogy alacsonyabb hőmérsékleten (-40
°C) ez a folyamat váljon a sebességmeghatározó lépéssé. Halpern és munkatársai ezt a jelenséget felhasználva alacsony hőmérsékleten NMR spektroszkópia segítségével bizonyították a monohidrido-ródium-komplex jelenlétét a katalitikus ciklusban.
Az egyetlen intermedier, melyet ez idáig nem sikerült kimutatni és jellemezni, a hidrogén oxidatív addíciójával keletkező szubsztrátum-dihidrido-komplex.
Létezésére a ródium(I)-hez hasonló d8-elektronkonfigurációjú átmenetifém-ionok hasonló aktiválási paraméterekkel rendelkező reakcióiból következtethetünk.
A Halpern-Brown-féle mechanizmus alapján tehát elmondható, hogy az enantioszelektív szintézis kritériuma az, hogy a prokirális szubsztrátum kétféle koordinációja révén kialakuló intermedierek – amelyek egymásnak diasztereomerjei – a további reakció során különböző sebességgel alakuljanak át. A termék kiralitását nem a szubsztrátum egyik oldalának kedvezőbb koordinációja, hanem a kisebb koncentrációjú diasztereomer nagyobb reakciókészsége határozza meg.
A reakció aszimmetrikus voltának feltétele tehát a diasztereomerek eltérő reaktivitása a hidrogénnel szemben. Az 1 diasztereomer komplexek stabilitása közötti különbség jól magyarázható a királis ligandum által létrehozott aszimmetrikus környezet jelenlétével, mely a szubsztrátum egyik vagy másik oldalának koordinációját kedvezőbbé teszi. Ez a klasszikus „kulcs-zár” modell azonban nem ad kielégítő magyarázatot a diasztereomerek hidrogénnel szembeni eltérő reaktivitására.
Jóllehet nem meglepő, hogy a nagyobb termodinamikai stabilitású komplex reaktivitása kisebb, azonban a stabilitás-különbség önmagában nem ad kielégítő magyarázatot a reakciók enantioszelektivitására, ahhoz ugyanis sokkal nagyobb stabilitásbeli eltérésre lenne szükség. Feltehetően a kisebb stabilitású 1’
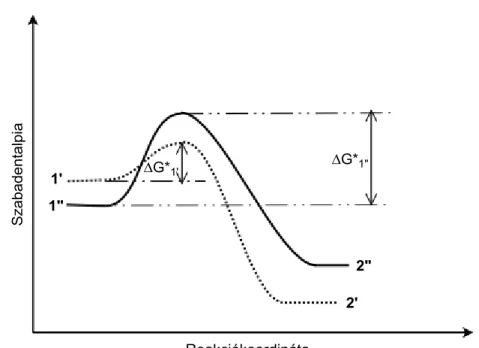
szubsztrátum-komplex valamivel kisebb aktiválási szabadentalpiával alakul át diasztereomerjénél a nagyobb stabilitású 2’ dihidrido-komplexszé. A keletkezett 2 jelű komplexek stabilitása tehát éppen ellentétes a kiindulási 1 jelű komplexek stabilitásához képest (24. ábra).
24. ábra Az aszimmetrikus hidrogénezés „hajtóereje”
A 100%-os enantioszelektivitást megközelítő katalitikus rendszerek esetében óriási aktiválási szabadentalpia-különbséget (ΔΔG*) kell a katalizátornak biztosítania. A ΔΔG* = -RTlnE (E: enantiomerarány, E = [R]/[S]) képlet segítségével például megmutatható, hogy nagyobb enantioszelektivitás tartományban az ugyanakkora optikai hozam-változás sokkal nagyobb szabadentalpia-különbség biztosítását igényli. Az enzimatikus szelektivitást megközelítő hidrogénező katalizátorok szerkezeti finomhangolása révén bekövetkezett, jelentéktelennek tűnő enantioszelektivitás-változás mögött tehát rendkívüli katalitikus teljesítmény nyugszik.
Fontos azonban megjegyezni, hogy az aszimmetrikus hidrogénezés Halpern- Brown-féle mechanizmusa, nem általános érvényű, nem alkalmazható minden katalitikus rendszerre. Imamoto és Gridnev kutatásai nyomán kiderült, hogy erősen bázikus karakterű difoszfin ligandumokkal módosított ródiumtartalmú katalizátorok esetében, α-dehidroaminosavak hidrogénezése során, a dihidrogén oldószerkomplexre történő addíciója megelőzheti a szubsztrátum koordinációját.68 A Halpern-Brown-mechanizmussal („unsaturated-modell”) szemben, ezen új elképzelés
(„dihydride-modell”) szerint a reakció sebességmeghatározó lépése az olefin koordinációja a dihidrido-komplexhez. A mechanizmus egyik érdekes következménye, hogy a nyomás növelésének hatására a reakció sebessége ugyan növekszik, hiszen nő az oldószer-dihidrido-komplex koncentrációja, azonban az enantioszelektivitás elvben állandó marad, értéke nem csökken. A jelenség azzal magyarázható, hogy a dihidrogén addícióját követő lépésben keletkező, diasztereomer viszonyban lévő oktaéderes szubsztrátum-dihidrido-komplexek aránya független a nyomástól, így a belőlük keletkező termékek mennyisége is független marad.
Heller és munkatársai β-acilamino-akrilátok hidrogénezésének vizsgálata során megállapították, hogy a Halpern-Brown-mechanizmussal ellentétben, a főtermék nem a kisebb koncentrációban jelenlévő síknégyzetes szubsztrátum- komplexből származtatható, hanem a nagyobb mennyiségben előforduló disztereomer hidrogénnel történő reakciójának eredménye.69 A mechanizmus egyik érdekessége, hogy magyarázatot adhat a nyomás emelése hatására bekövetkező enantioszelektivitás-emelkedésre, hiszen a nagyobb koncentrációban jelenlévő diszetereomer reagál gyorsabban a dihidrogénnel. A reakció sebességmeghatározó lépése szobahőmérsékleten ez esetben is – akár a Halpern-Brown-mechanizmus esetén – a hidrogén oxidatív addíciója.
A bemutatott lehetséges mechanizmusok kiváló bizonyítékai annak, hogy az aszimmetrikus hidrogénezés alapvetően kinetikai folyamatok eredője. A reakció aktivitásának és szelektivitásának növelése érdekében a reakciókörülmények gondos megválasztása szükséges. Jóllehet számos esetben a kísérleti megfigyelések nem igazolják a Halper-Brown-féle mechanizmus alapfeltevéseit, az elmélet azonban az aszimmetrikus hidrogénezési reakciók jelentős részét jól leírja, alkalmazása mindmáig általánosan elterjedt.
1.4. Foszfin-foszfit ligandumok sztereo-elektronikus tulajdonságai
A ligandumok sztérikus és elektronikus tulajdonságainak vizsgálata, illetve ezek katalitikus folyamatokra gyakorolt hatásának tanulmányozása rendkívül fontos a katalizátorok szerkezeti finomhangolása érdekében. A sztérikus és elektronikus jellemzők természetesen szorosan összefüggnek, megváltoztatásuk külön-külön nem lehetséges. A továbbiakban az egyszerűbb áttekinthetőség érdekében mégis külön fejezetekben esik szó a foszfortartalmú ligandumok sztérikus és elektronikus tulajdonságairól.
1.4.1. Sztérikus sajátságok
A háromértékű foszforvegyületek esetében a foszforatom sp3-hibridizációjú, továbbá a foszfor magános elektronpárjának köszönhetően a molekula téralkata trigonális piramis. Ez a téralkat lehetőséget ad egy ún. kúpszög (cone angle) vizsgálatára, mely egy komplexben lévő foszforatomhoz kapcsolódó szubsztituensek térkitöltéséről, elhelyezkedéséről és sztérikus sajátosságairól ad felvilágosítást. Ha egy ligandum kúpszöge 180°, akkor az a komplex egyik oldalát teljesen „lefedi”.
A háromértékű foszforvegyületek jellemzésére leggyakrabban a Tolman-féle kúpszöget használják. A Tolman-féle kúpszög (Θ) C3 és C3v szimmetriájú ligandumok esetében annak a képzeletbeli kúpnak a nyílásszöge, melynek tengelye a molekula C3 tengelyével egybeesik, csúcsa a foszforatom nemkötő elektronpárjának irányában, az atommagtól 2,28 Å távolságra helyezkedik el, és palástja érinti a foszfor vegyértékeit lekötő csoportok van der Waals-sugár szerinti felületét (25.
ábra).70
25. ábra Egy trialkil-foszfin kúpszöge (Θ)
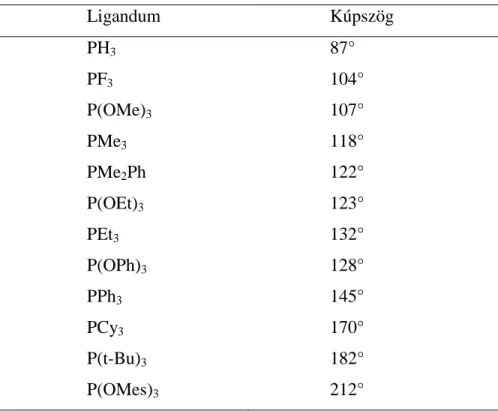
A kúpszög nagyságát jelentős mértékben befolyásolja a foszforon lévő szubsztituensek mérete, elhelyezkedése, hiszen ha a szubsztituens nagyobb térkitöltésű, akkor az adott vegyület kúpszöge is nagyobb. Ezen megállapításokkal összhangban vannak az 1. táblázat adatai.
1. táblázat Néhány egyfogú foszfin és foszfit ligandum kúpszöge71
Ligandum Kúpszög
PH3 87°
PF3 104°
P(OMe)3 107°
PMe3 118°
PMe2Ph 122°
P(OEt)3 123°
PEt3 132°
P(OPh)3 128°
PPh3 145°
PCy3 170°
P(t-Bu)3 182°
P(OMes)3 212°
Figyelemreméltó az a tény, hogy azonos R-csoportokat tartalmazó foszfin és foszfit ligandumok esetében a foszfitok kúpszöge kisebb. Az azonos R-csoportokkal rendelkező ligandumok kúpszögének különbözősége annak köszönhető, hogy a
foszfitok esetében az oxigénatom egyfajta „lazító”, illetve feszültségcsökkentő (spacer) szereppel bír.
Jóllehet a Tolman-féle kúpszöget először egyfogú ligandumok jellemzésére definiálták, azonban alkalmazható koordinált kétfogú ligandumok térigényének jellemzésére is. Az egyes kúpszögértékek a legtöbb molekula esetében egyszerű méretarányos molekulamodell segítségével is meghatározhatók.
1.4.2. Elektronikus sajátságok
A foszfor-fém koordinatív kötés, ahogy az az alkén- és a karbonil- ligandumokat tartalmazó fémorganikus komplexek esetében is megfigyelhető, két komponensből tevődik össze. A foszfor-fém kötés egyik komponense egy σ-donor kapcsolat, amely a foszfor magános elektronpárja és a fématom egyik üres d- atompályája között alakul ki. A második komponens a viszontkoordináció: a fématom egyik betöltött orbitálja és a ligandum egyik üres pályája közötti kapcsolat.
A ligandum betöltetlen orbitáljaként említhető a P-R σ-kötés lazító pályája (σ*-orbitál), vagy a foszforatom egyik üres d atomi orbitálja. Megállapodás szerint azonban az előbbi eset az elfogadott, ami érthető is, hiszen a d-pálya energiája relatíve túl nagy lenne ahhoz, hogy ott a viszontkoordináció bekövetkezzen (26.
ábra).71b
A foszforatom elektronikus jellemzőit a hozzá kapcsolódó szubsztituensekkel befolyásolhatjuk. Amennyiben a kapcsolódó csoportok nagyobb elektronegativitásúak (negatív induktív effektusúak, pl. halogének, alkoxi- vagy aminocsoportok), akkor a ligandum elektronküldő képessége csökken, ugyanakkor a molekula σ*-orbitáljának energiája is csökken, így megnő a viszontkoordináció mértéke. Fordított esetben, ha elektronküldő csoportok helyezkednek el a foszforatomon (pozitív induktív effektusúak, pl. alkil- vagy arilcsoportok), akkor a ligandum σ-donor képessége nő, míg a viszontkoordináció mértéke csökken.
Újabb fogalmak bevezetésével tehát elmondható, hogy az egyes ligandumok σ-donor sajátsága és -savassága egymással „antiparalel” viszonyban áll. Mindezen
információk tudatában egy elméletileg is igazolható, empirikus ligandum-sor állítható fel (27. ábra).
26. ábra A foszfor-fém koordinatív kötés kialakulása
Az általunk vizsgált foszfin-foszfit típusú vegyületek esetében tehát két különböző elektronikus sajátságú foszforatom található meg egyetlen molekulán belül. A foszfit egység foszforatomja (a hozzá kapcsolódó oxigénatomok hatására) erős π-akceptor sajátságú, míg a foszfiné jó σ-donor jelleggel bír.
27. ábra Foszfortartalmú vegyületek elektronikus tulajdonságainak változása
A foszforatom bázicitását illetően rendkívül informatív a megfelelő foszfin- szelenid (R3P=Se) vagy szelenofoszfát ((RO)3P=Se) típusú vegyületek 31P{1H} NMR spektrumából meghatározható 1J(31P,77Se) csatolási állandó, melynek nagysága fordítottan arányos a foszforatom σ-donor sajátságával.72 A 1J(31P,77Se) csatolási állandók és a megfelelő P(III)-vegyületek elektronikus sajátságai közötti összefüggés az NMR spektroszkópiában ismeretes Fermi-kontaktus kölcsönhatás73 és Bent- szabály74 segítségével magyarázható. A Fermi-kontaktus kölcsönhatás következménye, hogy minél nagyobb egy adott kötésben résztvevő atomok kötő elektronjainak s-karaktere, a magok közötti csatolás mértéke is annál nagyobb. A Bent-szabály kimondja, hogy az atomi orbitálok s-karaktere azon irányokban összpontosul, melyek elektropozitív elemek felé mutatnak. A foszfit egységben lévő foszforatom esetében például, a foszforatom oxigénatomok felé irányuló orbitáljainak p-karaktere – az oxigén elektronegatív jellege folytán – nagyobb, így a négy hibrid atomi orbitál közül a nemkötő pálya s-karaktere nő meg. Az ezzel az orbitállal kötést kialakító szelénatom csatolása jóval nagyobb lesz, mint a foszfinocsoport esetében.
A megfelelő szelén-vegyületek könnyen előállíthatók a ligandum és elemi szelén felhasználásával akár szobahőmérsékleten is. Lényeges megemlíteni, hogy a foszfin-foszfit típusú vegyületek eltérő elektronikus sajátságú foszforatomjainak reaktivitása eltér, így a ligandum egymást követő reakciókban egyesül szelénnel (28.
ábra).42
28. ábra Foszfin-foszfit reakciója elemi szelénnel
A mérendő csatolási állandók – az NMR-aktív 77Se izotóp 7,63%-os relatív természetes gyakoriságának köszönhetően – szatelit jelek segítségével határozhatók meg.
A 2. táblázat adatai alapján jól látható, hogy a nagyobb elektonsűrűségű arilcsoportokkal szubsztituált foszfinok 1J(31P,77Se) csatolási állandója kisebb.
Ugyanakkor látható, hogy a több elektonküldő csoportot tartlamazó foszforatom bázicitása nagyobb.
2. táblázat Tercier foszfinok szelenidjeinek 1J(31P,77Se) csatolási állandói75
Foszfin 1J(31P,77Se) (Hz)
PPh3 729,4
725,6
723,3
722,2
723,6
721,7
718,0
P(OPh)3 1024
1010