[Ru(LL)(CN)
4]
2-típusú komplexek fotofizikai és foto- kémiai tulajdonságai
Doktori (PhD) értekezés
Pannon Egyetem Kémia Doktori Iskola
Készítette:
Kovács Margit okleveles vegyészmérnök
Témavezető:
Dr. Horváth Attila egyetemi tanár
Pannon Egyetem, Kémia Intézet
Általános és Szervetlen Kémia Intézeti Tanszék Veszprém, 2007
[RU(LL)(CN)4]2- TÍPUSÚ KOMPLEXEK FOTOFIZIKAI ÉS FOTOKÉMIAI TULAJDONSÁGAI
Értekezés doktori (PhD) fokozat elnyerése érdekében Írta:
Kovács Margit
Készült a Pannon Egyetem Kémia Doktori iskolája/
Szervetlen fotokémia programja keretében Témavezető: Dr. Horváth Attila
Elfogadásra javaslom (igen / nem)
(aláírás) A jelölt a doktori szigorlaton …... % -ot ért el,
Az értekezést bírálóként elfogadásra javaslom:
Bíráló neve: Dr. Lente Gábor igen /nem
……….
(aláírás) Bíráló neve: Dr. Demeter Attila igen /nem
……….
(aláírás)
A jelölt az értekezés nyilvános vitáján …...% - ot ért el
Veszprém/Keszthely, ……….
a Bíráló Bizottság elnöke A doktori (PhD) oklevél minősítése…...
………
Az EDT elnöke
Tartalomjegyzék
Ábrajegyzék ... 5
Táblázatjegyzék ... 7
Köszönetnyilvánítás... 11
Bevezetés... 12
1. Irodalmi összefoglaló... 14
1.1 A [tetraciano-monodiimin-rutenát(II)]-komplexek előállítása... 14
1.2 A [Ru(LL)(CN)4]2- komplex fotofizikai tulajdonságai ... 16
1.3 Szolvatokromizmus ... 20
1.4 A [Ru(bpy)(CN)4]2- sav-bázis egyensúlya alap és gerjesztett állapotban ... 23
1.5 Energia- és elektronátadás... 25
1.5.1 Elektronátadás ... 25
1.5.2 Energiaátadás kovalens kötésű rendszerekben... 26
1.5.3 Energiaátadás hidrogénkötésű rendszerekben ... 27
1.5.4 NIR érzékenyítés [Ru(LL)(CN)4]2- komplexekkel... 30
1.6 Példák gyakorlati alkalmazásra ... 31
1.6.1 [Ru(bpy)(CN)4]2- mint páratartalom-érzékelő... 31
1.6.2 Tetraciano-monodiimin-Ru(II) komplex fotoelektrokémiai cellában ... 32
2. Kísérleti rész ... 33
2.1 Felhasznált anyagok ... 33
2.2 Mérőműszerek és módszerek ... 33
2.3 Preparatív eljárások ... 36
3. Eredmények és értékelésük ... 40
3.1 Az előállított komplexek jellemzése ... 40
3.1.1 NMR színképek... 40
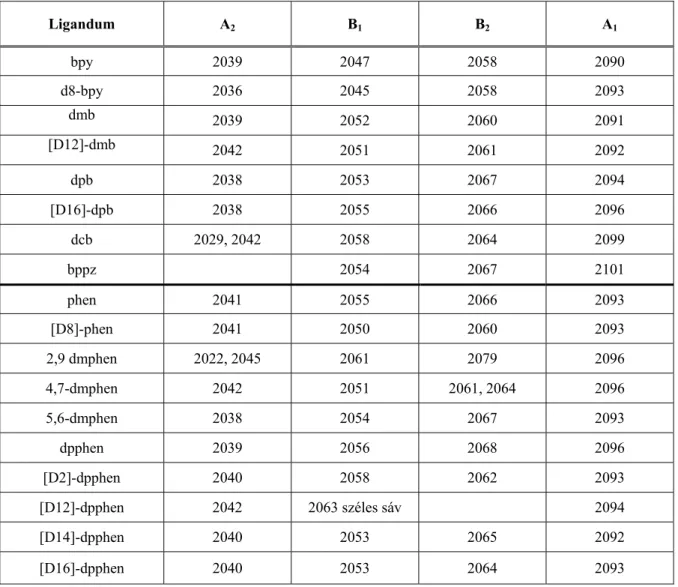
3.1.2 IR színképek ... 40
3.2 Elnyelési színképek és értelmezésük... 42
3.2.1 A bipiridilligandum és származékainak komplexei... 42
3.2.2 A fenantrolinligandum és származékainak komplexei ... 44
3.3 A gerjesztett komplexek fotofizikai tulajdonságai... 46
3.3.1 Kisugárzási színképek szobahőmérsékleten... 46
3.3.2 Szilárd mátrixban, 77 K-en mért kisugárzási színképek ... 48
3.3.3 A színképek Franck-Condon analízise ... 49
3.3.4 A fotofizikai folyamatok sebességének meghatározása... 53
3.3.5 A diiminligandumok hatása a fotofizikai folyamatokra ... 55
3.3.5.a A lumineszcencia-élettartamok és kvantumhasznosítási tényezők ... 55
3.3.5.b A diiminligandum hatása a hőmérséklettől független sugárzásmentes energiavesztési folyamatra ... 56
3.3.5.c A hőmérsékletfüggő folyamatok ... 59
3.3.5.d A diiminligandumok deuterálása... 61
3.3.6 Az oldószerdeuterálás hatása a fotofizikai folyamatok sebességére... 62
3.3.6.a Az oldószer- és ligandumdeuterálás hőmérsékletfüggésének együttes kiértékelése... 65
3.4 A [Ru(dcb)(CN)4]4- és [Ru(bppz)(CN)4]2- komplexek protonálódási egyensúlyai alap és gerjesztett állapotban... 67
3.4.1 A [Ru(bppz)(CN)4]2- komplex sav-bázis egyensúlya... 67
3.4.1.a Fotometriás titrálás ... 67
3.4.1.b Protonálódás követése 13C-NMR spektroszkópiával... 70
3.4.2 A [Ru(dcb)(CN)4]4- komplex sav-bázis egyensúlya... 71
3.4.2.a Fotometriás titrálás ... 71
3.4.2.b A sav-bázis egyensúly követése 13C-NMR spektroszkópiával... 73
3.4.3 A [Ru(dcb)(CN)4]4- és [Ru(bppz)(CN)4]2- komplexek protonálódási egyensúlyai gerjesztett állapotban... 75
3.4.3.a [Ru(bppz)(CN)4]2- komplex sav-bázis egyensúlya gerjesztett állapotban ... 75
3.4.3.b [Ru(dcb)(CN)4]4- komplex sav-bázis egyensúlya gerjesztett állapotban. 76 4. Összefoglalás ... 80
5. Tézisek ... 82
6. Theses ... 85
7. Irodalomjegyzék ... 88
Ábrajegyzék
1. ábra. Az eddig előállított [Ru(LL)(CN)4]2- komplexekben felhasznált diiminligandumok és rövidítéseik. ... 15 2. ábra. A [Ru(bpy)(CN)4]2- elnyelési és korrigált kisugárzási színképe szobahőmérsékleten vízben. .
... 17 3. ábra. A [Ru(bpy)(CN)4]2- egyszerűsített Jablonski-diagramja ... 19 4. ábra. A [Ru(pyr1bpy)(CN)4]2- komplex energiaszint-diagramja, víz, metanol és acetonitril
oldószerben [14]. ... 26 5. ábra. 1,5,9,13,17,21,25,29-oktaaza-ciklodotriaeikontán ([32]-ane-N8H88+)... 27 6. ábra. Szubsztituált ciklámszármazékok, melyeket hidrogénkötés révén kapcsolták a
[Ru(bpy)(CN)4]2- komplexhez... 29 7. ábra. A {[Ru(bpy)(CN)4]2-·(2H+)dendrimer} ’logikai kapu’ igazságtáblája. Az input sav vagy/és
lúg hozzáadása, az output az emisszió intenzitása (a) λ=330 és (b) λ=670 nm-en. ... 30 9. ábra. A K2[Ru(bpy)(CN)4] és a K2[Ru([D8]-bpy)(CN)4] IR színképe KBr pasztillában a cianid-
vegyértékrezgések tartományában... 42 10. ábra. A [Ru(LL)(CN)4]2- elnyelési színképei vízben szobahőmérsékleten, LL=bpy, dmb, dpb, dcb
és bppz... 43 11. ábra. A [Ru(LL)(CN)4]2- elnyelési színképei vízben szobahőmérsékleten, LL=phen származékok.
... 45 12. ábra. A [Ru(LL)(CN)4]2- komplexek normalizált kisugárzási színképei 298 K-en oxigénmentes
vízben. ... 47 13. ábra. A [Ru(LL)(CN)4]2- komplexek elnyelési és kisugárzási színkép maximumaiból számítható
Stokes-eltolódások az MLCT sávenergiája függvényében. A piros négyzet a
[Ru(dpphen)(CN)4]2-, a zöld háromszög a [Ru(2,9-dmphen)(CN)4]2- komplex értékei. ... 48 14. ábra. A [Ru(LL)(CN)4]2- komplexek 77 K-en mért korrigált kisugárzási színképei etanol-metanol
(4:1) oldószer elegyben. ... 49 15. ábra. A 0-0 vibrációs szinteknek megfelelő emissziós energia (E00) függése a hőmérséklettől
[Ru(bpy)(CN)4]2- komplex esetében, CH3OH/C2H5OH (○) és CH3OD/C2H5OD (●) oldószer elegyben... 49 16. ábra. A [Ru(phen)(CN)4]2- 77K-en mért kisugárzási színképének illesztése... 50 17. ábra. A Franck-Condon analízisből származtatott E00 paraméter függése a Huang-Rhys faktortól.
Az illesztett egyenesek paraméterei: 4115.4SM + 13918 cm-1 (R2= 0.9659) phen sorozatra és 4284.9SM + 13153 cm-1 (R2 = 0.9971) bpy sorozatra. ... 51 18. ábra. A dpb, dotb (4,4’-di-o-tolil-2,2’-bipiridin) és a dpphen ligandumok egyszerű geometria
optimalizációval (Hiperchem) kapott rajza... 52 19. ábra. A [Ru(LL)(CN)4]2- komplexek reciprok-élettartamának hőmérsékletfüggése L=bpy (●), dmb (▲), dcb (□), dpb (▲)... 57
20. ábra. A [Ru(LL)(CN)4]2- komplexek reciprok-élettartamának hőmérsékletfüggése L=phen (●), dpphen (▲), 4,7-dmphen (□), 2,9-dmphen (▲), 5,6-dmphen (■). ... 58 21. ábra. Az energiarés (E0) és a gerjesztett állapot torzulásának hatása a vibrációs
hullámfüggvények átlapolására. (A.) nagy torzulás és nagy energiarés, (B.) kis torzulás nagy energiarés, (C.) kis energiarés és kis torzulás. Forrás: [53] ... 58 22. ábra. A dpphen ligandum különböző mértékben deuterált származékainak sematikus rajza. ... 61 23. ábra. A [Ru(bpy)(CN)4]2- komplex reciprok-élettartamának hőmérsékletfüggése CH3OH-ban
(○),CH3OD-ban (▲) és CD3OD-ban ()... 64 24. ábra. A [Ru(bpy)(CN)4]2- komplex és az oldószermolekulák közti H-kötés sematikus ábrázolása.
... 65 25. ábra. A K2[Ru(bppz)(CN)4] elnyelési színképe különböző pH értékeknél... 68 26. ábra. A K2[Ru(bppz)(CN)4] komplex és protonált származékainak számolt színképe. ... 69 27. ábra. [Ru(dcb)(CN)4]4- komplex elnyelési színképe különböző pH értékeknél. (a) pH=4,8-2,4 és
(b) pH=2,0-0,1. ... 72 28. ábra. A [Ru(dcb)(CN)4]4- komplex és protonált származékainak számolt színképe... 73 29. ábra. A [Ru(dcb)(CN)4]4- komplex 13C kémiai eltolódásának változása a C4, a karboxilcsoportok
és a cianidligandumok vonalai esetében. ... 74 30. ábra. [Ru(bppz)(CN)4]2- komplex relatív emissziójának változása a pH függvényében és a
kiindulási (Ru) és az egyszer protonált (RuH) származékok parciális móltörtjei alapállapotban. Belső ábra: A komplex lumineszcencia-élettartamának változása a pH függvényében... 75 31. ábra. A [Ru(bppz)(CN)4]2- komplex lumineszcenciájának kioltása a hidrogénion-koncentráció
függvényében (KSV=659,5, R2=0,9990)... 76 32. ábra. A [Ru(dcb)(CN)4]4- komplex kisugárzási színképének változása a pH függvényében. A
gerjesztés hullámhossza: 427 nm. ... 77 33. ábra. A [Ru(dcb)(CN)4]4- komplex 666 nm-en mért relatív emissziójának változása a pH
függvényében és a különböző mértékben protonált termékek parciális mólhányada alapállapotban. Relatív emisszióintenzitás (▲), [Ru(dcb)(CN)4]4- (□), [Ru(dcbH)(CN)4]3- (∆), [Ru(dcbH2)(CN)4]2- (○) és [Ru(dcbH2)(CN)2(CNH)2] (×) komplex parciális
mólhányada. ... 78
Táblázatjegyzék
1. táblázat A [Ru(LL)(CN)4]2- komplexek előállításának különböző lehetőségei. A ligandumok szerkezetét az 1. ábra tartalmazza... 16 2. táblázat Néhány [Ru(LL)(CN)4]2- komplex fotofizikai adatai vízben, szobahőmérsékleten... 20 3. táblázat A [Ru(bpy)(CN)4]2- elnyelési valamint kisugárzási színképeinek maximumai és a [Ru(III)/Ru(II)]
redoxipotenciál értékei különböző oldószerekben. (Fc=ferrocén) ... 21 4. táblázat A K2[Ru(bpy)(CN)4] protonálódási egyensúlyainak jellemző hidrogénion-koncentráció
tartományai és a protonálódási egyensúlyi állandók... 23 5. táblázat [Ru(4py-bpy)(CN)4]2- és [Ru(quapyr)(CN)4]2- komplexek protonálódását jellemző egyensúlyi
állandók és az elnyelési színkép MLCT átmeneteinek változása a protonálódás során. ... 25 6. táblázat A Ru(bpy)32+ és [Ru(bpy)(CN)4]2- komplexek redoxipotenciáljai vs. SCE alap és gerjesztett
állapotban... 25 7. táblázat A [Ru(LL)(CN)4]2- komplexek előállításához felhasznált, korábban nem említett diiminek és a
szövegben használt rövidítéseik. ... 36 8. táblázat A két különböző módszerrel előállított komplexek összefoglalása és az preparatív munka
kitermelési százalékai. ... 39 9. táblázat A [Ru(LL)(CN)4]2- komplexek cianid-vegyértékrezgéseinek energiái cm-1 mértékegységben... 41 10. táblázat A [Ru(LL)(CN)4]2- komplexek elnyelési és kisugárzási maximumai és az MLCT átmenetek
moláris fényelnyelési együtthatói... 43 11. táblázat Az egy módusú Franck-Condon analízisből nyert paraméterek. (A paraméterek
konfidenciaintervalluma 1%-on belül van)... 50 12. táblázat A [Ru(bpy)(CN)4]2- komplexek lumineszcencia-élettartama, kvantumhasznosítási tényezője 298
K-en és az ebből számolható foszforeszcencia sebességi állandó... 56 13. táblázat A hőmérsékletfüggő élettartammérésekből származtatott fotofizikai paraméterek és a Franck-
Condon analízisből kapott E00 paraméter... 57 14. táblázat A különböző deuterált [Ru(LL)(CN)4]2- komplexek fotofizikai folyamatainak sebességei. ... 62 15. táblázat [Ru(LL)(CN)4]2- és a Ru(bpy)32+ komplex fotofizikai adatai normál és deuterált oldószerekben.
... 63 16. táblázat A [Ru(LL)(CN)4]2- (LL=bpy és phen) komplexek fotofizikai paraméterei a τ-T adatsorokat két
potenciálgát figyelembevételével együttesen illesztve... 67 17. táblázat A [Ru(bppz)(CN)4]2- komplex és protonált származékainak fotofizikai és egyensúlyi adatai. .... 68 18. táblázat A [Ru(bppz)(CN)4]2- komplex 13C adatai különböző pH értékeknél... 70 19. táblázat A [Ru(dcb)(CN)4]4- komplex és protonált származékainak fotofizikai és egyensúlyi adatai... 72
KIVONAT
Cím: [Ru(LL)(CN)4]2- típusú komplexek fotofizikai és fotokémiai tulajdonságai A dolgozatban tárgyalt kutatómunka során új [Ru(LL)(CN)4]2- (LL=diimin, 2,2’-bipiridil és 1,10-fenantrolin, valamint különböző szubsztituált és deuterált származékaik) típusú komplexek előállítását és fotofizikai valamint sav-bázis egyensúlyi folyamatainak részletes vizsgálatát tűztük ki célul. A komplexeket NMR, IR, UV látható spektroszkópiai módsze- rekkel jellemeztük. A komplexek fotofizikai folyamatainak sebességét lumineszcencia spektroszkópiás és villanófény-fotolízis rendszer segítségével határoztuk meg. A sav-bázis egyensúlyi rendszerek jellemzését spektrofotometriás titrálással és 13C-NMR spektroszkó- pia vizsgálatokkal végeztük el.
A vizsgálatok eredményei rámutattak arra, hogy a legkisebb energiájú gerjesztett, MLCT állapot energiaszintjét jelentősen befolyásolja a diiminváz jellege és szubsztituensei. Az alacsony hőmérsékleten mért lumineszcenciás színképek Franck-Condon analízise alapján kapcsolatot találtunk a diiminek szerkezete és a gerjesztett állapot alapállapothoz viszonyí- tott torzulásának mértéke között. Hőmérsékletfüggő lumineszcenciaélettartam-mérésekkel megállapítottuk, hogy a gerjesztett állapotú komplexek sugárzásmentes eltűnésének sebes- ségét is alapvetően meghatározza a diiminváz szerkezete. A hőmérséklettől függő energia- vesztési csatornák kinetikai paraméterei arra utalnak, hogy a potenciálgátakon keresztüli energiavesztésért – szobahőmérsékleten - elsősorban a negyedik-MLCT állapot a felelős.
A ligandumok, de még inkább az oldószer deuterálásának hatására a hőmérséklettől füg- getlen és a hőmérséklettől függő sugárzásmentes energiavesztési csatornák hatékonysága is csökken. A nehézvízben és a különböző mértékben deuterált metanolokban oldott komple- xek vizsgálatával nyert adatok azt mutatják, hogy a komplex- és az oldószermolekulák között kialakuló hidrogénkötés frekvenciája döntően befolyásolja a sugárzásmentes folya- matok sebességét.
Meghatároztuk a [Ru(bppz)(CN)4]2- és a [Ru(dcb)(CN)4]4- (bppz=2,3-bis(bipiridil)-pirazin és dcb=4,4’-dikarboxi-2,2’-bipiridil) komplexek protonálódási lépcsőit jellemző savi disz- szociációs állandókat. NMR vizsgálatokkal igazoltuk, hogy az egyes lépcsőkhöz a moleku- lák mely atomjainak protonálódása rendelhető. Kimutattuk, hogy a gerjesztett komplexek diiminligandumának funkciós csoportjai könnyebben protonálhatóak, mint az alapállapotú komplexeké, és a keletkező protonált részecskék lumineszcencia élettartama kisebb, mint a nem protonált vegyületeké.
ABSTRACT
Title: Photophysical and photochemical properties of [Ru(LL)(CN)4]2- complexes Spectroscopic and photophysical characterisations of [Ru(LL)(CN)4]2- complexes (where LL=bidentate diimine like 2,2’-bipyridine, 1,10-phenanthroline and their substituted and deuteriated derivatives) have been reported in this thesis. The rates of photophysical proc- esses have been determined in water, deuterium-oxide and different deuteriated forms of methanol as solvent. It is demonstrated that the energy level of the lowest MLCT state and the rate of non-radiative decay of the complexes can be tuned significantly with the proper choosing of diimine ligand. It has been proved that among the non-radiative and tempera- ture dependent decays the most efficient pathway is going through the fourth-MLCT state.
The deuteriation of solvents results in a stronger reduction of non-radiative rate constants than the deuteriation of the coordinated diimine ligand. It has been revealed that the protic solvent molecules provide a very efficient deactivation route for the excited complexes due to their hydrogen bonded solute-solvent interaction.
The ground and excited state acid-base equilibria of two [Ru(LL)(CN)4]2- complexes pos- sessing electron donating sites on the diimine ligand have been also characterised by spec- trophotometric titration, luminescence and laser flash kinetic spectroscopy.
AUSZUG
Titel: Photochemische und photophysische Eigenschaften der Komplexe vom [Ru(LL)(CN)4]2--Typ
Spektroskopische und photophysische Charakterisierung von den Komplexen [Ru(LL)(CN)4]2-- (wo LL = zweizähniger-Ligand Diimin wie 2,2′-Bipyridin, 1,10- Phenanthrolin und ihre substituierte und deuterierte Derivate) wurde in dieser Dissertation beschrieben. Die Geschwindigkeiten der photophysischen Prozesse wurden im Wasser, Deuterium-Oxid und in verschiedenen deuterierten Methanolen als Lösungsmittel bestimmt. Es wurde demonstriert, daß das Energieniveau des niedrigsten MLCT-Zustandes und die Geschwindigkeit der strahlungslosen Desaktivierung von den Komplexen durch die geeignete Auswahl des Diimin-Liganden bedeutend beeinflußt werden können. Es wurde bewiesen, daß der wirksamste Weg unter den strahlungslosen und temperaturabhängigen Desaktivierungen von den Komplexen durch den vierten-MLCT- Zustand geht. Die Deuterierung des Lösungsmittels resultiert stärkere Abnahmen der Geschwindigkeitskonstanten von den strahlungslosen Desaktivierungsprozessen als die Deuterierung des koordinierten Liganden. Es wurde nachgewiesen, daß die protische Lösungsmittelmoleküle für die angeregte Komplexe sehr wirksame Desaktivierungsweisen durch Lösungsmittel-Komplex-Wasserstoffbrückenbindungen ergeben. Die Säure-Base- Gleichgewichte von den Grund- und Anregungszuständen für zwei [Ru(LL)(CN)4]2-- Komplexe, die Elektronenpaar-Donatoratome an dem Diimin-Ligand haben, wurden auch durch spektrophotometrische Titration, stationäre und zeitaufgelöste Emissionsspektroskopie charakterisiert.
Köszönetnyilvánítás
Ezúton mondok köszönetet témavezetőmnek, Dr. Horváth Attila professzor úrnak, hogy több éves közös munkánk során mindvégig támogatott és értékes szakmai tanácsaival ellátott. Úgy érzem, hogy az együtt eltöltött évek során olyan emberi és kutatói példával szolgált, ami életem végéig elkísér. Köszönettel tartozom, az Általános és Szervetlen Kémia Tanszék kollektívájának, hogy mindvégig jó hangulatú és segítőkész közegben végezhettem a munkámat. Köszönöm Dr. Szalontai Gábor professzor úrnak az NMR mé- rések során nyújtott segítségét.
Végül, de nem utolsósorban köszönöm férjemnek és édesanyámnak, hogy mindvé- gig biztattak, munkámhoz a nyugodt és kiegyensúlyozott hátteret biztosították.
Bevezetés
Már a XIX. század végén felismerték, hogy nagy lehetőségek rejlenek a fényener- gia hasznosításában. Napjainkban a fosszilis energiahordozók használatának káros követ- kezményei és készleteik csökkenése miatt már kényszer is a megújuló és környezetbarát alternatívák kutatása, fejlesztése és alkalmazása a gyakorlatban. A napenergia bármilyen típusú hasznosításának első és kulcsfontosságú feladata a megfelelő fényelnyelés biztosítá- sa. Azonban az elnyelt fényhányad lehető legnagyobb hatásfokú átalakítása szempontjából a molekulán belül bekövetkező fotofizikai lépések és a gerjesztett molekula kémiai reakci- ói is nagy jelentőséggel bírnak. Így nem meglepő, hogy az elmúlt 3-4 évtizedben a fotofizikai és fotokémiai szempontból ígéretes molekulák kutatása jelentős fejlődésen ment keresztül. A fotoaktív rendszerek kutatása azonban természetesen nem a kizárólag nap- energia hasznosítása miatt fontos, számos más gyakorlati alkalmazás, mint pl. a fotokatalízis, orvosi diagnosztika és terápia, lumineszcenciás és elektrolumineszcenciás szenzorok fejlesztése sarkallják az újabb tudományos erőfeszítéseket. A szervetlen foto- kémiai rendszerekben jelentős szerepet töltenek be az átmeneti-fémionok koordinációs vegyületei, ezen belül is a különböző ruténium(II)-komplexek.
A különböző diiminligandumokat tartalmazó ruténium(II)-komplexek fotokémiai karrierje minden kétséget kizáróan a trisz-bipiridil-ruténium(II)-komplex előnyös fotofizikai tulajdonságainak felismerésével kezdődött. A komplexet tartalmazó reakcióele- gyet fénnyel megvilágítva olyan reakciók is lejátszódnak, amelyek az alapállapotú komp- lex számára termodinamikailag nem kedvezményezettek. A [Ru(bpy)3]2+ kedvező tulaj- donságai között, kiemelendő a kémiai stabilitás, a fény látható tartományában mutatott nagy moláris fényelnyelési együttható és a viszonylag hosszú élettartamú gerjesztett álla- pot, ami elektronátadási reakciókban donorként és akceptorként is reagálhat. Ezek a tulaj- donságok gyakorlati szempontból is érdekessé tették a komplexet, így például sikeresen alkalmazták lumineszcenciás oxigén- és pH-érzékelőkben. A különböző diiminligandumokkal előállított trisz-komplexek tulajdonságainak megismerésével párhu- zamosan a 70-es években megindult a vegyesligandumú ruténiumkomplexek kutatása is.
Ezek a komplexek képezik pl. annak a Grätzel-féle fotogalván cellának a „fénnyel hajtott elektronpumpáját” is, amely megközelítőleg 10%-os hatásfokkal működik, és napjainkban már technológiai szinten is az ipari gyárthatósághoz közelít.
A vegyesligandumú ruténiumkomplexek csoportján belül a kezdetektől nagy érdek- lődés mutatkozott a cianokomplexek iránt, mivel más átmeneti-fémionok ilyen vegyületei- ről régóta közismert, hogy elnyelési színképük oldószerfüggő és a cianidligandumok híd szerepet betöltve összekapcsolhatnak több fémcentrumot is. Ebből a szempontból a [monodiimin-tetraciano-rutenát(II)]-komplexek ideális összetételűek, mivel a diiminligandum révén rendelkeznek a trisz-komplexekre jellemző előnyös fotofizikai tu- lajdonságokkal, de ezzel párhuzamosan a cianokomplexekben rejlő lehetőségeket is ma- gukban hordozzák, azaz fotofizikai tulajdonságaik oldószerfüggők és összetettebb szupramolekuláris rendszerekbe is beépíthetők. Napjainkban számos kutatócsoport szentel jelentős figyelmet annak, hogy a fényenergiát hasznosító molekuláris méretű készülékeket illetve meghatározott funkciók ellátására alkalmas szupramolekulákat állítson elő. A trisz- (diimin)-ruténium(II)-komplexekről több évtized alatt tekintélyes mennyiségű adat gyűlt össze arra vonatkozóan, hogy a diiminligandumok megválasztása hogyan befolyásolja a legkisebb energiájú lumineszckáló állapot energiáját és a gerjesztett komplex eltűnéséért felelős fotofizikai folyamatok sebességét. Ezek ismerete elengedhetetlen, amennyiben mű- ködőképes, a célfeladatnak megfelelő rendszereket akarunk előállítani. Annak ellenére, hogy tetraciano-komplexeket - jelen dolgozat megírásának idejére - már tekintélyes számú különböző diiminligandummal állítottak elő, és több szupramolekuláris rendszerben is al- kalmazták azokat, részletes fotofizikai jellemzésüket nem végezték el. Ezért a szerző PhD munkájának elsődleges célja az volt, hogy a gerjesztett komplexek fotofizikai folyamatait részleteiben is megismerje, s a diiminek ezeket befolyásoló hatását megértse. Tekintettel a komplexek oldószerérzékenységére várható, hogy az oldószerdeuterálás is jelentősen mó- dosíthatja a gerjesztett állapot eltűnési sebességét így ennek vizsgálatát is fontosnak ítéltük.
A vegyületcsalád részletes vizsgálatával természetesen távlati célokat is kitűztünk.
A tetraciano-ruténium(II)-komplexek ugyan könnyen beépíthetők többmagvú rendszerekbe cianidoldali koordinációval, de a variabilitásuk tovább növelhető, ha olyan diiminligandumot tartalmaznak, amely szabad donoratomjaival koordinálódhat további központi atomokhoz. Két ilyen típusú komplexet is előállítottunk és jellemeztük azért, hogy a későbbiekben segítségükkel összetettebb, meghatározott funkciójú, pl. egyetlen redoxicentrumú, több kromofórcsoportot magában foglaló antennához kapcsolt rendszere- ket építhessünk fel.
1. Irodalmi összefoglaló
1.1 A [tetraciano-monodiimin-rutenát(II)]-komplexek előállítása
Bignozzi és munkatársai [1] 1986-ban 2,2’-bipiridil ligandumból és kálium- [hexaciano-rutenát(II)]-ből kiindulva fotokémiai úton állították elő az első [tetraciano- monodiimin-rutenát(II)]-komplexet, a K2[Ru(bpy)(CN)4]-öt.
[Ru(CN)6]4-+ bpy [Ru(bpy)(CN)4]2- + 2 CN- (1)
A reakció során 254 nm–es fénnyel fotolizált [Ru(CN)6]4- reagál a szabad bpy ligandummal (1. egyenlet). A szerzők metanol-víz (1:3) oldószerelegyet használtak és ion- csere kromatográfiás úton tisztították a reakcióterméket. Ezt követően többen is hivatkoz- tak erre a módszerre, de a fenti komplex előállítására létezik néhány, más ruténium vegyü- letet felhasználó preparatív eljárás is. Így például [Ru(bpy)Cl4]2- és tetrametil-ammónium- cianid [2] vagy [Ru(bpy)BzCl] (Bz=benzol) és kálium–cianid [3] reakciójával is előállítot- ták a [Ru(bpy)(CN)4]2--ot. Ezek a szintézisek azonban több lépésesek, ugyanis már a ligandumcsere-reakcióhoz használt ruténium-komplexeket is elő kell állítani. Ráadásul a reakcióidő hosszabb és a végtermék izolálása is csak többlépéses tisztítással valósítható meg. A fotokémiai módszert alkalmazták más ligandumokkal képzett komplexek előállítá- sára is (bipirazin, dimetil-bipiridil és dipirido-fenazin; lásd 1. táblázat). Az utóbbi esetében a szerzők nagyon rossz hatásfokról és sok melléktermékről számoltak be, amit a ligandum metanol-víz oldószerelegyben mutatott rossz oldhatóságával magyaráztak.
Jiwan és munkatársai a K2[Ru(bpy)(CN)4] előállítására a fotokémiai reakciónál egyszerűbb eljárást közöltek 1995-ben [4]. A módszer elve az, hogy savas közegben (pH≤4) a hexaciano-rutenát(II) protonálódik és melegítés hatására a protonált komplexből könnyen hidrogén-cianid lép ki szabad koordinációs helyet hagyva maga után. A termék tisztítását nem ioncserélő-oszlopon, hanem méretkizáráson alapuló gélkromatográfiával végezték. Ez azért célszerűbb, mert eluensként víz használható szemben az ioncsere- kromatográfiánál használt viszonylag nagy sókoncentrációjú eluens helyett. Ezt követően ezzel az eljárással vagy ennek kissé módosított változatával több új tetraciano-komplexet is előállítottak.
hν=254 nm
Az eddig vizsgált [Ru(LL)(CN)4]2- komplexekben felhasznált diiminligandumokat (LL) rövidítéseikkel együtt az 1. ábra mutatja, a preparációjuk során alkalmazott kiindulási anyagok és a reakciókörülmények az 1. táblázatban találhatóak.
Meg kell jegyezni, hogy a bppz és bpym ligandumok esetében a [Ru(LL)(CN)4]2- komplex mellett két illetve a HAT ligandummal végzett reakcióban két és három tetraciano-egységet tartalmazó többmagvú komplexek is képződnek. A termékek elválasz- tását ioncserélő oszlopon, NaI különböző koncentrációjú eluensoldataival végezték. [5, 12, 15].
N N
R R R=H bpy
R=CH3 dmb R=COO- dcb
N
N N
N R
R N
N N
N
N
N N
N N NH
N N
5,5'-dmb
bpym
N N
N N bpz
N
N N
N bppz
N N
N
4py-bpy
N
N N
N N
N N
terpy
quapyr
pypz
N
N N
pbe N
dppz
R=H ppb R=Me Meppb R=Cl Clppb (H2C)17
CH3
N N
(CH2)17 C H3
N
N N N
pyr1bpy
pyr2bpy dc18bpy
N N
N
N N
N
HAT
1. ábra. Az eddig előállított [Ru(LL)(CN)4]2- komplexekben felhasznált diiminligandumok és rövidítéseik.
1. táblázat A [Ru(LL)(CN)4]2- komplexek előállításának különböző lehetőségei. A ligandumok szerkezetét az 1. ábra tartalmazza.
LL Kiindulási vegyület Alkalmazott oldó-
szer Egyéb Referencia
bpy 1
bppz 5
dmb 6
bpz 3
dppz
metanol/víz (1/3)
7
ppb 8
Meppb 8
Clppb
K4[Ru(CN)6]
8 dc18bpy ((C2H5)4N)2[Ru(CN)6]
metanol
besugárzás, λ=254 nm
9 bpy RuCl4(bpy) + N(CH3)4CN víz/etanol (4/1) - 2 bpy [BzRu(bpy)Cl]Cl + KCN metanol besugárzás középnyomású
Hg-gőz lámpával 10 bpy HRu(bpy)Cl4
+ KCN víz/etanol 19,5/1 - 11
bpy K4[Ru(CN)6] metanol/víz 1/3 pH=4 4
5,5’-dmb 12
terpy 12
pypz 12
pbe 12
4py-bpy 13
quapyr
K4[Ru(CN)6] metanol/víz 1/1 pH=3-4
13 pyr1bpy TBA4[Ru(CN)6] metanol/DMF 5/1 Savas közeg (H2SO4) 14
pyr2bpy TBA4[Ru(CN)6] DMF Savas közeg (H2SO4) 14
bpym 12
HAT K4[Ru(CN)6] víz pH=1,3 15
1.2 A [Ru(LL)(CN)4]2- komplex fotofizikai tulajdonságai
A tetraciano-komplexek, mint a polipiridil-ruténium(II)-komplexek egyik legegysze- rűbb típusai, fotofizikai tulajdonságai sok tekintetben hasonlóságot mutatnak a Ru(bpy)32+
fotofizikai tulajdonságaihoz.
A K2[Ru(bpy)(CN)4] komplex vizes oldatban felvett színképét a 2. ábra mutatja. Az eddig jellemzett [Ru(LL)(CN)4]2- komplexek fotofizikai adatait az 2. táblázat tartalmazza.
A semleges vizes oldatban legnagyobb hullámhosszaknál található elnyelési sávot minden eddig vizsgált komplexeknél a legkisebb energiájú MLCT átmenethez rendelték. Az átme- net töltésátviteli jellegére vonatkozóan végeztek elektrokémiai és ESR spektroszkópiai
vizsgálatokat is [16, 17]. Megállapították, hogy a redukált [Ru(bpz)(CN)4]2- komplex ESR spektruma azonos hiperfinom szerkezetet mutat, mint a bpz- gyökanion jelezvén, hogy a komplex LUMO-ja a diiminligandum *π pályája. A HOMO pálya eredetére a hasonló szerkezetű [Fe(bpz)(CN)4]2- komplex oxidált formájának ESR spektrumából következtet- tek, ami kisspinszámú vas(III)ionra jellemző paramétereket mutat. A legkisebb energiájú elnyelési sáv töltésátviteli jellegének további bizonyítéka annak jelentős oldószerfüggése, amit a későbbiekben részletesebben tárgyalunk is. A közelmúltban általunk végzett, a [Ru(bpy)(CN)4]2- komplexre vonatkozó, DFT számítások is egyértelműen az eddigi Ru(t2g6)LL(*π0)Æ Ru(t2g5)LL(*π1) hozzárendelést erősítették meg [18]. A bpy komplex színképének nagyobb energiájú tartományaiban 286 nm-nél, hasonlóan a Ru(bpy)32+
komplexhez (λLL=285 nm) [19], a bipiridil ligandum π-π* átmenete azonosítható, mely széles sáv eltakar egy nagyobb energiájú MLCT átmenetet is. Ez utóbbi egyértelműen lát- hatóvá válik a víznél kisebb akceptorképességű oldószerekben (lásd később), mert ez - a legkisebb energiájú MLCT sávhoz hasonlóan - jelentékeny oldószerfüggést mutat. A leg- nagyobb energiánál (≈200 nm) jelentkező, nagy moláris elnyelési együtthatójú sávot a dπ(Ru)Æ*π(CN) átmenetként azonosították [3].
0 5 10 15 20 25
200 400 600 800
Hullámhossz (nm) ε/103 (M-1 cm-1 )
0 0.2 0.4 0.6 0.8 1
Normalizált intenzitás
2. ábra. A [Ru(bpy)(CN)4]2- elnyelési és korrigált kisugárzási színképe szobahőmérsékle- ten vízben.
Az oktaéderes koordinációjú ruténium(II) elektronkonfigurációjából (t2g6eg0) követ- kezik, hogy a komplex alapállapota 1A1g termszimbólummal jellemezhető. Így az elnyelési színképben található nagy moláris fényelnyelési együtthatójú sávok mind szingulett- szingulett, szimmetria-megengedett átmenetek következményei.
A komplexek kisugárzási színképe szobahőmérsékleten egyetlen maximumot tar- talmazó strukturálatlan színkép (2. ábra). A tapasztalt jelentős Stokes eltolódás, valamint a viszonylag hosszú lumineszcencia-élettartam azt mutatja, hogy a Ru(II)-polipiridil komp- lexek legtöbbjéhez hasonlóan, a [Ru(bpy)(CN)4]2- komplex emissziója is a 3MLCT álla- potból történik [1]. Egyértelműen bizonyították, hogy a Ru(LL)32+ komplexek gerjesztését követően a nagyobb energiájú állapotokból, gyors folyamatban mintegy 300 femtoszekundum alatt, a legkisebb energiájú 3MLCT állapot képződik [20], ráadásul a ruténiumatom viszonylag nagy spin-pálya csatolása miatt a spinváltó folyamat kvantum- hasznosítási tényezője egységnyi [19]. A [Ru(bpy)(CN)4]2- esetében a ΦISC egységnyi vol- tát közvetlenül nem igazolták, azonban az eddig vázolt hasonlósága a trisz-komplexekhez valamint az a tény, hogy oldatukat UV fénnyel hosszú ideig bevilágítva sem tapasztalták az elnyelési színkép változását [6], arra enged következtetni, hogy ΦISC=1 erre a komplexre is ésszerű feltételezés.
Hirota és munkatársai [] alacsony hőmérsékleten végzett lumineszcenciaélettartam- mérésekkel bebizonyította, hogy az emisszió - a Ru(bpy)32+-hoz hasonlóan - három egy- máshoz közeli triplett MLCT állapotról következik be. Ezek szobahőmérsékleten lényegé- ben azonos mértékben betöltöttek. Ezen állapotok felett a Ru(bpy)32+ komplex esetében oldószertől függően 3200-4000 cm-1 energiakülönbséggel a torzult szerkezetű, triplett d-d állapot található, mely a szobahőmérséklet környezetében viszonylag hatékony sugárzás- mentes energiavesztési csatornaként működik. Tekintettel arra, hogy a cianidion erős terű ligandum (a bpy-nél is erősebb) feltehető, hogy a [Ru(LL)(CN)4]2- komplexekben a t2g-eg
felhasadás elegendően nagy ahhoz, hogy a 3d-d állapotot jóval a 3MLCT állapot felett tart- sa, ami megakadályozza a gerjesztett állapot gyors sugárzásmentes eltűnését vagy fotodisszociációját a d-d állapoton keresztül. Az irodalomban erre vonatkozó adatok nin- csenek, mivel hőmérsékletfüggő élettartamméréseket szobahőmérséklet környezetében nem végeztek. A tetraciano-komplexek legfontosabb elektron átmeneteit Jablonski- diagramban foglaltuk össze a 3. ábrán. Meg kell azonban említenünk, hogy a trisz-diimin- Ru(II)-komplexek esetében az irodalom beszámol az úgynevezett negyedik-MLCT állapot- ról is, melynek energiaszintje mintegy 600-800 cm-1-gyel
1MLCT
3MLCT
3d-d
1A1g
8 cm-1 53 cm-1
3MLCT E
ISC
hν
Foszf ISC ISC
3. ábra. A [Ru(bpy)(CN)4]2- egyszerűsített Jablonski-diagramja
nagyobb a 3MLCT állapoténál és jelentősebb szingulett karakterrel rendelkezik, mint az alatta található három 3MLCT állapot [21].
A nagyobb t2g-eg felhasadás ellenére szobahőmérsékleten a [Ru(bpy)(CN)4]2- komplex lumineszcencia-élettartama 100 ns és kvatumhasznosítási tényezője Φph=0,0068 vízben [], ami mutatja, hogy valamely sugárzásmentes energiavesztési folyamat hatéko- nyabban működik, mint a lényegesen nagyobb élettartamú 3Ru(bpy)32+ esetében (τ25ºC,víz=660 ns) [22].
Néhány eddig előállított [Ru(LL)(CN)4]2- komplex fotofizikai adatait a 2. táblá- zatban foglaltuk össze. A szingulett és triplett MLCT állapot energiáját alapvetően a diiminligandum minősége határozza meg. A legnagyobb energiánál a [Ru(pypz)(CN)4]2- komplex 1MLCT és 3MLCT állapota található, ami mutatja, hogy a 2. táblázatban bemuta- tott komplexek közül a t2g és *π pályák közti energiakülönbség a pypz ligandumnál a leg- nagyobb. Ugyanezen komplex lumineszcencia-élettartama ugyanakkor szokatlanul kicsi, amit azzal magyaráztak, hogy a nagyobb energiájú 3MLCT olyan közel a kerül a 3dd álla- pothoz, hogy az utóbbin keresztül bekövetkező energiavesztés hatékonnyá válik. Általáno- san azonban elmondható, hogy azok a komplexek, melyek 3MLCT állapotának energiája kisebb, mint a [Ru(bpy)(CN)4]2-é - összhangban az energiarés-törvénnyel - rendre kisebb lumineszcencia-élettartammal bírnak, mint a bpy analóg.
2. táblázat Néhány [Ru(LL)(CN)4]2- komplex fotofizikai adatai vízben, szobahőmérsékleten.
Ligandum λabs,MLCT (nm) λem,MLCT (nm) τ (ns) Ref.
pypz 353 554 17a 12
dmb 392 600 115 6
5,5’-dmb 393 621 370a 12
pbe 404 665 471a 12
terpy 411 647 106a 12
bpym 437 -b 3,4a,c 12
quapyr 440 680 30 13
HAT 443 -b - 15
bppz 447 652 n.a. 5
4py-bpy 448 684 60 13
bpz 465 708 5 3
a nehézvízben, b nem mérhető az emisszió, c tranziens IR mérésből határozták meg, n. a.: nincs adat.
1.3 Szolvatokromizmus
A [tetraciano-monodiimin-rutenát(II)]-komplexek egyik legérdekesebb és a gyakorlati hasznosítás szempontjából is fontos tulajdonsága az, hogy a cianidligandum nemkötő elektronpárja révén elektrondonor molekulákkal, ionokkal másodlagos kölcsönhatás kiala- kítására képesek.
A K2[Ru(bpy)(CN)4]-et először előállító olasz kutatók, majd később többen is leír- ták a komplex fotofizikai tulajdonságainak, elsősorban az MLCT átmenet energiájának jelentős oldószerfüggését [1, 2, 3, 7, 23]. Timson és munkatársai [23] közölték a legrészle- tesebb tanulmányt vegyesligandumú Ru(II)komplexek olyan sorozatáról, melyben a cianidligandumok száma 1-5-ig változik és a maradék koordinációs helyeket piridin és/vagy annak származékai foglalják el. Tizenkét különböző oldószerben mérték a komp- lexek elnyelési és kisugárzási színképét, valamint a [Ru(III)/Ru(II)] redoxipotenciált. A [Ru(bpy)(CN)4]2- komplexre kapott értékeket a 3. táblázatban foglaltuk össze.
Megállapították, hogy adott komplexnél, különböző oldószerekben kapott MLCT sáv maximumok változása nem hozható korrelációba a dielektromos kontinum elméletből származtatható oldószerparaméterrel. Ezzel szemben a Gutmann-féle akceptorszámmal∗
∗ A Gutmann-féle akceptorszám dimenziómentes mennyiség, segítségével az oldószerek Lewis-savasságának relatív mértéket adhatjuk meg. Definiálásakor az Et3PO 31P kémiai eltolódását hexánban nullának tekintették, ez jelöli ki a skála egyik pontját AN=0-val. A skála másik végpontjának az Et3PO:SbCl5 adduktot választot- ták 1,2-diklór-etánban, melyre AN=100.
(AN) lineáris korrelációt mutat az MLCT (Eabs,MLCT) és a π-π* (Eπ-π*) átmenetek energiája, valamint a kisugárzási energia és [Ru(III)/Ru(II)] redoxipotenciál is (3. táblázat). Mind a négy mennyiség növekedik az AN növekedtével. Mivel a dielektromos-kontinum modell nem képes leírni a mért adatok oldószerfüggését, az oldószer-oldottanyag kölcsönhatást nem lehet csak elektrosztatikus okokra visszavezetni. Speciális kölcsönhatással kell szá- molni, ami a cianidion nemkötő elektronpárja és az oldószermolekula megfelelő donorpá- lyája között jön létre. Nagy akceptorszámú oldószerek esetén az elektronküldés a cianidligandumtól az oldószer irányába jelentős, ami megnöveli a komplexen belüli dπ(Ru)→π*(CN) viszontkoordinációt és ezáltal stabilizálja a dπ(RuII) pályát. Ennek kísér- leti bizonyítéka, hogy a ν(CN) frekvenciák csökkennek (ezt részletesen a cis- [Ru(bpy)2(py)(CN)]+ komplexre vizsgálták), míg a [Ru(III)/Ru(II)] redoxipotenciál mind- egyik vizsgált cianokomplexnél nő az oldószer akceptorképességének növekedtével.
A szerzőket meglepte ugyanakkor, hogy az elnyelési színkép π-π* átmenetének energiája is AN függést mutat. Azt várták, a szabad bpy és a Ru(bpy)32+ oldószerhatás vizsgálatai alapján, hogy a központi fémiont nem érintő π-π* átmenet energiájának változá- sa a dielektromos-kontinum modellt fogja követni. A cianokomplexek esetében tapasztal- takat azzal magyarázzák, hogy fellép a központi fémion dπ(Ru) pályájának és a ligandum betöltött π pályájának keveredése és így a π-π* átmenet némi MLCT jelleget mutat. (Ezt az eddig nem közölt DFT szimulációk eredményei is alátámasztják [24].)
3. táblázat A [Ru(bpy)(CN) ] elnyelési valamint kisugárzási színképeinek maximumai és a [Ru(III)/Ru(II)]
redoxipotenciál értékei különböző oldószerekben. (Fc=ferrocén4
2-
)
Oldószer AN Eπ-π* × 10-3 (cm-1) EMLCT × 10-3 (cm-1) Eem × 10-3 (cm-1) E1/2(RuIII/II) V vs Fc+/0
THF 8,0 32,67 17,89 - -
aceton 12,5 - 18,55 - -0,26
piridin 14,2 - 19,05 12,53 -
DMF 16,0 33,56 17,89 12,22 -0,28 DMSO 19,3 33,44 18,18 12,41 -0,18 CH3CN 19,3 33,90 18,69 12,41 -0,14 CH2Cl2 20,4 33,67 18,93 12,89 -
CH3NO2 20,5 - 20,79 - -
n-propil-OH 33,5 34,01 20,28 13,81 0,01 EtOH 37,1 34,13 21,23 14,04 0,11 MeOH 41,3 34,36 22,22 14,62 0,27
H2O 54,8 35,09 24,75 15,63 0,77
A kisugárzási maximumokat tekintve megállapították, hogy az emissziós energia (Eem) oldószer érzékenysége kb. 70 %-a az Eabs,MLCT esetében kimutatott értéknek. Ez azzal magyarázható, hogy a gerjesztés következtében a központi fémion környezetéből, a dπ(RuII) pályáról a diiminligandum π*(LL) pályájára kerül egy elektron, ami lecsökkenti a fémion π-donor képességét. Ez utóbbi hatására lecsökken a cianidligandumok oldószermolekulák felé irányuló donicitása, következésképp az oldószer hatás mértéke jelentékenyen csökken. Az Eem eltérő oldószerfüggése azt is jelenti, hogy az alap és a ger- jesztett állapotban az oldószer újrarendeződési energia különböző, tehát a két állapot elekt- ronszerkezete jelentősen eltér egymástól. Sőt nem is lehet az oldószer és a molekula újra- rendeződési energiáit élesen elkülöníteni, mivel a speciális kölcsönhatás miatt a belső szfé- ra vibrációs potenciál függvényei is perturbálódnak. Az alap és gerjesztett állapot szerkeze- tének jelentős különbségét mutatták ki Braslavsky és munkatársai is a [Ru(bpy)(CN)4]2- komplex lézerindukált optoakusztikus spektroszkópiai vizsgálatával [4]. Megállapították, hogy a triplett gerjesztett állapot kialakulása a molekulatérfogat növekedésével jár együtt (∆VR=15 ml/mol), mivel az elsődleges hidrátburokban található vízmolekulák és a komplex között gyengül a kölcsönhatás. Tehát a komplex-oldószer rendszer kvázi kitágul a gerjesz- tés következtében. Amennyiben a cianidligandumokat egyenként metil-cianidra cserélték a gerjesztési térfogatváltozás mértéke csökkent (∆VR1=10.3 ml/mol, ∆VR2=-0.9 ml/mol,
∆VR3=-1.0 ml/mol). Ezzel gyakorlatilag azonos eredményre vezettek a gázfázisú komplex részleges hidratált klasztermodelljének, [Ru(bpy)(CN)4]2-·(H2O)n (n=4, 8) DFT számításai [18]. Az alapállapotban viszonylag erős CN····H-OH hidrogénkötés erőssége a triplett ger- jesztett állapotban jelentősen csökken (a kötési energiák különbsége 700 cm-1 n=4 esetén) és az N····H kötéshossz mintegy 0,05 Å-mel nagyobb.
A lumineszcencia-élettartam és kvantumhasznosítási tényező is jelentékeny oldó- szerfüggést mutat. Kisebb akceptorszámú oldószerekben, a kisugárzási színkép maximu- mának vörösbe tolódásával párhuzamosan csökken az élettartam és a lumineszcenciaintenzitás is. A [Ru(bpy)(CN)4]2- lumineszcencia-élettartama pl. szobahő- mérsékleten, vízben 120, etanolban 25, míg DMF-ban csak ~4 ns [1]. A jelenségnek két oka is lehet, egyrészt az alap és gerjesztett állapot közötti kisebb energiarés a sugárzásmen- tes folyamatok felgyorsulását eredményezi, másrészt a kisebb akceptorszámú oldószerek- ben lecsökken a t2g-eg felhasadás, ami a 3dd állapoton keresztüli gyors energiavesztésnek kedvezhet.
1.4 A [Ru(bpy)(CN)4]2- sav-bázis egyensúlya alap és gerjesztett állapotban
A komplexben található négy cianidion négy proton felvételére teszi képessé a mo- lekulát. Ezek közül a második lépcsőben semleges H2[Ru(bpy)(CN)4] keletkezik, mely vízben kevéssé oldható. A komplex protonálódási egyensúlyait vizsgálva pH<3-nál indul meg az elnyelési színkép látható tartományában található, legkisebb energiájú MLCT sáv kékbe tolódása, ami 9 M-os kénsavban már olyan mértékű, hogy az MLCT sáv takarásba kerül a ligandum π-π* átmenete által. A különböző protonált formákhoz tartozó pH tarto- mányokat a 4. táblázatban tüntettük fel [25].
4. táblázat A K2[Ru(bpy)(CN)4] protonálódási egyensúlyainak jellemző hidrogénion-koncentráció tartomá- nyai és a protonálódási egyensúlyi állandók.
[H+] M Komplexek pKs
10-3-0,05 [Ru(bpy)(CN)4]2- ,[Ru(bpy)(CN)3(CNH)]- 1.78
0,4-2 [Ru(bpy)(CN)3(CNH)]-, [Ru(bpy)(CN)2(CNH)2] -1.1 2-5 [Ru(bpy)(CN)2(CNH)2], [Ru(bpy)(CN)(CNH)3]+
>5 [Ru(bpy)(CN)(CNH)3]+, [Ru(bpy)(CNH)4]2+
Az elnyelési színképek alapján az első két protonálódási lépcsőre Ks1=60 M-1 és Ks2=8×10-2 M-1 értéket határoztak meg. Minden egyes proton felvételét az elnyelési szín- kép MLCT sáv maximumának körülbelül 2500 cm-1-es kék eltolódása követi, amiből a szingulett gerjesztett állapotra nézve 5 egységnyi pK eltolódás becsülhető az alapállapot pK-jához képest [26]. A kék eltolódás a hidrogénion elektronszívó hatásával magyarázha- tó. Ahogyan már az oldószer hatás bemutatásánál is leírtuk, a cianidoldalon kifejtett elekt- ronszívó hatás lecsökkenti a központi fémion elektronsűrűségét, ami stabilizálja a dπ(Ru) pályát.
A kisugárzási színképek változása csak nagyobb hidrogénion-koncentrációnál indul meg [H+]>1M, ami mutatja, hogy a gerjesztett állapot savasabb, mint az alapállapot és a protontranszfer sokkal gyorsabb folyamat, mint a gerjesztett állapot energiavesztése. 1M- nál nagyobb hidrogénion-koncentrációknál megindul a színkép kék eltolódása, amelyet jelentős intenzitásnövekedés is kísér. [H+]>14M koncentrációnál váll jelenik meg a színkép nagyobb energiájú tartományában, majd tovább növelve a koncentrációt 18 M-os oldatban egy teljesen strukturált emisszió figyelhető meg. A koncentrált kénsavban, 77K-en mért kisugárzási színképek nagy hasonlóságot mutatnak a Rh(bpy)33+ alacsony hőmérsékletű színképéhez. Az utóbbi komplexről ismert, hogy ligandumon lokalizált ππ*
foszforeszcenciát mutat. Tehát a protonálás hatására [Ru(bpy)(CN)4]2--ben megfordul a sorrend az eredetileg HOMO t2g és a ligandum betöltött π pályája között, aminek eredmé- nyeképpen a π-π* átmenet lesz a legkisebb energiájú..
A [Ru(bpy)(CNH)4]2+ komplexszel azonos tulajdonságokat mutat a [Ru(bpy)(CN)4]2- metilálásával előállított tetraizocianid komplex is. Itt a cianidligandum nitrogénoldalán a metilcsoport révén csökken az elektronsűrűség. Ennek eredményeképpen szintén lejátszódik a dπ(Ru) és π pályák energiaszintjének felcserélődése. Mindez a fent említett, jellegzetes strukturált alakú ππ* foszforeszcenciához vezet.
Végeztek pH függő kísérleteket olyan tetraciano-komplexekkel is, melyek a diiminoldalon is rendelkeznek protonálható donoratomokkal []. E vizsgálat során a kiindu- ló pontot a két ligandum, 4py-bpy és quapyr trisz-Ru(II) komplexekből ismert röntgenada- tai adták. Ezek szerint ugyanis a 4py-bpy ligandum mindhárom piridinegysége megközelí- tőleg azonos síkban helyezkedik el, míg a quapyr esetében a négy piridinegységből kettő- kettő páronként egymásra merőlegesen áll. Ez alapján az várható, hogy a 4py-bpy ligandum protonálható része viszonylag erős, míg a quapyr-é gyengébb elektronikus csato- lásban van a komplex többi részével. A pH csökkenésének hatására mindkét tetraciano- komplex először a diiminligandum perifériás nitrogénjén protonálódik. A 4py-bpy eseté- ben ez mintegy 1000 cm-1 vörös eltolódást okoz az MLCT sávmaximumban, míg a quapyr ligandummal képzett komplexeknél csak a diiminligandum LL sáv maximuma mutat vál- tozást. A cianidligandumok protonálódását a színkép MLCT sávmaximumának kék eltoló- dása jelzi, ami - mivel független a diiminoldaltól - mindkét komplexnél tapasztalható és értéke mintegy 2200 cm-1. Az egyes lépcsőkhöz rendelhető egyensúlyi állandókat az 5.
táblázatban foglaltuk össze. A hidrogénion koncentrációjának növekedtével a 4py-bpy ligandummal képzett komplexnél a lumineszcencia teljes, míg a quapyr komplex részleges kioltását tapasztalták. Ezt gerjesztett állapotbeli elektronátadásnak tulajdonították, a koor- dinált bipiridinrészről a protonált piridin- vagy bipiridinrészre kerül a gerjesztett elektron.
A lumineszcencia részleges kioltása valamint az a tény, hogy a diimin protonálódása során az elnyelési színkép MLCT sávja nem tolódik el a vörösbe, a kezdeti feltételezést támaszt- ják alá, miszerint gyengébb a csatolás a quapyr-rel képzett komplex központi része és a perifériás piridinegység között.
![1. ábra. Az eddig előállított [Ru(LL)(CN) 4 ] 2- komplexekben felhasznált diiminligandumok és rövidítéseik](https://thumb-eu.123doks.com/thumbv2/9dokorg/873389.46982/15.892.128.806.384.1070/ábra-előállított-ru-ll-komplexekben-felhasznált-diiminligandumok-rövidítéseik.webp)
![2. ábra. A [Ru(bpy)(CN) 4 ] 2- elnyelési és korrigált kisugárzási színképe szobahőmérsékle- szobahőmérsékle-ten vízben](https://thumb-eu.123doks.com/thumbv2/9dokorg/873389.46982/17.892.216.689.659.1030/ábra-elnyelési-korrigált-kisugárzási-színképe-szobahőmérsékle-szobahőmérsékle-vízben.webp)
![2. táblázat Néhány [Ru(LL)(CN) 4 ] 2- komplex fotofizikai adatai vízben, szobahőmérsékleten](https://thumb-eu.123doks.com/thumbv2/9dokorg/873389.46982/20.892.141.775.134.449/táblázat-ru-ll-komplex-fotofizikai-adatai-vízben-szobahőmérsékleten.webp)
![4. táblázat A K 2 [Ru(bpy)(CN) 4 ] protonálódási egyensúlyainak jellemző hidrogénion-koncentráció tartomá- tartomá-nyai és a protonálódási egyensúlyi állandók](https://thumb-eu.123doks.com/thumbv2/9dokorg/873389.46982/23.892.124.817.446.598/táblázat-protonálódási-egyensúlyainak-hidrogénion-koncentráció-protonálódási-egyensúlyi-állandók.webp)
![5. táblázat [Ru(4py-bpy)(CN) 4 ] 2- és [Ru(quapyr)(CN) 4 ] 2- komplexek protonálódását jellemző egyensúlyi állandók és az elnyelési színkép MLCT átmeneteinek változása a protonálódás során](https://thumb-eu.123doks.com/thumbv2/9dokorg/873389.46982/25.892.127.779.151.246/táblázat-protonálódását-egyensúlyi-állandók-elnyelési-átmeneteinek-változása-protonálódás.webp)
![6. ábra. Szubsztituált ciklámszármazékok, melyeket hidrogénkötés révén kapcsolták a [Ru(bpy)(CN) 4 ] 2- komplexhez](https://thumb-eu.123doks.com/thumbv2/9dokorg/873389.46982/29.892.246.673.106.648/ábra-szubsztituált-ciklámszármazékok-melyeket-hidrogénkötés-révén-kapcsolták-komplexhez.webp)
![9. ábra. A K 2 [Ru(bpy)(CN) 4 ] és a K 2 [Ru([D8]-bpy)(CN) 4 ] IR színképe KBr pasztillában a cianid-vegyértékrezgések tartományában](https://thumb-eu.123doks.com/thumbv2/9dokorg/873389.46982/42.892.195.668.139.440/ábra-ru-színképe-kbr-pasztillában-cianid-vegyértékrezgések-tartományában.webp)
![10. ábra. A [Ru(LL)(CN) 4 ] 2- elnyelési színképei vízben szobahőmérsékleten, LL=bpy, dmb, dpb, dcb és bppz](https://thumb-eu.123doks.com/thumbv2/9dokorg/873389.46982/43.892.187.692.318.735/ábra-ru-ll-elnyelési-színképei-vízben-szobahőmérsékleten-bppz.webp)
![11. ábra. A [Ru(LL)(CN) 4 ] 2- elnyelési színképei vízben szobahőmérsékleten, LL=phen származékok](https://thumb-eu.123doks.com/thumbv2/9dokorg/873389.46982/45.892.202.728.635.1071/ábra-ru-elnyelési-színképei-vízben-szobahőmérsékleten-phen-származékok.webp)