Faigl, Ferenc Kollár, László Kotschy, András
Szepes, László
Kollár, László Kotschy, András Szepes, László Publication date 2002
Szerzői jog © 1996 dr. Faigl F., dr. Kollár L., dr. Kotschy A., dr. Szepes L., Nemzeti Tankönyvkiadó Rt. - Budapest
Készült az Oktatási Minisztérium Felsőoktatási Pályázatok Irodája által bonyolított felsőoktatási tankönyvtámogatási program keretében Bírálók:
dr. Markó László
akadémikus, a kémiai tudomány doktora Alkotó szerkesztő:
Dr. Kollár László
a kémiai tudomány doktora dr. Timári Géza
a kémiai tudomány kandidátusa Nemzeti Tankönyvkiadó Zrt. www.ntk.hu
A mű más kiadványban való részleges vagy teljes felhasználása, utánközlése illetve sokszorosítása a kiadó engedélye nélkül tilos!
BEVEZETÉS ... xxix
A. Rövidítések jegyzéke ... 1
Vegyületek rövidítése ... 1
Egyéb rövidítések ... 4
1. I. A SZERVES FÉMVEGYÜLETEK ÁLTALÁNOS JELLEMZÉSE ... 7
I.1. Alapfogalmak ... 7
I.1.1. A szerves fémvegyületek meghatározása, története és helye a kémiában ... 7
Irodalmi hivatkozások ... 11
I.2. A szerves fémvegyületek kutatásának főbb irányai ... 12
I.2.1. Fémorganikus vegyületek mint modellek és prekurzorok ... 12
I.2.2. Reaktív molekulák stabilizálása ligandumként ... 13
I.2.3. Metallaciklusok ... 13
I.2.4. Fémorganikus klaszterek ... 14
I.2.5. Fémorganikus katalízis ... 15
Irodalmi hivatkozások ... 16
I.3. A fém-szén kötés ... 18
Irodalmi hivatkozások ... 21
I.4. A ligandumok ... 22
I.4.1. A ligandumokról általában ... 22
I.4.2. Szerves ligandumok ... 23
1.4.3. Egyéb ligandumok ... 40
Irodalmi hivatkozások ... 43
I.5. A 18-elektronos szabály ... 44
I.6. Az átmenetifém-klaszterek és a többszörös fém-fém kötés ... 48
I.6.1. A klaszterek definíciója és általános jellemzése ... 48
I.6.2. Többszörös fém-fém kötésű vegyületek ... 51
Irodalmi hivatkozások ... 52
I.7. A szerves fémvegyületek csoportosítása ... 53
Irodalmi hivatkozások ... 55
I.8. A szerves fémvegyületek termokémiája ... 55
I.8.1. Kísérleti módszerek ... 56
I.8.2. Kötési entalpiák és meghatározásuk ... 59
Irodalmi hivatkozások ... 63
I.9. A fémorganikus vegyületek stabilitása ... 65
Irodalmi hivatkozások ... 68
I.10. A fémorganikus vegyületek spektroszkópiája és szerkezetkutatása (Tarczay György és Szepes László) ... 68
I.10.1. Mágneses magrezonancia-spektroszkópia ... 70
I.10.2. Elektronspinrezonancia-spektroszkópia ... 81
I.10.3. Forgási spektroszkópia ... 82
I.10.4. Rezgési spektroszkópia ... 83
I.10.5. Elektrongerjesztési spektroszkópia ... 91
I.10.6. Tömegspektrometria ... 93
I.10.7. UV fotoelektronspektroszkópia ... 96
I.10.8. Mössbauer-spektroszkópia ... 99
I.10.9. Diffrakciós módszerek ... 102
I.10.10. Kvantumkémiai számítások ... 105
Irodalmi hivatkozások ... 105
2. II. A FŐCSOPORTBELI FÉMEK SZERVES SZÁRMAZÉKAI ... 112
II.1. Általános jellemzés ... 112
Irodalmi hivatkozások ... 116
II. 2. Általános előállítási módszerek ... 116
ΙΙ.3. Poláris fémorganikus vegyületek ... 120
II.3.1. Az alkálifémek szerves vegyületei ... 122
ΙΙ.3.2. Az alkáliföldfémek szerves vegyületei ... 146
II.3.3. A 12. csoport elemeinek szerves vegyületei ... 153
II.3.4. A 11. csoport féméinek szerves vegyületei ... 160
II.3.5. A poláris fémorganikus vegyületek gyakorlati alkalmazása ... 165
Irodalmi hivatkozások ... 170
II.4. Kovalens fémorganikus vegyületek ... 181
II.4.1. A 13. csoport elemeinek szerves vegyületei ... 181
II.4.2. A 14. csoport elemeinek fémorganikus vegyületei ... 192
II.4.3. Az arzén, antimon és bizmut szerves vegyületei ... 203
II.4.4. A szelén és tellúr vegyületei ... 207
Irodalmi hivatkozások ... 210
3. III. ÁTMENETIFÉM-ORGANIKUS VEGYÜLETEK ... 213
III. 1. σ-Donor ligandumok ... 214
III. 1.1. Fém-C(sp3) kötést tartalmazó vegyületek ... 215
III.1.2. Fém-C(sp2) kötést tartalmazó vegyületek ... 224
III.1.3. Fém-C(sp) kötést tartalmazó vegyületek ... 238
Irodalmi hivatkozások ... 245
III.2. σ-Donor/π-akceptor ligandumok ... 251
III.2.1.Átmenetifém-karbonil-komplexek ... 251
III.2.2. Átmenetifém-kalkogén-karbonil (tiokarbonil, szelenokarbonil, tellurokarbonil) komplexek ... 263
III.2.3. Átmenetifém-izocianid-komplexek ... 266
Irodalmi hivatkozások ... 269
III.3. σ/π-Donor/π-akceptor ligandumok ... 271
III.3.1. Alkénkomplexek ... 272
III.3.2. Konjugált diének komplexei ... 277
III.3.3. Heteroalkénkomplexek ... 280
III.3.4.Alkinkomplexek ... 282
III.3.5. Heteroalkinkomplexek ... 284
III.3.6. CnHn+2 típusú ligandumok komplexei ... 285
III.3.7. CnHn típusú ligandumok komplexei ... 293
III.3.8. Heterociklusos vegyületek átmenetifém-komplexei ... 314
Irodalmi hivatkozások ... 317
III.4. Klaszterek ... 322
Irodalmi hivatkozások ... 325
4. IV. ÁTMENTIFÉM-ORGANIKUS VEGYÜLETEK SZINTETIKUS ALKALMAZÁSAI ... 326
IV.1. Átmenetifém-hidridek ... 328
IV.1.1. Átmenetifém-monohidridek ... 328
IV.1.2. Átmenetifém-dihidridek ... 329
IV.1.3. Enantioszelektív redukciós eljárások ... 330
ΙV.1.4. Irídiumkomplexekkel katalizált redukciós reakciók ... 335
IV.1.5. Katalitikus hidroborálás és hidroszililezés ... 336
IV.1.6. Egyéb átmenetifém-komplexek által katalizált redukciós reakciók ... 338
Irodalmi hivatkozások ... 339
IV.2. σ-kötésű fémorganikus vegyületek ... 341
IV.2.1. σ-kötésű átmenetifém-organikus vegyületek előállítása ... 342
IV.2.2. σ-Kötésű átmenetifém-organikus vegyületek átalakítása ... 350
Irodalmi hivatkozások ... 365
IV.3. Karbonilkomplexek ... 369
IV.3.1. Karbonilezési reakciók ... 369
IV.3.2. Dekarbonilezési reakciók ... 372
IV.3.3. Kapcsolási reakciók ... 373
IV.3.4. Vas-acil-komplexek szintetikus alkalmazása ... 374
IV.3.5. Hidroformilezés és kapcsolódó reakciók ... 375
IV.3.6. Monsanto-féle ecetsavszintézis ... 379
IV.3.7. Pauson–Khand-reakció ... 380
Irodalmi hivatkozások ... 381
IV.4 Karbénkomplexek ... 384
IV.4.1. Heteroatommal stabilizált (Fischer) karbének ... 384
IV.4.2. Heteroatomot nem tartalmazó elektrofil karbének ... 391
IV.4.3. Átmenetifémekkel katalizált ciklopropanálás diazovegyületekkel ... 392
IV.4.4. Alkénmetatézis ... 394
IV.4.5. Nukleofil karbének ... 396
Irodalmi hivatkozások ... 398
IV.5. Alkén-, dién- és dienilkomplexek ... 400
IV.5.1. Nukleofil támadás palládiumkomplexekre ... 401
IV.5.2. Nukleofil támadás alkén-vas-komplexekre ... 406
IV.5.3. Nukleofil támadás vas-dién- és -dienil-komplexekre ... 407
IV.5.4. Átmenetifém-katalizált cikloaddíciós reakciók ... 409
Irodalmi hivatkozások ... 411
IV.6. Alkinkomplexek ... 413
IV.6.1. Nukleofil támadás palládium-alkin-komplexekre ... 413
IV.6.2. Alkinek védelme átmenetifém-komplexként ... 415
IV.6.3. Alkinek átmenetifémek által katalizált oligomerizációja ... 416
IV.6.4. Alkinek nikkel által katalizált karboxilatív átlakításai ... 419
IV.6.5. Cirkónium-dehidrobenzol-komplexek szintetikus alkalmazása ... 420
Irodalmi hivatkozások ... 421
IV.7. η3-allilkomplexek ... 423
IV.7.1. Konjugált diének átmenetifémek által katalizált dimerizációja ... 424
IV.7.2. η3-Allil-palládium-komplexek szintetikus átalakításai ... 426
IV.7.3. Α palládium trimetilénmetán komplexének átalakításai ... 434
IV.7.4. η3-allil-nikkel-komplexek átalakításai ... 435
Irodalmi hivatkozások ... 436
IV.8. Arénkomplexek ... 439
IV.8.1. Nukleofil szubsztitúció átmenetifém-arén-komplexeken ... 439
IV.8.2. Nukleofil addíció átmenetifém-arén-komplexeken ... 441
IV.8.3. Litiálási reakciók arén-króm-komplexeken ... 444
IV.8.4. Diasztereoszelektív átalakítások átmenetifém-arén-komplexeken ... 446
IV.8.5. η2-Arén-ozmium-komplexek alkalmazásán alapuló átalakítások ... 448
Irodalmi hivatkozások ... 450
B. Ajánlott irodalom ... 453
C. Név- és tárgymutató ... 457
(I.1). ... 8
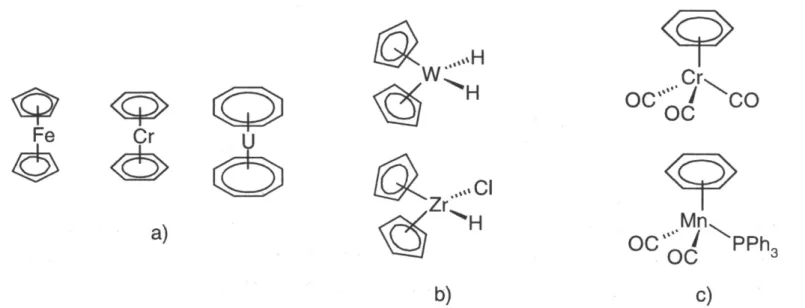
I.1. A ferrocén szerkezete ... 10
I.2. A ciklobutadién-vas-trikarbonil-komplex ... 13
I.3. Tipikus metallaciklusos szerkezetek ... 14
I.4. Az Os-atomok szoros illeszkedésű köbös elrendeződése a (Os20(CO)40)2–-klaszterben ... 14
-. ... 16
I.5. A trimetil-alumínium-dimer szerkezete (2) ... 19
I.6. A trimetil-alumínium-dimer Al-Al és többcentrumú, elektronhiányos Al-C kötése ... 19
I.7. Donor-akceptor kötés kialakulása átmenetifém-karbonilokban ... 21
I.8. Donor-akceptor kötés kialakulása átmenetifém-alkén-komplexekben ... 21
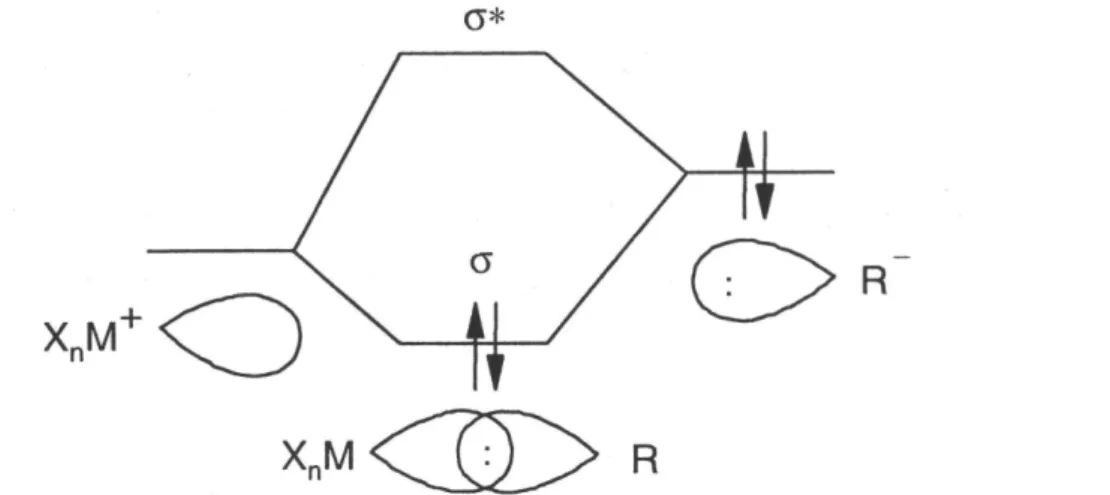
I.9. M-R σ-, σ*-molekulapályák kialakulása az XnM+ és R- fragmenseken lokalizált pályák kölcsönhatásával ... 23
I.10. A CO-ligandum leggyakrabban előforduló kötési módjai ... 25
I.11. Aszimmetrikus CO-híd ... 26
I.12. Lineáris és hajlott alkil-izocianid-ligandum ... 27
I.13. Lineáris és hajlott térszerkezetű NO-ligandum ... 27
I.14. A dinitrogén, N2 mint ligandum lehetséges helyzetei ... 28
I.15. Az M(dπ) és C(pz) viszonylagos energiájának szerepe a karbénszénatom elektrofil/nukleofil jellegének alakításában (5) ... 29
I.16. M≡C hármas kötés kialakulása az átmenetifém-karbin-komplexekben (7) ... 30
I.17. A butadién-vas-trikarbonil szerkezete ... 33
I.18. Fém-ligandum kölcsönhatás a butadiénkomplexekben ... 34
I.19. Fém-dién rezonanciaszerkezetek ... 34
I.20. A koordinált alkinek lehetséges kapcsolódásai ... 35
I.21. σ-, π- és hídhelyzetű allilcsoportot tartalmazó komplexek ... 35
I.22. A fém-allil kötés ... 36
I.23. „Enyl”-komplexek ... 36
I.24. A gyűrűs π-donorokkal alkotott komplexek szerkezeti alaptípusai: „szendvics” (a); „hajlott szendvics” (b) és „félszendvics” (c) vegyületek ... 37
I.25. A ciklopentadienilcsoport elektronszerkezete (a) és a fém-Cp kölcsönhatás egyik kombinációja (b) az (5) irodalmi hivatkozás 123. oldaláról átvett ábra ... 38
I.26. A ferrocén kvalitatív molekulapálya-diagramja (a); a Cp(ψ1)-pályák szimmetrikus és antiszimmetrikus kombinációjának kölcsönhatása a fématomon lokalizált dz2- és pz-pályákkal (b). (A jobb áttekinthetőség kedvéért a Cp(ψ1) hullámfüggvénynek csak az egyik felét tüntettük fel az ábrán.) ... 39
I.27. Agosztikus kölcsönhatás a TiEtCl3X2-komplexben ... 41
I.28. A foszfánligandum π-akceptor pályái ... 41
I.29. A ligandumok térigényét jellemző θ kúpszög ... 42
I.30. A (η5-Cp)Fe(CO)2Cl vegyértékelektron-számának meghatározása: a) „donorpár” módszer; b) „semleges ligandum” módszer ... 45
I.31. Divas-enneakarbonil, Fe2(CO)9 ... 46
I.32. A központi Cr körül oktaéderesen elhelyezkedő CO-ligandumok σ-donorpályáinak és az atomi 4s- és 4pz-pályák kölcsönhatása ... 47
I.33. A Cr(CO)6 molekulapályái ... 48
I.34. Az Ir4(CO)12 szerkezete ... 49
I.35. Az(Os6(CO)18)2– térszerkezete ... 50
I.36. Lehetséges kölcsönhatások két fématom d-pályái között (a z tengely az atommagokat összekötő egyenes irányában helyezkedik el) (6) ... 51
I.37. A dxy-pályák kölcsönhatása a klóratomok fedőállásánál az (Cl4Re≡–ReCl4)2–-ionban ... 51
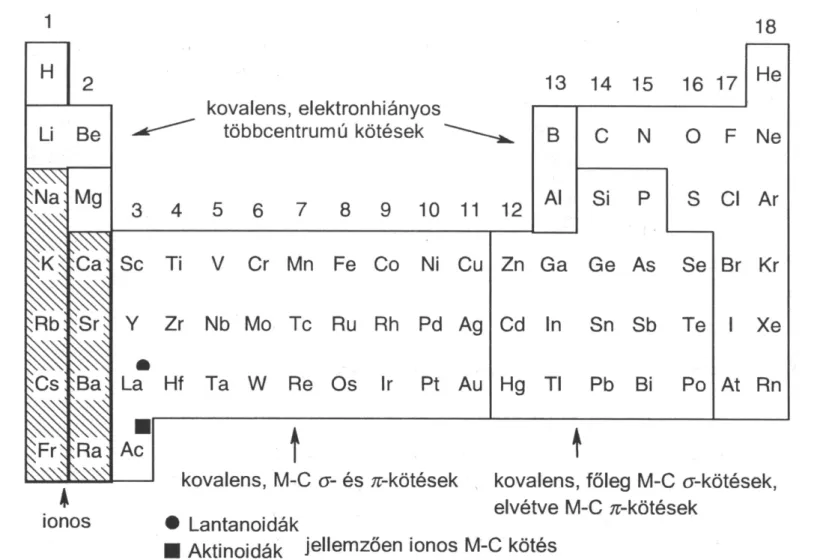
I.38. A periódusos rendszer elemeinek csoportosítása a fém/elem-szén kötéstípus alapján ... 54
(I.15). ... 59
(I.16). ... 59
(I.17). ... 60
(I.18). ... 60
-. ... 61
-. ... 61
(I.20). ... 62
(I.29). ... 67
I.39. Néhány jellemző NMR csatolási állandó ... 73
I.40. Fém- (M) és elem(E)-organikus vegyületek jellemző 1H NMR-eltolódásai ... 73
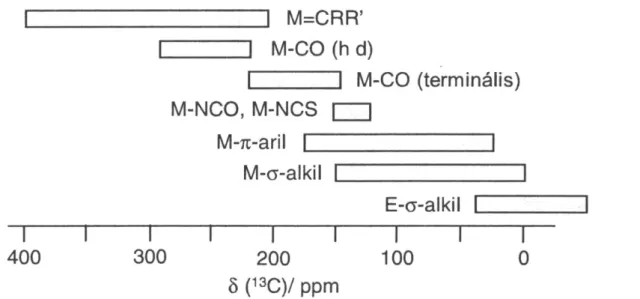
I.41. Fémorganikus vegyületek jellemző 13C NMR-eltolódásai ... 74
I.42. Összefüggés a fém NMR kémiai eltolódásai és a reakciósebességi állandók között (13) (lásd szöveg) ... 75
I.43. A Sn(CH3)4 1H NMR-spektruma (2) ... 76
I.44. Az Al(BH4)31H NMR- (a); 1H{27Α1} NMR- (b); és 1H{11Β} NMR- (c) spektruma (1) ... 77
I.45. A B10H14 szerkezete (a); homonukleáris 11B COSY (b); és heteronukleáris 11B/1H COSY-spektruma (c) (1) ... 79
I.46. (a) Berry-átrendeződés a (HRhL∩L(CO)2)-komplexben (ahol L∩L kétfogú foszforligandum); (b) a vegyület hőmérsékletfüggő kísérleti 31P{1H} NMR-spektruma; (c) az elméleti spektrum (18) ... 80
I.47. A Li4Me3CH2-gyök szerkezete (a); és ESR-spektruma (b) (4) ... 82
I.48. Karakterisztikus fém-ligandum és ligandum rezgési frekvenciák fémorganikus vegyületekben (ν: nyújtási rezgés, β: hajlítási rezgés) ... 84
I.49. Összefüggés az MLn(CO)m típusú karbonilkomplexek L ligandumának elektronküldő (+I) hatása és a szén-oxigén nyújtási frekvencia (ν(CO)) között ... 85
I.50. Összefüggés a karbonilkomplexek oxidációs állapota, a viszontkoordináció és a szén-oxigén nyújtási frekvencia (ν(CO)) között ... 85
I.51. A C-O nyújtási frekvencia (ν(CO)) függése a CO-ligandum kötéstípusától ... 86
I.52. A ferrocén hagyományos pasztillatechnikával készült (a); és mátrixizolációs (b) infravörös spektruma (3) ... 88
I.53. A Cr(CO)6 mátrixizolációs infravörös spektruma (a); és a minta UV-fotolízisével képződő Cr(CO)5 mátrixizolációs infravörös spektruma (b) (27,28) ... 89
I.54. A fotokémiailag indukált CO-kihasadás mechanizmusa a CH3C(O)Co(CO)3(PPh3) vegyületben, (a) A kiindulási vegyület (K) IR-
spektrumának részlete; (b) a spektrum változása a fotolízis hatására (az egymásra rajzolt spektrumok a fotolízis után 5 μs-onként készültek);
(c) A kiindulási vegyület (K), az átmeneti komplex (ÁK) és a termék (T) egy-egy jellemző sávjának intenzitásváltozása az idő függvényében
(29) ... 90
I.55. A piridin és a η1-piridin-W(CO)5 elektronszerkezete valamint az n → π* és π → π* átmenetek (32) ... 93
I.56. Az elemi germánium és a tetrafenil-germánium molekulaionjának izotópeloszlása (38) ... 95
I.57. Az Me3E (E = P, As, Sb. Bi) vegyületsor He(I) fotoelektronspektruma (41) ... 98
I.58. A Mo(PF3)6 He(I) fotoelektronspektruma (44) ... 99
I.59. Vaskomplexek Na2Fe(CN)5NO 2H2O-hoz viszonyított izomereltolódási tartománya ... 100
I.60. Ónvegyületek SnO9-hoz viszonyított izomereltolódási tartománya ... 100
I.61. Vas-karbonilok Mössbauer-spektruma ... 101
I.62. A Cr2Ac4 gázfázisú (a); és szilárdfázisú (b) szerkezete (1) ... 103
I.63. A Li4(CH3)4 szerkezete (53) ... 104
II.1. A 11-14. csoportokba tartozó elemek metilszármazékainak képződéshője az elemek rendszámának függvényében ... 113
(II.1.). ... 114
(II.2.). ... 115
(II.3.). ... 115
(II.4.). ... 116
(II.5.). ... 117
(II.6.). ... 117
(II.7.). ... 117
(II.8.). ... 118
(II.9.). ... 118
(II.10.). ... 118
(II.11.). ... 118
(II.12.). ... 119
(II.13.). ... 119
(II.14.). ... 119
(II.15.). ... 119
II. 2. A poláris fémorganikus vegyületek fém-szén kötéséhez tartozó pillératomok tulajdonságai ... 120
(II.16.). ... 121
(II.17.). ... 121
(II.18.). ... 122
(II.19.). ... 122
(II.20.). ... 123
(II.21.). ... 124
(II.22.). ... 124
II. 3. A dilítio-naftalin TMEDA-komplex (a) és a „Freeman’s-reagens” (b) szerkezete ... 125
(II.23.). ... 125
(II.24.). ... 126
(II.25.). ... 126
(II.26.). ... 126
(II.27.). ... 127
(II.28.). ... 127
(II.29.). ... 127
(II.30.). ... 128
(II.31.). ... 129
(II.32.). ... 129
(II.33.). ... 130
(II.34.). ... 130
(II.35.). ... 130
(II.36.). ... 131
II.4. Akirális (TMEDA, PMDTA) és királis (Spartein) aktiváló ligandumok ... 132
II.5. A hidrogén-fém kicserélési reakció négycentrumos átmeneti állapotának szerkezete tetrahidrofurán (a), TMEDA (b), alkáli-alkoholát (c) és komplexképző szomszédcsoport (d) jelenlétében ... 132
(II.37.). ... 133
(II.38.). ... 134
(II.39.). ... 134
(II.40.). ... 134
(II.41.). ... 136
II.6. A szerves lítiumyegyületek 7Li kémiai eltolódásértékei ciklopentánban és dietil-éterben ... 137
II.7. Az anizol:butil-lítium = 1:1 arányú elegy (a), és az anizol:butil-lítium:TMEDA = 1:1:1 elegy (b) 6Li,1HHOESY-spektruma ... 138
(II.42.). ... 139
II.8. A lítium-perklorát bisz-dietiléterát (9), a lítium-tetrafluoroborát bisz-cisz,cisz-1,2;3,4;5,6-triepoxiciklohexán-komplex (10) és a rubidium- tiocianát kriptand-komplexének (11) molekulaszerkezete (a koordinációs kötéseket szaggatott vonal jelöli) ... 140
II.9. A poláris fémorganikus vegyületek aggregátumainak tipikus szerkezeti egységei ... 141
II.10. A metil-lítium (a) és a metil-kálium (b) elrendeződése kristályaik elemi celláiban ... 141
II.11. A 2,4,6-trimetilfenil-lítium tetrahidrofurános szolvátjának (a) és a 2,2’-dilítio-difenil TMEDA-komplexének (b) szerkezete röntgenkrisztallográfiai mérések alapján ... 142
(II.43.). ... 143
(II.44.). ... 144
(II.45.). ... 145
(II.46.). ... 145
(II.47.). ... 145
(II.48.). ... 146
(II.49.). ... 147
II.12. A Grignard-vegyületek képződésének (II.49. egyenlet) részfolyamatai; a metil-jodid katalitikus hatása ... 147
(II.50.). ... 148
(II.51.). ... 148
(II.52.). ... 149
(II.53.). ... 149
(II.54.). ... 149
(II.55.). ... 150
II.13. A dimetil-berillium monomer, dimer és trimer szerkezete ... 150
II.14. A fenil-magnézium-bromid oligomer szerkezete dietil-éterben ... 150
(II.56.). ... 151
II.15. A Grignard-vegyületek néhány jellegzetes kémiai reakciója ... 152
(II.57.). ... 152
(II.58.). ... 153
(II.59.). ... 154
(II.60.). ... 154
(II.61.). ... 154
(II.62.). ... 154
(II.63.). ... 155
(II.64.). ... 155
II.16. A dimetil-cink (a), valamint dimetil-éterátjának (b), és a dibutil-cink TMEDA-komplexének (c) szerkezete ... 155
II.17. Az alkil-cink-halogenidek jellemző asszociátumai ... 156
II.18. A Zn(Cp*)2 (a) és a Cp*HgCl (b) komplexek szerkezete ... 156
(II.65.). ... 157
(II.66.). ... 157
(II.67.). ... 157
(II.68.). ... 158
(II.69.). ... 158
(II.70.). ... 158
(II.71.). ... 159
II.19. A Novurit vízhajtó szerkezeti képlete ... 159
(II.72.). ... 160
(II.73.). ... 160
(II.74.). ... 160
(II.75.). ... 161
(II.76.). ... 162
(II.77.). ... 162
(II.78.). ... 162
(II.79.). ... 163
(II.80.). ... 163
II.20. A (LiCuMe2)2-molekula szerkezete és a dimer disszociációs egyensúlyi reakciója oldatban ... 163
II.21. A szerves rézvegyületek fontosabb helyettesítéses reakciói ... 164
II.22. A3,5,5-trimetil-ciklohex-2-en-1-on 1,4-konjugált addíciós reakciójának termelése a reagens minőségének függvényében ... 165
(II.81.). ... 165
II.23. Fémorganikus reakciók reaktorának víz- és oxigénmentesítő rendszere ... 166
(II.82.). ... 167
(II.83.). ... 168
(II.84.). ... 168
(II.85.). ... 169
(II.86.). ... 169
II.24. Grignard-reagensek enantioszelektív addíciója prokirális oxovegyületekre TADDOL jelenlétében (Ar=fenil-, 2-naftilcsoport) ... 170
(II.87.). ... 182
(II.88.). ... 182
(II.89.). ... 182
(II.90.). ... 182
(II.91.). ... 183
(II.92.). ... 183
(II.93.). ... 183
(II.94.). ... 183
II.25. Karborán termikus izomerizációja ( a • a szénatomokat jelöli) ... 183
(II.95.). ... 185
(II.96.). ... 185
(II.97.). ... 185
(II.98.). ... 186
(II.99.). ... 186
(II.100.). ... 186
(II.101.). ... 187
II.26. A trimetil-aluminium dimerek szerkezete ... 187
(II.102.). ... 187
(II.103.). ... 188
(II.104.). ... 188
(II.105.). ... 189
(II.106.). ... 189
(II.107.). ... 190
(II.108.). ... 190
(II.109.). ... 190
(II.110.). ... 190
(II.111.). ... 191
(II.112.). ... 191
(II.113.). ... 191
(II.114.). ... 192
(II.115.). ... 192
(II.116.). ... 193
(II.117.). ... 193
(II.118.). ... 193
(II.119.). ... 194
(II.120.). ... 194
(II.121.). ... 194
(II.122.). ... 194
(II.123.). ... 195
(II.124.). ... 195
(II.125.). ... 195
(II.126.). ... 195
(II.127.). ... 197
(II.128.). ... 197
(II.129.). ... 197
(II.130.). ... 197
(II.131.). ... 197
(II.132.). ... 198
(II.133.). ... 198
(II.134.). ... 199
(II.135.). ... 200
(II.136.). ... 200
(II.137.). ... 201
II.27. A szerves ólomvegyületek jellemző koordinációs komplexei ... 202
(II.138.). ... 202
(II.139.). ... 202
(II.140.). ... 202
(II.141.). ... 203
(II.142.). ... 204
(II.143.). ... 204
(II.144.). ... 204
(II.145.). ... 204
(II.146.). ... 204
(II.147.). ... 205
(II.148.). ... 205
II.28. A trialkil-antimon jellegzetes átalakulási reakciói ... 206
(II.149.). ... 206
(II.150.). ... 207
(II.151.). ... 207
(II.152.). ... 208
(II.153.). ... 209
(II.154.). ... 209
(II.155.). ... 210
III.1. Az átmenetifém és a ligandum közötti σ/π kölcsönhatás ... 213
(III.1.). ... 215
(III.2.). ... 216
(III.3.). ... 216
(III.4.). ... 216
(III.5.). ... 217
III.2. 1-ciano-etil-csoportot tartalmazó vaskomplex ... 217
(III.6.). ... 217
(III.7.). ... 218
(III.8.). ... 218
(III.9.). ... 218
(III.10.). ... 218
(III.11.). ... 219
(III.12.). ... 219
(III.13.). ... 220
III.3. A trisz-(2-dimetilarzino-tolil)-króm(III) szerkezete ... 220
(III.14.). ... 221
III.4. Kobalamin-származékok szerkezete ... 222
III.5. A bisz(dimetilglioximáto)-metil-piridin-kobalt szerkezete ... 223
III.6. Bisz(μ-metil)-bisz(η3-l,3-dimetilallil)Ni2 -komplex szerkezete ... 223
III.7. Ru2(μ-CH3)(μ-CO)(CO)2(Cp)2 -komplex szerkezete ... 223
(III.19.). ... 224
(III.20.). ... 224
(III.21.). ... 225
(III.22.). ... 225
(III.23.). ... 225
III.8. A transz-Pt(2,4,6-Me3-Ph)2(PR3)2-komplex szerkezete ... 226
(III.24.). ... 226
(III.25.). ... 227
(III.26.). ... 227
(III.27.). ... 227
(III.28.). ... 227
III.9. σ/π-hídhelyzetü ligandumot tartalmazó kétmagvú vaskomplex szerkezete ... 228
(III.29.). ... 229
(III.30.). ... 229
(III.31.). ... 229
(III.32.). ... 229
(III.33.). ... 230
(III.34.). ... 230
(III.35.). ... 230
(III.36.). ... 231
(III.37.). ... 231
(III.38.). ... 231
(III.39.). ... 231
III.10. A Ta=CHCMe3 szerkezeti részletet tartalmazó komplex szerkezete ... 232
III.11. MC(X)Y szerkezeti részletet tartalmazó Fischer-karbének mezomer határformái ... 232
(III.40.). ... 233
(III.41.). ... 233
(III.42.). ... 234
(III.43.). ... 234
(III.44.). ... 234
(III.45.). ... 234
(III.46.). ... 235
III.12. Átmenetifém-acil-komplexek és rokon származékaik ... 235
(III.47.). ... 236
(III.48.). ... 236
(III.49.). ... 236
(III.50.). ... 237
III.13. A cirkónium η2-acetil-komplexe ... 237
(III.51.). ... 237
III.14. Hídhelyzetü η2-acetil-ligandumot tartalmazó Zr-Mo-komplex ... 238
(III.52.). ... 239
(III.53.). ... 239
(III.54.). ... 239
(III.55.). ... 239
(III.56.). ... 240
(III.57.). ... 240
(III.58.). ... 240
III.15. A W(dmpe)(CH2CMe3)(CHCMe3)(CCMe3) szerkezete ... 241
III.16. Dialkilamino-alkilidin-komplexek mezomer határformái ... 241
(III.59.). ... 241
(III.60.). ... 242
(III.61.). ... 242
(III.62.). ... 242
(III.63.). ... 242
(III.64.). ... 243
(III.65.). ... 243
III.17. A réz-alkinil-komplexek polimer szerkezete ... 244
(III.66.). ... 244
III.18. A Pt(PPhMe2)2(CCPh)Cl-komplex szerkezete ... 244
(III.67.). ... 245
(III.68.). ... 252
(III.69.). ... 252
(III.70.). ... 252
(III.71.). ... 253
(III.72.). ... 253
(III.73.). ... 253
(III.74.). ... 253
(III.75.). ... 253
(III.76.). ... 253
(III.77.). ... 254
III.19. A biner karbonilok szerkezete ... 255
III.20. A Co2(CO)8 oldatban kimutatható szerkezeti izomerjei ... 255
III.21. Kétmagvú, „félhídhelyzetű” karbonilligandumot tartalmazó komplex szerkezete, valamint a karbonilligandumok σ/π aszimmetrikus hídhelyzetű koordinációja ... 256
(III.78.). ... 258
(III.79.). ... 258
(III.80.). ... 259
(III.81.). ... 259
(III.82.). ... 259
(III.83.). ... 259
(III.84.). ... 260
III.22. A (HFe(CO)4)- előállításának feltételezett kulcsintermedierje ... 260
(III.85.). ... 260
(III.86.). ... 260
(III.87.). ... 260
(III.88.). ... 261
(III.97.). ... 263
(III.98.). ... 264
(III.99.). ... 264
III.23. Tiokarbonilkomplexek koordinációjának típusai ... 265
III.24. A Fe2(μ-CS)2(CO)2(Cp)2-komplex szerkezete ... 265
(III.100.). ... 265
(III.101.). ... 266
(III.102.). ... 266
(III.103.). ... 266
III.25. Szén-monoxid és alkil-izocianid szerkezetének összehasonlítása ... 267
(III.104.). ... 267
III.26. Az M(CNR)-részlet lehetséges mezomer határszerkezetei ... 268
(III.105.). ... 268
(III.106.). ... 268
(III.107.). ... 272
(III.108.). ... 273
(III.109.). ... 273
(III.110.). ... 273
(III.111.). ... 273
(III.112.). ... 273
(III.113.). ... 274
(III.114.). ... 274
(III.115.). ... 274
(III.116.). ... 275
(III.117.). ... 275
III.27. Rh(Cp)(C2Η4)(C2F4)-komplex szerkezete ... 276
(III.118.). ... 276
(III.119.). ... 277
(III.120.). ... 277
(III.121.). ... 277
(III.122.). ... 278
(III.123.). ... 278
(III.124.). ... 279
(III.125.). ... 279
(III.126.). ... 279
(III.127.). ... 280
(III.128.). ... 280
(III.129.). ... 281
III.28. A Mn2Cp2(CO)4(η2(C,E), η1(E)-CH2=E)-komplexek szerkezete ... 281
III.29. Az 1-fenil-2-metoxi-3-metil-1-foszfabutadién koordinációja W(CO)n (n=1,2) szerkezeti egységekhez ... 281
(III.130.). ... 282
(III.131.). ... 282
(III.132.). ... 282
(III.133.). ... 283
(III.134.). ... 283
(III.135.). ... 284
(III.136.). ... 285
(III.137.). ... 285
(III.138.). ... 286
(III.139.). ... 286
(III.140.). ... 286
(III.141.). ... 286
(III.142.). ... 287
(III.143.). ... 287
(III.144.). ... 287
(III.145.). ... 287
(III.146.). ... 288
(III.147.). ... 288
III.30. A bisz(2-metallil)nikkel szerkezete ... 288
(III.148.). ... 289
(III.149.). ... 289
(III.150.). ... 290
(III.151.). ... 290
(III.152.). ... 290
(III.153.). ... 291
(III.154.). ... 291
(III.155.). ... 291
III.31. A bisz(2,3,4-trimetilpentadienil)-ruténium szerkezete ... 292
(III.156.). ... 292
(III.157.). ... 293
(III.158.). ... 294
III.32. Különböző M(C3Ph3)-egységet tartalmazó komplexek szerkezete ... 294
(III.159.). ... 295
(III.160.). ... 295
(III.161.). ... 296
III.33. A Ni(η4-C4Ph4)2-komplex szerkezete ... 296
(III.162.). ... 296
(III.163.). ... 297
(III.164.). ... 297
(III.165.). ... 297
(III.166.). ... 298
(III.167.). ... 298
(III.168.). ... 298
(III.169.). ... 298
(III.170.). ... 298
(III.171.). ... 298
III.34. A ferrocén szerkezete és fontosabb térszerkezeti jellemzői (42) ... 299
III.35. A „titanocén” szerkezete ... 299
III.36. Cp-anellált gyűrűrendszerek ... 300
III.37. A (Ni2Cp3)+ szerkezete ... 300
(III.172.). ... 300
(III.173.). ... 301
(III.174.). ... 301
(III.175.). ... 301
(III.176.). ... 302
(III.177.). ... 302
(III.178.). ... 302
(III.179.). ... 303
III.38. A MnCp(CO)3 félszendvics szerkezete ... 303
III.39. A Ni2(μ-CO)2Cp2 és az Os2(CO)4Cp2 szerkezete ... 303
(III.180.). ... 303
(III.181.). ... 304
(III.182.). ... 304
(III.183.). ... 304
(III.184.). ... 304
III.40. A ReHCp2- és a MoH2Cp2-komplexek hajlott szendvics szerkezete ... 305
(III.185.). ... 305
(III.186.). ... 305
(III.187.). ... 306
(III.188.). ... 306
(III.189.). ... 306
(III.190.). ... 306
(III.191.). ... 306
(III.192.). ... 307
III.41. M(η6-PhCl)2- és M(η6-PhNMe2)2-komplexek szerkezete (M’=Cr, Mo) ... 307
III.42. A (η12-(2,2) paraciklofán)Cr(0)-komplex szerkezete ... 307
(III.193.). ... 308
(III.194.). ... 308
(III.195.). ... 309
(III.196.). ... 310
(III.197.). ... 310
(III.198.). ... 310
(III.199.). ... 310
(III.200.). ... 310
(III.201.). ... 311
(III.202.). ... 311
(III.203.). ... 312
(III.204.). ... 312
(III.205.). ... 312
III.43. Az uranocén szerkezete ... 313
III.44. A Cr2(C8H8)3-komplex szerkezete ... 313
III.45. A Ni2(C8H8)2-komplex szerkezete ... 313
(III.206.). ... 314
(III.207.). ... 314
(III.208.). ... 315
(III.209.). ... 315
(III.210.). ... 315
(III.211.). ... 316
(III.212.). ... 316
(III.213.). ... 316
(III.214.). ... 324
(III.215.). ... 324
(III.216.). ... 324
(III.217.). ... 325
IV.1. Átmenetifém-organikus komplexek általános szerkezete ... 327
IV.2. Alkének redukciója monohidrido-komplexekkel ... 329
IV.3. Alkének redukciója dihidridkomplexekkel (Wilkinson-katalizátor) ... 330
IV.4. Néhány királis difoszfánligandum ... 331
IV.5. Enamidok aszimmetrikus hidrogénezésének mechanizmusa ... 331
(IV.1.). ... 332
(IV.2.). ... 332
(IV.3.). ... 332
(IV.4.). ... 333
(IV.5.). ... 333
(IV.6.). ... 333
(IV.7.). ... 334
(IV.8.). ... 334
(IV.9.). ... 334
IV.6. A Crabtree-katalizátor előállítása és reaktivitása ... 335
(IV.10.). ... 335
(IV.11.). ... 336
IV.7. A katalitikus hidroborálás és hidroszililezés mechanizmusa ... 337
(IV.12.). ... 337
(IV.13.). ... 337
(IV.14.). ... 337
(IV.15.). ... 338
(IV.16.). ... 338
IV.8. σ-fémorganikus vegyületek előállítása és átalakításai ... 341
IV.9. σ-fémorganikus komplexek szintézise oxidatív addícióval ... 342
IV.10. σ-fémorganikus komplexek szintézise transzmetallálással ... 343
IV.11. σ-fémorganikus komplexek szintézise hidrometallálással ... 343
(IV.17.). ... 344
IV.12. σ-fémorganikus komplexek szintézise karbometallálással ... 344
(IV.18.). ... 345
(IV.19.). ... 346
(IV.20.). ... 346 (IV.21.). ... 347 IV.13. σ-fémorganikus komplexek szintézise ciklometallálással ... 347 (IV.22.). ... 348 (IV.23.). ... 349 (IV.24.). ... 349 IV.14. A keresztkapcsolási reakciók általános mechanizmusa ... 351 (IV.25.). ... 351 (IV.26.). ... 352 (IV.27.). ... 352 (IV.28.). ... 352 (IV.29.). ... 353 IV.15. Az organopalládium-halogenid-komplex aktiválása ... 353 (IV.30.). ... 354 (IV.31.). ... 354 (IV.32.). ... 354 (IV.33.). ... 355 (IV.34.). ... 355 (IV.35.). ... 355 (IV.36.). ... 356 (IV.37.). ... 356 (IV.38.). ... 356 (IV.39.). ... 357 (IV.40.). ... 357 (IV.41.). ... 357 (IV.42.). ... 358 (IV.43.). ... 359 (IV.44.). ... 359 (IV.45.). ... 359 (IV.46.). ... 360 IV.16. A Heck-reakció általános mechanizmusa és néhány új, hatékony ligandum ... 360 (IV.47.). ... 361 (IV.48.). ... 361 (IV.49.). ... 362 (IV.50.). ... 362 (IV.51.). ... 362 (IV.52.). ... 363
(IV.53.). ... 363 IV.17. Karbonilatív keresztkapcsolás általános mechanizmusa ... 364 (IV.54.). ... 364 (IV.55.). ... 364 IV.18. Karbonilkomplexek reaktivitása ... 369 (IV.56.). ... 370 (IV.57.). ... 370 IV.19. Collman-reagensből kiinduló átalakítások ... 371 (IV.58.). ... 371 (IV.59.). ... 371 (IV.60.). ... 372 IV.20. A Wilkinson-katalizátorral kiváltott dekarbonilezés mechanizmusa ... 372 (IV.61.). ... 373 (IV.62.). ... 373 (IV.63.). ... 374 (IV.64.). ... 374 (IV.65.). ... 375 (IV.66.). ... 375 (IV.67.). ... 375 IV.21. A ródiumkatalizált hidroformilezés általános mechanizmusa ... 376 (IV.68.). ... 376 (IV.69.). ... 377 IV.22. A hidrokarboxilezés mechanizmusa ... 378 (IV.70.). ... 378 (IV.71.). ... 378 (IV.72.). ... 379 IV.23. A Monsanto-féle ecetsavszintézis mechanizmusa ... 379 IV.24. A Pauson–Khand-reakció feltételezett mechanizmusa ... 380 (IV.73.). ... 381 (IV.74.). ... 381 (IV.75.). ... 381 IV.25. Karbének általános szerkezete ... 384 IV.26. Heteroatomokkal stabilizált (Fischer) karbének reaktivitása ... 385 (IV.76.). ... 386 (IV.77.). ... 386 (IV.78.). ... 386 (IV.79.). ... 387
(IV.80.). ... 387 (IV.81.). ... 388 (IV.82.). ... 388 IV.27. A Dötz-reakció mechanizmusa ... 389 (IV.83.). ... 389 (IV.84.). ... 389 (IV.85.). ... 390 (IV.86.). ... 390 (IV.87.). ... 390 (IV.88.). ... 391 (IV.89.). ... 391 IV.28. Átmenetifémekkel katalizált ciklopropanálás mechanizmusa diazovegyületekkel ... 392 (IV.90.). ... 392 (IV.91.). ... 393 (IV.92.). ... 393 (IV.93.). ... 393 (IV.94.). ... 394 IV.29. Az alkénmetatézis általános mechanizmusa és néhány új típusú katalizátor ... 395 (IV.95.). ... 395 (IV.96.). ... 396 (IV.97.). ... 396 (IV.98.). ... 396 IV.30. A Tebbe-reagens előállítása és reaktivitása ... 397 (IV.99.). ... 397 (IV.100.). ... 397 IV.31. Átmenetifém-alkén-komplexek reakciói ... 401 IV.32. A Wacker-oxidáció mechanizmusa ... 402 (IV.101.). ... 402 (IV.102.). ... 403 (IV.103.). ... 403 (IV.104.). ... 403 (IV.105.). ... 404 (IV.106.). ... 404 (IV.107.). ... 404 (IV.108.). ... 405 IV.33. A palládium(II)-vel katalizált (3,3) átrendeződés mechanizmusa ... 405 (IV.109.). ... 405
(IV.110.). ... 405 IV.34. Vas(II)-alklén-komplexek előállítása és továbbalakítása ... 406 (IV.111.). ... 406 (IV.112.). ... 407 (IV.113.). ... 408 (IV.114.). ... 408 (IV.115.). ... 409 (IV.116.). ... 409 (IV.117.). ... 409 IV.35. Átmenetifém-katalizáit (4+2) cikloaddíció feltételezett mechanizmusa ... 409 (IV.118.). ... 410 (IV.119.). ... 410 (IV.120.). ... 410 (IV.121.). ... 411 (IV.122.). ... 414 (IV.123.). ... 414 (IV.124.). ... 414 (IV.125.). ... 415 (IV.126.). ... 416 (IV.127.). ... 416 IV.36. Alkinek kobaltkatalizált trimerizációja ... 417 (IV.128.). ... 417 (IV.129.). ... 417 (IV.130.). ... 418 (IV.131.). ... 418 (IV.132.). ... 419 (IV.133.). ... 419 (IV.134.). ... 420 (IV.135.). ... 420 (IV.136.). ... 421 (IV.137.). ... 421 (IV.138.). ... 421 IV.37. η3-allilkomplexek előállításának lehetséges módjai ... 424 IV.38. Konjugált diének telomerizációjának általános mechanizmusa ... 424 (IV.139.). ... 425 (IV.140.). ... 425 (IV.141.). ... 425
(IV.142.). ... 426 IV.39. Allil-palládium-komplexek általános reaktivitása ... 426 (IV.143.). ... 427 (IV.144.). ... 427 (IV.145.). ... 428 (IV.146.). ... 428 (IV.147.). ... 428 (IV.148.). ... 429 (IV.149.). ... 429 (IV.150.). ... 429 (IV.151.). ... 430 (IV.152.). ... 430 (IV.153.). ... 431 (IV.154.). ... 431 (IV.155.). ... 432 (IV.156.). ... 432 (IV.157.). ... 432 (IV.158.). ... 433 (IV.159.). ... 433 (IV.160.). ... 433 (IV.161.). ... 434 IV.40. Palládium-trimetilénmetán-komplex szintézise és reaktivitása ... 434 (IV.163.). ... 435 (IV.164.). ... 435 (IV.165.). ... 435 (IV.166.). ... 436 (IV.167.). ... 436 IV.41. Átmenetifém-arén-komplexek előállítása és reaktivitása ... 439 (IV.168.). ... 440 (IV.169.). ... 440 (IV.170.). ... 441 (IV.171.). ... 441 IV.42. Nukleofil támadás arén-króm-komplexekre ... 442 (IV.172.). ... 442 IV.43. A planáris kiralitás jelensége és néhány jellemző példa ... 442 (IV.173.). ... 443 (IV.174.). ... 443
(IV.175.). ... 444 (IV.176.). ... 445 (IV.177.). ... 445 (IV.178.). ... 445 (IV.179.). ... 445 (IV.180.). ... 446 (IV.181.). ... 446 (IV.182.). ... 446 (IV.183.). ... 447 (IV.184.). ... 447 (IV.185.). ... 447 (IV.186.). ... 448 (IV.187.). ... 448 (IV.188.). ... 448 (IV.189.). ... 449 (IV.190.). ... 449 (IV.191.). ... 449
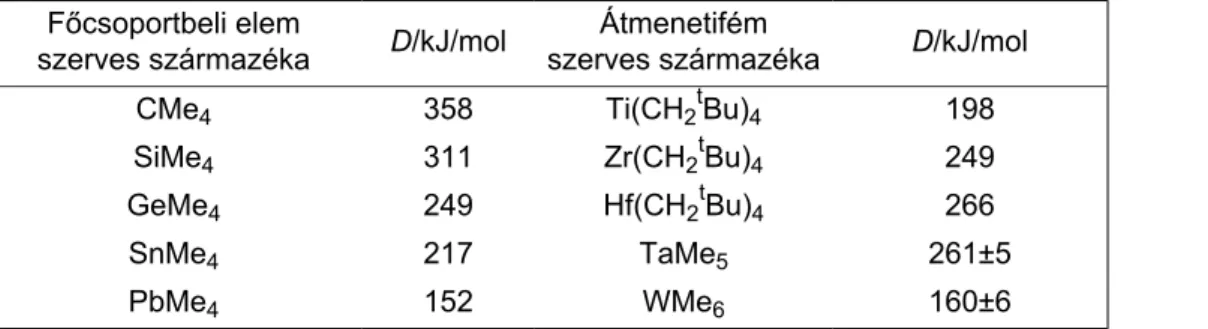
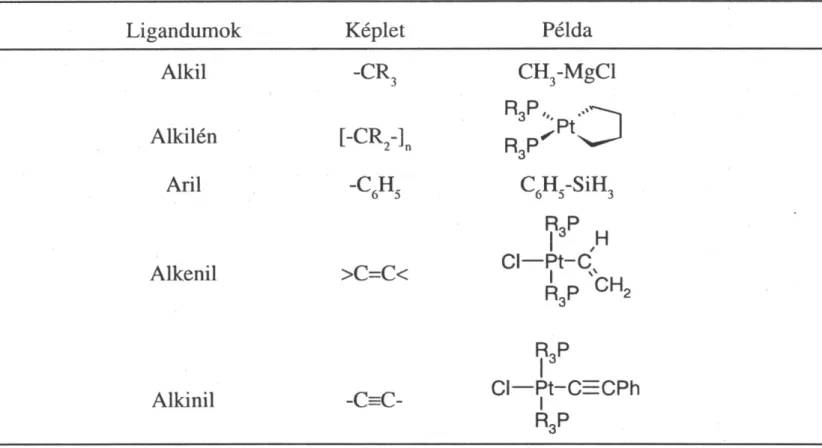
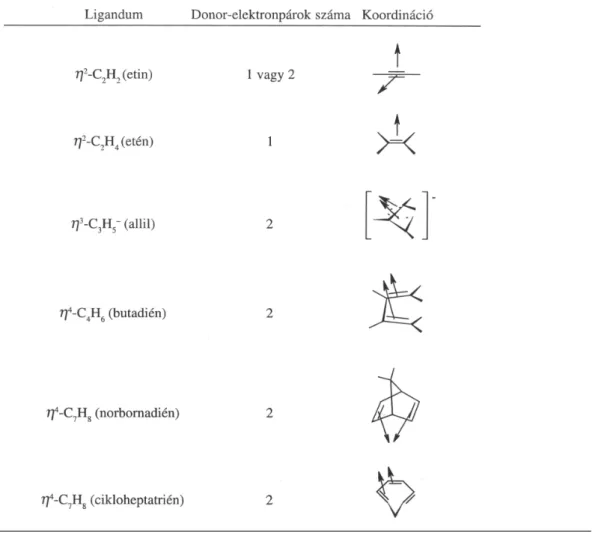
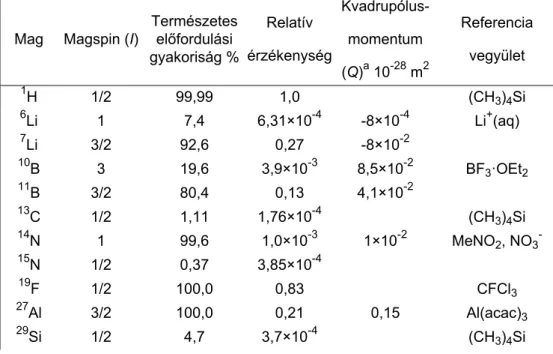
I.1. Néhány főcsoportbeli elem- és átmenetifém-szén kötés kötésdisszociációs energiája (D/kJ/mol) (3) ... 20 I.2. A fématomhoz σ-kötéssel kapcsolódó ligandumok ... 24 I.3. ν(NO) vegyértékrezgési frekvenciák szabad molekulában/ionban és ligandumban ... 28 I.4. A szerves π-donor-ligandumok néhány jellemző képviselője és koordinációs sajátságaik ... 31 I.5. Néhány foszfortartalmú ligandum kúpszöge (θ) ... 42 I.6. Gyakrabban előforduló egyszerű ligandumok és a donorelektronpárok száma ... 45 I.7. Fontosabb spektroszkópiai technikák, fizikai hátterük és az általuk vizsgált jelenségek hozzávetőleges energiatartománya ... 69 I.8. Fontosabb NMR-aktív magok mágneses jellemzői és NMR-referenciavegyületük ... 71 I.9. Néhány karbonilvegyület C-O nyújtási (ν(CO)) frekvenciája ... 84 I.10. Infravörös (IR), Raman (R) és polarizációs Raman (pR)a -aktív nyújtási (ν) és hajlítási (β) rezgési átmenetek száma a leggyakrabban
előforduló szimmetriájú molekulákban ... 86 I.11. Gerjesztett állapotok típusai fémorganikus és koordinációs vegyületekben ... 91 II.1. Az M-C, M-Cl és M-O kötések közepes kötésdisszociációs entalpiája az alumínium és a szilícium néhány vegyületében. ... 112 II.2. Az alkálifémek szerves vegyületeinek előállítási módszerei ... 122 II.3. Fontosabb irányító csoportok ... 135 II.4. Néhány szerves lítiumvegyület jellemző aggregációs foka különböző oldószerekben (DEE – dietil-éter, HEX – hexán, THF –
tetrahidrofurán ... 142 III.1. Pt-C kötéstávolságok különböző szerves ligandumok Pt(II) komplexeiben. ... 215 III.2. Biner karbonilok ... 251 III.3. A karbonilligandum különböző koordinációihoz tartozó ν(CO) hullámszámértékek ... 256 III.4. A fémen lévő negatív töltés hatása átmenetifém-karbonilkomplexek ν(CO) hullámszámértékeire ... 256 III.5. L3Mo(CO)3-komplexek ν(CO) értékei ... 257 III.6. Kalkogén-karbonil-komplexek jellegzetes ν(CE) értékei ... 264 III.7. (4-CH3-C6H4)-NC szabad ligandum (L) és átmenetifém-komplexeinek ν(CN) ... 267 III.8. Átmenetifém-alkin-komplexek szerkezeti adatai ... 282 III.9. Különböző, M(C3Ph3) -egységet tartalmazó komplexek M-C(ciklopropenil) kötéstávolságai ... 294 III.10. A ferrocén Cp gyűrűinek elhelyezkedése különböző kristályformákban ... 299 III.11. Karbénanalóg szerkezeti egységet szolgáltató komplexek néhány típusa (a táblázatban csupán a „karbénfragmenseket”
szerepeltetjük) ... 323
Könyvünk megírásánál az a cél vezetett bennünket, hogy megkíséreljünk átfogó képet adni a fémorganikus kémia jelenlegi állásáról az egyetemi alapképzésben résztvevő hallgatók (vegyész, vegyészmérnök, középiskolai kémiatanár, környezetmérnök, környezeti kémikus), valamint a téma iránt érdeklődő ipari szakemberek és középiskolai tanárok számára. Mivel egy ilyen széles szakmai közönség érdeklődése szerteágazó, nyilvánvalóan csupán az alapvető fémorganikus kémiai ismeretek bemutatására vállalkozhattunk. Olyan kutatók esetében, akik kutatásaik során a fémorganikus kémia valamely részterületére kalandoznak, csupán a figyelem felkeltése, néhány összefüggés bemutatása lehet a célunk. A megadott általános irodalom és néhány eredeti szakmai közlemény áttekintése az ő esetükben is segítséget adhat a szakterület mélyebb megismerésére.
Mint több alfejezetben is utalunk rá, szinte minden magyar nyelvű szervetlen és szerves kémia tankönyv tárgyalja a fémorganikus kémia bizonyos részterületeit, mint pl. a fém-szén σ- vagy π-kötést tartalmazó vegyületek szintézisét, szerkezeti jellemzőit vagy reaktivitását. Tudomásunk szerint azonban magyar nyelvű tankönyv szerzői első ízben tesznek kísérletet arra, hogy négy, számos ponton kapcsolódó alfejezetre bontva átfogóan ismertessék a fémorganikus kémia legfontosabb alapelemeit. A feladat nem egyszerű, mert a kémiának ez a területe nagyon dinamikusan fejlődik. Az egy évtizeddel ezelőtt született, akkor kuriózumszámba menő alapvető felismerések ma már szintetikus homogénkatalitikus eljárások alapjául szolgálnak, a főcsoportbeli fémek szerves származékai mellett az átmenetifém-organikus vegyületek is a szintetikus vegyészek mindennapi eszközeivé váltak. Ezt a fejlődést bárki könnyen nyomon követheti, ha valamely vezető szintetikus kémiai folyóiratban megjelenő közleményeket ebből a szempontból vizsgálja. A klasszikus lítium- és magnéziumorganikus vegyületek mellett pl. egyre nagyobb teret kapnak az alumínium és az ón szerves származékai. A forradalmi változást azonban az átmenetifém-organikus származékok hozták, amelyek általában csupán intermedierként jelennek meg különböző átmenetifémek segítségével lejátszódó – és gyakran főcsoportbeli fémek szerves származékait alkalmazó – homogénkatalitikus reakciókban. Összességében arra a – sokak számára talán meglepő – eredményre jutunk, hogy szinte minden új közlemény tartalmaz legalább egy-egy reakciót, amely fémek szerves származékainak alkalmazását igényli.
Elsősorban felsőbb évfolyamokon tartott speciálkollégiumi és alapkurzusokon szerzett tapasztalataink alapján elmondhatjuk, hogy szervetlen, szerves kémiai, valamint alapvető fizikai-kémiai és analitikai ismeretek birtokában a fémek szerves kémiájának ilyen mélységű tárgyalása eredményesen megoldható.
A könyv elsősorban a fémorganikus kémia műveléséhez szükséges alapismeretek és gondolkodásmód kifejlesztését tűzi ki célul és sem az elmélet, sem a gyakorlat területén nem törekszik teljességre. (Könnyen belátható, hogy „teljességről” szó sem eshet, ha arra gondolunk, hogy könyvünk
„alalfejezeteiben” tárgyalt reakciókról általában önálló szakkönyvek jelennek meg.)
A könyv tartalmazza a legfontosabb elméleti alapokat, a reakciókészség, a reakciómechanizmusok magyarázatának azon legfőbb elemeit, amelyek kiindulópontul szolgálhatnak a további irodalmakban való tájékozódás során. A területen jártas olvasó számára bizonyára szemet szúr, hogy viszonylag kis teret kap a könyvben a reakciómechanizmusok tárgyalása, különösen néhány vitatott reakció esetében. A rendelkezésünkre álló terjedelem ezek részletesebb elemzésére nem nyújtott lehetőséget. Még néhány olyan – más könyvekben főfejezetként szereplő – vegyületcsalád is
„kitekintés”, „széljegyzet” vagy utalás formában jelenhet csak meg, mint pl. az átmenetifém-hidridek vagy a szilícium szerves származékai. Néhány alapvető fontosságú analitikai (NMR, IR, ESR, stb.) eredményt is csak hasonló formában tudunk bemutatni.
A könyv alfejezetei a következők: 1) A szerves fémvegyületek általános jellemzése (elméleti háttér). 2) A főcsoportbeli elemek fémorganikus vegyületei (szerkezet, előállítás, reaktivitás) és gyakorlati alkalmazásuk. 3) Az átmenetifémek fémorganikus vegyületei (szerkezet, előállítás, reaktivitás). 4) Átmenetifém-organikus vegyületek alkalmazása szerves szintézisekben (laboratóriumi és ipari alkalmazások).
A könyv szerzői ezúton szeretnének köszönetet mondani a könyv lektorálásáért Markó László akadémikusnak és Tímári Gézának, a kémiai tudomány kandidátusának.
Ugyancsak köszönet illeti a könyv szerkesztésének munkáiért Csóka Balázst, Kotschy Pétert, Novák Zoltánt, Pusztai Zoltánt és Vincze Zoltánt.
Köszönettel tartozunk a Nemzeti Tankönyvkiadó munkatársainak a könyv elkészítésében nyújtott segítségükért.
Őszintén reméljük, hogy könyvünk több kiadást megér és a korszerű egyetemi kémiaoktatás jól használható tankönyve lesz. Remélhetőleg korábban végzett szakemberek számára is lehetőséget nyújt a terület felfedezésére és ismereteik elmélyítésére. Mint a szakterület első magyar nyelven megjelenő könyve, biztosan számos következetlenséget, kisebb-nagyobb hibát is tartalmaz. Mindnyájan köszönettel vesszük, ha ezekre felhívják figyelmünket, és megjegyzéseiket eljuttatják a szerkesztő címére.
Budapest – Pécs, 2000. szeptember
Vegyületek rövidítése
Ac – acetilcsoport Ar – arilcsoport
BINAP – 2,2’-bisz(difenilfoszfano)-1,1’-binaftil
BINAPHOS – 2-(difenilfoszfano)-1,1’-binaftalen-2’-il-difenilfoszfit BOC – terc-butoxikarbonil
BPE – 1,2-bisz(2’,5’-dialkil-2,3,4,5-tetrahidro-1H-foszfolo)-etán Bu – butilcsoport
sBu – szek-butilcsoport
tBu – terc-butilcsoport
CAN – cérium(IV)-ammónium-nitrát CDT – ciklododekatrién
CHIRAPHOS – 2,3-bisz(difenilfoszfano)-bután COD – ciklookta-1,5-dién
COT – ciklookta-1,3,5,7-tetraén Cp – ciklopentadienidcsoport
Cp* – pentametil-ciklopentadienidcsoport Cy – ciklohexilcsoport
DBBS – O,O’-dibenzoil-(R,R)-borkősav
DBU – 1,8-diazabiciklo[5.4.0]-undec-7-én DDQ – 2,3-diklór-5,6-diciano-1,4-benzokinon DEE – dietil-éter (Et2O)
diglym – bisz(2-metoxietil)-éter
DIOP – 2,3-O-izopropilidén-2,3-dihidroxi-1,4-bisz(difenilfoszfano)-bután DIPAMP – 1,2-bisz((2-anizil)-fenilfoszfano)-etán
DMAP – 4-dimetilamino-piridin DME – 1,2-dimetoxi-etán DMF – N,N-dimetilformamid
dmpe – 1,2-bisz(dimetilfoszfano)-etán DMSO – dimetilszulfoxid
dppb – 1,4-bisz(difenilfoszfano)-bután dppe – 1,2-bisz(difenilfoszfano)-etán dppf – 1,1’-bisz(difenilfoszfano)-ferrocén dppp – l,3-bisz(difenilfoszfano)-propán
DuPHOS – 1,2-bisz(2’,5’-dialkil-2,3,4,5-tetrahidro-1H-foszfolo)-benzol EDTA – etiléndiamin-tetraecetsav
en – etilén-diamin Et – etilcsoport HEX – hexán
iPr – propán-2-il-csoport (izopropilcsoport)
LDA – lítium-diizopropilamid
LiTMP – lítium-2,2,6,6-tetrametil-piperidid MAO – metil-alumínium-oxid
MAPH – metil-alumínium-bisz(2,6-difenil-fenoxid) Me – metilcsoport
MEPY – 2-pirrolidon-5-karbonsav-metilészter MOM – metoximetil-csoport
NMO – N-metil-morfolin-N-oxid NMP – N-metil-2-pirrolidon Pent – pentilcsoport Ph – fenilcsoport
PMDTA – N,N-bisz(2-dimetilaminoetil)-metilamin(N,N,N’, N’’-pentametil-dietilén-triamin) PR3 – foszfán (triviális név: foszfin)
PTC – phase transfer catalysis, fázistranszfer katalízis PVC – poli(vinil-klorid)
py – piridin
PYBOX – 2,6-bisz(4H,5H-oxazolidin-2-il)-piridin R – szerves csoport
SAMP – (S)-l-amino-2-metoximetil-pirrolidin
TADDOL – (4R,5R)-4,5-di(hidroxi-difenil-metil)-2,2-dimetil-dioxalán TBDMS – terc-butil-dimetilszilil-csoport
TBS vagy TBDPS – terc-butil-difenilszilil-csoport TEA – trietilamin
Tf – trifluormetánszulfonil-csoport (triflátcsoport) THF – tetrahidrofurán
THP – tetrahidropiran-2-il-csoport TMANO – trimetilamin-N-oxid
TMEDA – N,N,N’,N’-tetrametil-etiléndiamin TMS – trimetil-szilil-csoport
triglyme – 2,2’-bisz(2-metoxietil)-dietiléter Ts – 4-metilbenzoszulfonil-csoport (tozilcsoport) TTA – tallium-triacetát
Z – benziloxikarbonil-csoport
Egyéb rövidítések
AE – apearance energy, megjelenési energia CC – cocondensation, „együttkondenzáció”
COSY – Correlation Spectroscopy, korrelációs spektroszkópia
CVD – Chemical Vapour Deposition, kémiai gőzfázisú rétegleválasztás DCD – Dewar-Chatt-Duncanson-modell
de – diasztereomerfelesleg
DEPT – Distortionless Enhancement by Polarisation Transfer
DFT – Density Functional Theory, sűrűségfunkcionál elmélet DGM-szabály – Davies-Green-Mingos-szabály
DMG – Directing Metallating Group, metallálást irányító csoport DoM – Directed ortho Metallation, irányított orto-metallálás
DSC – Differential Scanning Calorimetry, differenciális pásztázó kalorimetria E+ – általános elektrofil
ee – enantiomerfelesleg EN – elektronegativitás
ESR – elektronspinrezonancia-spektroszkópia ETS – elektrontranszmissziós spektroszkópia
FECS – Federation of European Chemical Societies, Európai Kémiai Társaságok Szövetsége FG – Functional Group, funkciós csoport
HF – Hartree–Fock-módszer
HOESY – Heteronuclear Overhauser Effect Spectroscopy, heteronukleáris korrelációs spektroszkópia HOMO – Highest Occupied Molecular Orbital, legmagasabb energiájú betöltött molekulapálya
IE – ionizációs energia
IL – Intra-Ligand, Ligand-Centered Transfer IR – infravörös spektrofotometria
L – ligandum
LF – Metal-Centered, Ligand Field Transfer LMCT – Ligand-to-Metal-Charge-Transfer
LUMO – Lowest Unoccupied-Molecular Orbital, legalacsonyabb energiájú üres molekulapálya M – fématom
MLCT – Metal-to-Ligand Charge-Transfer MO – Molecular Orbital, molekulapálya MSCT – Metal-to-Solvent-Charge-Transfer
NMR – Nuclear Magnetic Resonance, mágneses magrezonancia-spektroszkópia Nu – nukleofil
PSEPT – Polyhedral Skeleton Electron Pair Theory
RCM – Ring-Closing Methatesis, gyűrűzárással járó metatézis
RRKM/QET – Rice-Ramsperger-Kassel-Marcus/Quasy-Equilibrium Theory SE – elektrofil szubsztitúció
SET – Single Electron Transfer, egyelektron-átmenet SN – nukleofil szubsztitúció
TOF – Tumover Frequency, átalakulási frekvencia TON – Turnover Number, átalakulási szám UPS – ultraibolya fotoelektronspektroszkópia UV-VIS – ultraibolya-látható spektroszkópia VE – vegyértékelektronok
VUV – vákuum UV
XPS – röntgengerjesztéses fotoelektronspektroszkópia
JELLEMZÉSE
I.1. Alapfogalmak
I.1.1. A szerves fémvegyületek meghatározása, története és helye a kémiában
A szerves fémvegyületek, vagy idegen szóval fémorganikus vegyületek közvetlen fém-szén kötést tartalmaznak. Ez a definíció mind a fémek, mind a szerves környezet szempontjából további megszorításokat igényel. Számos kiadvány fémorganikus vegyületként tárgyalja a félfémek (pl. Si, Ge, As, Te) és a nemfémek (pl. B, P) szerves származékait is. Ezt a megközelítést az indokolja, hogy ezeknek az elemeknek a szerves kémiája nagyon hasonló a periódusos rendszernek ugyanabban a csoportjában található fémes elemek organikus kémiájához. Szigorúan véve a nem tipikusan fémes elemek szerves származékait az elemorganikus vegyületekhez soroljuk. Ilyen különválasztás azonban ritkán valósul meg és többnyire azzal a – didaktikai szempontokkal magyarázható – közelítő feltevéssel élünk, hogy minden, a szénnél kisebb elektronegativitású elemet (EN < 2,5) fémnek tekintünk.
A fém-szén kötésben résztvevő szerves molekularész származhat szerves iontól (többnyire karbanion, ritkábban karbokation), gyöktől vagy molekulától. Így pl. fémorganikus vegyület az etil-nátrium, (C2H5)Na, a dimetil-higany, (CH3)2Hg és a dibenzol-króm, (C6H6)2Cr, ahol rendre karbanion, gyök és semleges molekula adják a szerves molekularészt. Nem soroljuk viszont a szerves fémvegyületek közé a fémcianidokat, -izocianidokat és -karbidokat (a fém-alkinileket viszont a fémorganikus vegyületek között tartjuk számon). Ugyanígy nem tekintjük szerves fémvegyületeknek a karboránokat, amelyek bór- és szénatomokból felépülő poliéderes szerkezetek. Ezzel szemben a fém-karbonilokat, vagyis a CO-molekulát ligandumként tartalmazó átmenetifém-vegyületeket, a szerves fémvegyületek között tárgyaljuk. Ezt magyarázza az a tény, hogy a fém-karbonilok szerkezetét, kötésviszonyait, kémiai tulajdonságait és reakcióit tekintve igen hasonlók a szerves fémvegyületekhez és azokkal egységes elvek szerint tárgyalhatok. A fém-karbonilok továbbá fontos kiindulási anyagok a fémorganikus szintézisekben és meghatározó szerephez jutnak az átmenetifém- katalizált reakciókban.
A fémorganikus kémia kezdetei a XVIII. századra nyúlnak vissza. A történeti visszatekintések egyetértenek abban, hogy az első szerves fémvegyületet 1760-ban Cadet állította elő Párizsban egy katonai gyógyszertárban. Ez a vegyület bisz(dimetil-arzén(III))-oxid vagy hétköznapi nevén kakodil-oxid volt, és ahogy az olyan sokszor előfordult a tudomány történetében, nem szerves fémvegyület előállítása volt a cél.
Megjegyzés: Az első szerves fémvegyület: (CH3)2As-O-As(CH3)2 – Cadet, 1760.
Ezt követően számos tudományos eredményről számol be a szakirodalom, amelyekből egy válogatást adunk közre, természetesen a teljesség igénye nélkül.
Megjegyzés: Az első átmenetifém π-komplex: K(Pt(C2H4)Cl3) x H2O – Zeise, 1827.
Az első alkénkomplex előállítása Zeise dán kémikus nevéhez fűződik, aki a róla elnevezett „Zeise-só”-t, K[Pt(C2H4)Cl3] x H2O, 1827-ben állította elő. Zeise PtCl4 és PtCl2 keverékét forralta etil-alkoholban, amelyből KCl-oldat hozzáadása után sárga, tűszerű kristályok váltak ki [1]. A termékről Zeise helyesen azt állította, hogy eténcsoportot tartalmaz és meggyőződését még olyan tekintélyes tudósokkal szemben is fenntartotta, mint Liebig.
A néhány évtizeddel későbbi vizsgálatok őt igazolták, de arra több, mint 140 évet kellett várni, hogy a vegyület szerkezetét meghatározzák, és az etén-Pt között kialakuló kötést értelmezzék.
Megjegyzés: Az első σ-kötésű szerves átmenetifém-vegyület: (C2H5)2Zn – Frankland, 1849.
KITEKINTÉS
Az első szerves fémvegyület előállítása
Cadet eredeti szándéka szerint „láthatatlan” tintát szeretett volna előállítani kobalttartalmú ásványokból. Az arzén(III)-oxid-tartalmú ásvány kálium-acetátos feltárása során azonban Cadet azt tapasztalta, hogy a reakcióelegyből egy rendkívül kellemetlen szagú folyadék desztillál át.
Ezt a „Cadet-féle folyadék”-nak nevezett anyagot később Bunsen igen alaposan tanulmányozta és megállapította, hogy az egy oxigéntartalmú vegyület, amely egy különleges szerves „gyököt” tartalmaz. A vegyületet Berzelius kakodil-oxidnak, az összetett gyököt kakodil-nak nevezte el. Az elnevezés a vegyület kellemetlen szagára utal és a görög „κακωδης” szóból származik, amely „bűzös”-t jelent.
A rendkívül bűzös és mérgező kakodil-oxid az alábbi reakcióegyenlet szerint képződik:
(I.1). ábra -
Frankland, angol vegyész Bunsen laboratóriumában, Marburgban dolgozott az 1840-es években. Nevéhez több fémorganikus vegyület szintézise kapcsolódik, így ő állított elő elsőként dietil-cinket. Eredeti célját tekintve az „etilgyök” előállítását tervezte etil-jodid és fémcink közvetlen reakciójával, amelynek eredményeként cinkorganikus vegyületekhez jutott az alábbi reakcióegyenlet szerint:
((I.2). egyenlet)
A dietil-cink levegőre érzékeny, piroforos folyadék. Előállítása az (I.2.) egyenlet szerint azáltal vált lehetővé, hogy Frankland védőgázként H2- atmoszférát használt és ezáltal az inert atmoszférában történő szintézisek megalapozójának tekinthető.
Megjegyzés: A mai szintetikus kémikus szemével nézve Frankland teljesítménye egyedülálló, hiszen egy igen könnyű, gyúlékony és robbanásveszélyes gázt használt védőgázként. A helyzetet tovább bonyolítja, hogy ilyen körülmények között hidrid(H–) és dihidro-gén(H2) komplexek is képződhetnek. Napjainkban elsősorban nitrogénnel vagy argonnal biztosítják az inert atmoszférát.
Megjegyzés: Az első biner fém-karbonil: Ni(CO)4 – Mond, 1890.
Az első biner fém-karbonil és a hozzá kapcsolódó ipari eljárás szellemi atyja Ludwig Mond német származású, Angliában tevékenykedő kémikus volt.
Mond 1890-ben számolt be a nikkel-tetrakarbonil, Ni(CO)4, előállításáról, amely nikkel és atmoszferikus nyomású CO-gáz közvetlen reakciójában képződik 50 °C körüli hőmérsékleten [2]. Ennek az illékony folyadéknak a gőzei 230 °C-on elbomlanak és igen tiszta fémnikkelt eredményeznek:
((I.3). egyenlet)
A nikkel tisztítására alkalmazott Mond-féle eljárás az (I.3.) reakción alapul.
Megjegyzés: A tudományterület első Nobel-díjas tudósa: Grignard, 1912.
Az 1912. év hozta a fémorganikus kémia első nagy tudományos elismerését, amikor Victor Grignard megosztott Nobel-díjban részesült az alkil- magnézium- vegyületek területén végzett kutatásaiért. A róla elnevezett Grignard-reagens, szerves magnézium-halogenid (RMgX) igen hatékony reaktánsnak bizonyult a kémiai szintézisekben és alapvető szerepet játszott a szerves kémia fejlődésében [3].
Napjaink egyik legnagyobb volumenben gyártott fémorganikus vegyületcsaládja a szilikonok, amelyek sziloxán kötést tartalmazó szilíciumorganikus polimerek. Ipari gyártásukat Rochow és Müller alapozták meg 1943-ban, amikor kidolgozták a metil-klór-szilánok közvetlen szintézisét. Az eljárás lényege az, hogy ferroszilícium fölött metil-klorid-gázt vezetnek 300 °C-on, rézkatalizátor jelenlétében, miközben metil-klór-szilánok keletkeznek:
((I.4). egyenlet)
A mono-, di- és trifunkciós klór-szilánok (x = 1, 2 vagy 3) hidrolízisével lineáris és térhálós sziloxánpolimerek nagy változatosságban állíthatók elő.
Megjegyzés: Az első „szendvics” vegyület: (C5H5)2Fe – Kealy és Pauson, 1951.
A fémorganikus kémia fejlődése az 1950-es évekig meglehetősen lassú és néhány alkalmazástól eltekintve a fém-szén kötés tanulmányozása nem került a tudományos érdeklődés középpontjába. Ezt a helyzetet alapvetően megváltoztatta az első „szendvics” vegyület, a ferrocén, (C5H5)2Fe előállítása, amelyet 1951-ben Kealy és Pauson állítottak elő [4]. A ferrocénben a vasatomot a két ciklopentadienilgyűrű, C5H5 „szendvicsszerűen”
fogja közre (I.1. ábra).
I.1. ábra - A ferrocén szerkezete
A vegyület – az ismeretek akkori szintjén – mind a térszerkezet, mind a kötéselmélet szempontjából teljesen újszerű volt, és ez a tény friss lendületet adott a szerves fémvegyületek kutatásának. Ezt az eseményt gyakran a modem fémorganikus kémia kezdetének is tekintik. Megindulnak a szisztematikus kutatások, és ennek eredményeképp megjelennek a szerves átmenetifém-katalizátorok, amelyek forradalmasítják a vegyipart. Ziegler és Natta 1955-ben kidolgozzák az etén és propén kisnyomású polimerizációját, amely átmenetifém-halogenid/ alkil-alumínium vegyes katalizátoron alapul. Ezt a tudományos felfedezést 1963-ban Nobel-díjjal ismerik el, mint ahogy Fischerrel megosztva ebben a rangos kitüntetésben részesül 1973-ban Wilkinson is, akinek a nevét leginkább az alkének homogén fázisú hidrogénezésével és a róla elnevezett komplexszel, a Rh(PPh3)3Cl- dal kapcsolják össze. E. O. Fischer, a München-i egyetem nagytekintélyű professzora, a fémorganikus kémia számos területén nyújtott kimagasló teljesítményt. Nevéhez fűződik az első átmenetifém-karbén (1964) és átmenetifém-karbin (1973), azaz fém-szén kettős kötésű és fém-szén hármas kötésű komplexek előállítása. A tudományterület további Nobel-díjasai: W.N. Lipscomb (1976) a boránok szerkezet- és kötésviszonyaira vonatkozó kutatásaiért; H.C. Brown és G. Wittig (1979) a szerves bór- és foszforvegyületek szerves szintézisekben való alkalmazásáért; valamint R. Hoffmann és K. Fukui (1981) az izolobalitás elvének megalkotásáért, amelynek segítségével szervetlen, szerves és fémorganikus molekulák szerkezete és reaktivitása egységesen tárgyalható.
Ezek már a közelmúlt eseményei, amelyek elvezetnek napjaink kutatásaihoz. Ezeknek a kutatásoknak az az egyik meghatározó vonása, hogy a hangsúly egyre inkább a specifikus hatású és tulajdonságú anyagok előállítására helyeződik.
Az előzőek alapján érzékelhető, hogy a szerves fémvegyületek kémiája az 1950-es évektől kezdődően fejlődött a kémia önálló tudományterületévé.
Ez jól nyomon követhető az akkori időszak kémia-tankönyveiben. A szerves fémvegyületek először a szervetlen és szerves kémiai tankönyvek egy- egy alfejezetében vagy „apróbetűs” részében fordulnak elő (lásd pl. [5,6]), később már teljes főfejezetet alkotnak [7], végül nagy számban megjelennek azok a szakkönyvek, amelyek teljes terjedelmükben fémorganikus problémakörrel foglalkoznak.
Napjainkban a fémorganikus kémia a tudományterület egyik legdinamikusabban fejlődő ága; számos nemzetközi folyóirat, tudományos konferencia, hazai és nemzetközi tudományos munkacsoport szerveződött és szerveződik e problémakör köré. Sőt, annak is tanúi lehetünk, hogy a fémorganikus kémiából is újabb és újabb önálló tudományágak nőnek ki, mint pl. a fémorganikus katalízis, a fémorganikus reagensek alkalmazása szerves kémiai szintézisekben vagy a gázfázisú fémorganikus ionkémia.
KITEKINTÉS
Fémorganikus vegyészek az évezred 100 leghíresebb kémikusa között
Az Európai Kémikusegyesületek Szövetsége (Federation of European Chemical Societies, FECS) az ezredforduló alkalmából felmérést végzett arról, hogy az európai szakvélemény szerint kik sorolhatók az elmúlt évezred 100 leghíresebb kémikusa közé [8]. Az előkelő névsor a tagegyesületek véleményének összesítése alapján készült és olyan neveket tartalmaz mint Lavoisier, Lomonoszov és Ruprecht Antal a 18.
századból; Arrhenius, Avogadro, Davy, Gay-Lussac és Pasteur a 19. századból, valamint Brönsted, Hevesy, Rutherford, Sabatier és Zsigmondy a 20. századból. Ebben a rangos „tudósklub”-ban a fémorganikus kémiát a következő nevek fémjelzik: Bunsen, Frankland, Grignard, Natta, Wilkinson és Ziegler.
Irodalmi hivatkozások
Író (Szerző) Szerkesztő Kiadásdátuma Mű címe Kiadás
helye Kiadó Oldalszám
1. W.C. Zeise 1831. Annalen der
Physik und Chemie
21, 497
2. L. Mond, 1890. J. Chem. Soc. 57, 749
3. V. Grignard 1900. Comp. Rend. 130, 1322
4. T.J. Kealy,
P.L. Pauson 1951. Nature 168, 1039
5. B. Lengyel, J. Proszt, P.
Szarvas
1959. A szilikonok in Általános és Szervetlen Kémia
Tankönyvkiadó 532- 533
6. Gy.
Bruckner 1980. Phosphor- és
arsenvegyületek in Szerves
Tankönyvkiadó 443-448