A gastrooesophagealis refluxbetegség
kialakulásának és kezelésének kockázati tényezői
Doktori értekezés
Dr. Pregun István
Semmelweis Egyetem
Klinikai Orvostudományok Doktori Iskola
Konzulens: Dr. Herszényi László, DSc., egyetemi docens
Hivatalos bírálók: Dr. Korponay-Szabó Ilma, DSc., egyetemi tanár Dr. Dezsőfi Antal, PhD., egyetemi adjunktus Szigorlati bizottság elnöke: Dr. Szalay Ferenc, DSc., egyetemi tanár Szigorlati bizottság tagjai: Dr. Székely György, PhD., főorvos
Dr. Abonyi Margit, PhD., egyetemi docens Budapest
2015
2
Tartalomjegyzék
Rövidítések jegyzéke
………...41. Bevezetés
………...61.1 A GERD meghatározása és osztályozása………....6
1.2. A GERD epidemiológiája……….9
1.3 A GERD kóreredete, kockázati tényezői és tünetei…………...………...10
1.3.1. A GERD kóreredete ………..10
1.3.2. A GERD kockázati tényezői………..15
1.3.3. A GERD tünetei……….25
1.4. A GERD diagnózisa………28
1.5. A GERD szövődményei………..31
1.5.1. Nyelőcsőfekély………..31
1.5.2. Nyelőcső strictura………..31
1.5.3. Barrett oesophagus………32
1.6. A GERD kezelése………34
1.6.1. Étrend- és életmódváltoztatás………34
1.6.2. Gyógyszeres kezelés………..34
1.6.3. Refrakter GERD..………..37
1.6.4. Sebészi kezelés....………..37
1.7. A chromogranin A (CgA) jelentősége………...39
1.7.1. A CgA biológiai hatása………..39
1.7.2. A CgA klinikai jelentősége………40
1.7.3. A CgA és a gyomorsav-elválasztás összefüggése……….41
2. Célkitűzés
………....443. Módszerek
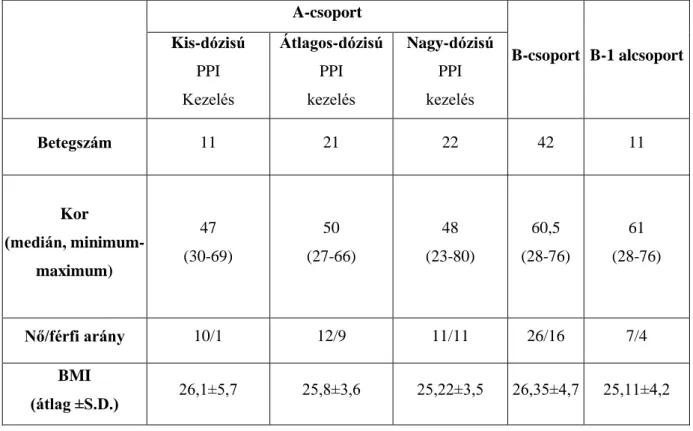
……….………..453.1. Résztvevők és módszerek….………...……….45
3.2. Kérdőív...………..48
3.3. Statisztikai elemzés…...………49
3
4. Eredmények
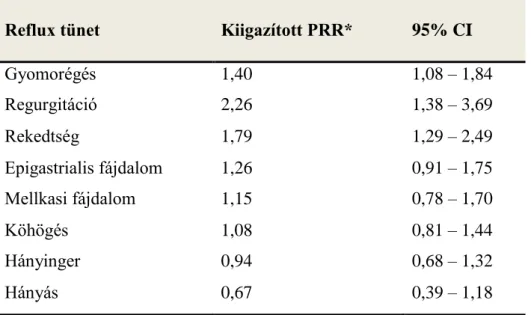
………...514.1. GERD tünetek gyakorisága………..51
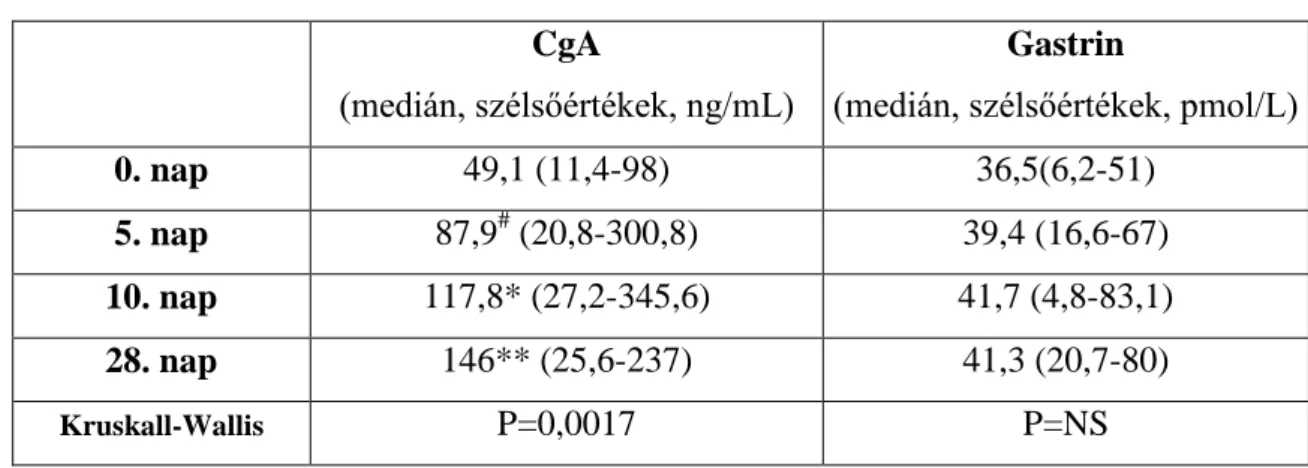
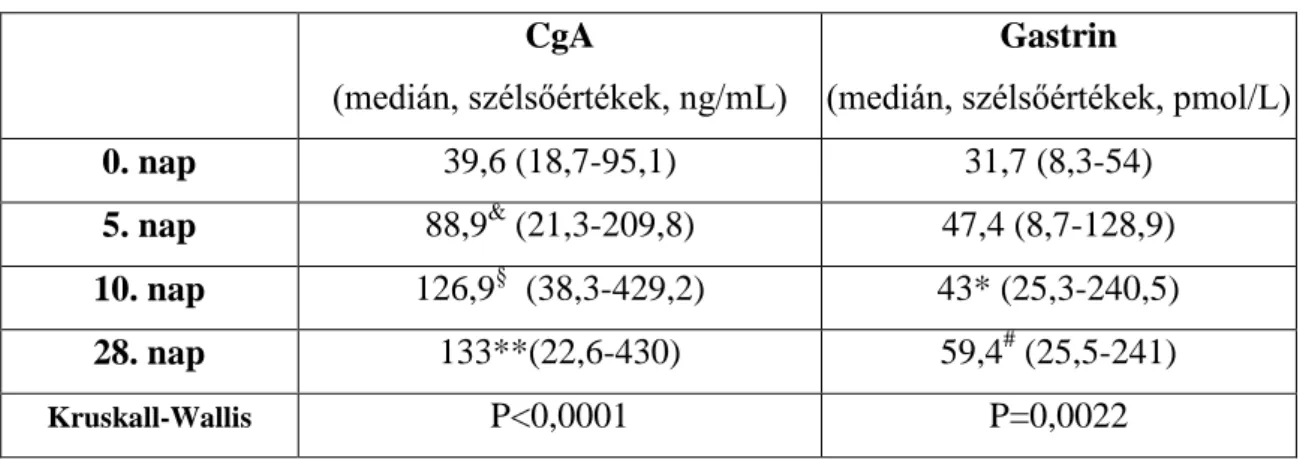
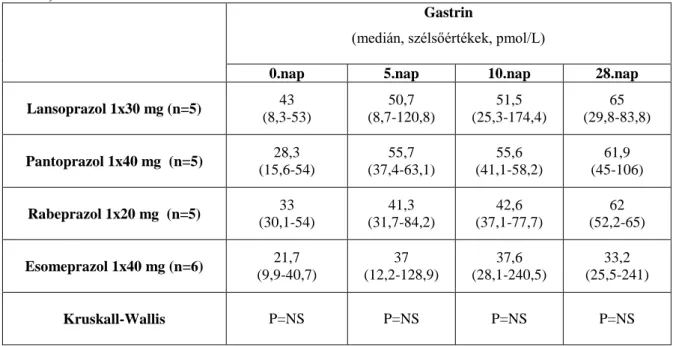
4.2. PPI szerek hatása a CgA és gastrin szintre………...………57
5. Megbeszélés
………656. Következtetések
………....807. Összefoglalás
………...…...818. Summary
……….829. Irodalomjegyzék
………...…8310. Saját közlemények jegyzéke
…………..………...………10911. Köszönetnyilvánítás
………1114
Rövidítések jegyzéke
BE – Barrett-oesophagus
BMI – Body Mass Index (testtömeg index) CCK-B – Cholecystokinin B
CI - Confidence interval (konfidencia-intervallum) CgA – Chromogranin A
ECL-cell – Enterochromaffin-like cell (enterochromaffinszerű sejt) ERD – Erosiv gastroesophageal reflux disease
(erozív refluxbetegség) GEJ - Gastrooesophagealis junkció
GERD – Gastroesophageal reflux disease (gastrooesophagealis refluxbetegség) H+/K+-ATP-áz – H+/K+ adenozin-trifoszfatáz
5-HIAA - 5-hydroxi-indolecetsav
H2RA – Histamin-2 receptor antagonista H. pylori – Helicobacter pylori
IGP – Intragastric pressure (intragastricus nyomás) IL-1ß – Interleukin-1 beta
LES – Lower esophageal sphincter (alsó oesophagus sphincter)
LES-BP – LES barrier pressure (alsó oesophagus sphincter barrier nyomás) MEN-I – Multiple endocrine neoplasia type I.
MEN-II - Multiple endocrine neoplasia type II.
MUSE- M-metaplasia U-ulceration S-stricturing E-erosions NERD – Non-erosive gastroesophageal reflux disease
(nem erozív refluxbetegség)
NCCP - Non-cardiac chest pain (nem szív-eredetű mellkasi fájdalom) NSE – Neuronspecifikus enolase
OR – Odds Ratio (esélyarány)
PPI – Proton-pump inhibitor (protonpumpa gátló) PRR - Prevalence rate ratio (prevalencia arány) PSA – Prostataspecifikus antigén
PTH - Parathormon
5
TLESR – Transient lower esophageal sphincter relaxation (tranziens alsó oesophagus sphincter relaxáció) TNFα – Tumornecrosis factor alfa
VIP- Vasoactive intestinal polypeptide
6
1. Bevezetés
A gastrooesophageális refluxbetegség (GERD) világszerte gyakori emésztőrendszeri betegség. Tünetei révén az életminőség jelentős rosszabbodásához vezethet, e mellett szövődmények kialakulásával is számolnunk kell.
1.1. A GERD meghatározása és osztályozása
A GERD pontos definíciója és korábbi osztályozása elsősorban morfológiai alapú volt, az endoszkópos vizsgálat eredményén alapult. Napjainkban is igen elterjedt ez az osztályozás, amely a GERD betegeket három csoportba sorolja, elsősorban az endoszkópos vizsgálat során észlelt eltérések alapján:
1. NERD (nem erozív refluxbetegség) – nem azonosíthatók jellegzetes nyálkahártyaeltérések az endoszkópia során, azonban a klinikai tünetek GERD-re típusosak
2. ERD (erozív refluxbetegség) – endoszkópos vizsgálattal típusos nyelőcső nyálkahártyája eltérések figyelhetők meg
3. Szövődményes ERD - nyelőcső fekély, szűkület, Barret-oesophagus, vagy adenocarcinoma igazolható az endoszkópia során
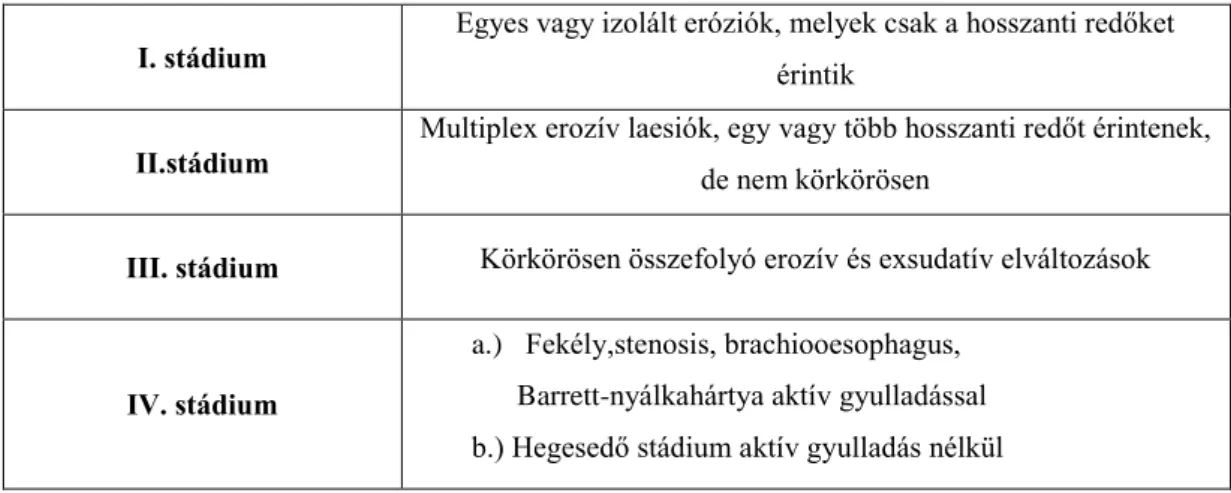
Az un. „Savary-Miller” féle osztályozás évtizedekig a morfológiai alapú osztályozás alapja volt (1.táblázat). A betegség súlyosságát a gyulladás mértéke, az oesophagitis kiterjedése határozza meg.
1. táblázat A Savary-Miller-féle osztályozás (1)
I. stádium
Egyes vagy izolált eróziók, melyek csak a hosszanti redőket érintik
II.stádium Multiplex erozív laesiók, egy vagy több hosszanti redőt érintenek, de nem körkörösen
III. stádium Körkörösen összefolyó erozív és exsudatív elváltozások
IV. stádium
a.) Fekély,stenosis, brachiooesophagus, Barrett-nyálkahártya aktív gyulladással b.) Hegesedő stádium aktív gyulladás nélkül
7
A „MUSE” (M-metaplasia, U-ulceration, S-stricturing, E-erosions) osztályozás az eróziók súlyosságának megítélésére a Savary-Miller beoosztást veszi alapul, azonban ettől függetlenül az esetleges fekélyek, stricturák vagy a metaplasia kiterjedésének értékelésére is lehetőséget ad (2). E két osztályozási rendszer mellett ismert több más is, amelyek a GERD különböző stádiumait (súlyossági fok) az eróziók kiterjedése alapján határozzák meg (Hetzel-1988, Tytgat-1990, Bytzer-1993) (1, 3).
A különböző osztályozási rendszerek használata azonban megnehezítette az egységes értékelést, többek között a különböző kezelési módok eredményességének összehasonlítását. Szükségessé vált a GERD különböző endoszkópos megjelenési formáinak egységes, egyszerű, nemzetközi, a mindennapi klinikai gyakorlatban jól alkalmazható osztályozása. A „Los Angeles” klasszifikáció a nyálkahártya- folytonosság megszakadása („mucosal break”) alapján különít el négy csoportot (A-D, 2.táblázat). Előnye, hogy egyszerű, könnyen reprodukálható, így a mindennapi gyakorlatban széles körben elterjedt (4). A GERD szövődményei azonban nem szerepelnek az osztályozásban.
2. táblázat A Los Angeles-i osztályozás
A. fokozat: a nyálkahártya folytonosságának megszakadása <5mm B. fokozat: a nyálkahártya folytonosságának a megszakadása
>5 mm, amely egy vagy több redőt érint
C. fokozat:
a nyálkahártya folytonosságának megszakadása a nyelőcső körfogatának kevesebb, mint 75%-át érinti és
több nyálkahártya redőt foglal magába
D. fokozat: a nyelőcső körfogatának 75%-át eléri, vagy meghaladja a folytonosság megszakadása
A fenti osztályozási rendszerek tehát elsősorban morfológiai alapúak voltak, alapjukat az endoszkópos eltérések jelentették. A legújabb, nemzetközi konszenzus- konferencia az irodalmi adatbázisok áttekintését követően a GERD új meghatározását és osztályozási rendszerét tette közzé (5). Állásfoglalása szerint („Montreal- meghatározás”), a GERD „mindazon kellemetlen panaszok és/vagy szövődmények összessége amely a gyomortartalom visszaáramlása következtében alakul ki”. Ez a
8
definícó jól jellemzi az új osztályozási rendszert: a korábbi, morfológiai alapú szemlélettel szemben betegközpontú, tünetorientált szemléletet tükröz (6). Az új osztályozás két nagy főcsoportot különít el:
oesophagealis szindróma
extraoesophagealis szindróma
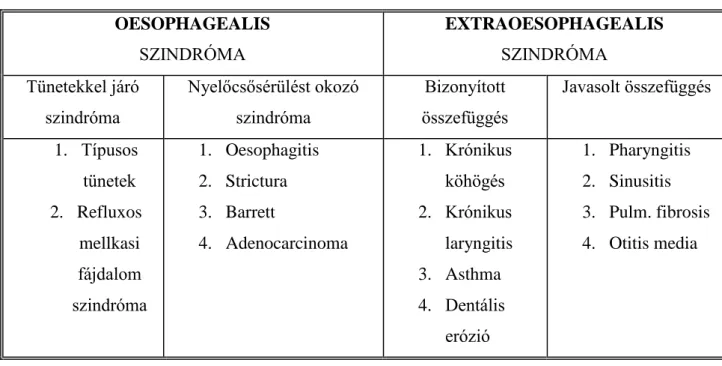
Az oesophagealis szindrómán belül tünetekkel járó és nyelőcsősérüléssel járó szindrómákról beszélhetünk. Az extraoesophagealis szindrómához azok a kórállapotok sorolhatóak, amelyek összefüggése a GERD-del bizonyított, azaz „egyértelmű”, vagy javasolt, azaz „lehetséges” (3.táblázat).
3. táblázat A Montreal-osztályozás (5,6) OESOPHAGEALIS
SZINDRÓMA
EXTRAOESOPHAGEALIS SZINDRÓMA
Tünetekkel járó szindróma
Nyelőcsősérülést okozó szindróma
Bizonyított összefüggés
Javasolt összefüggés
1. Típusos tünetek 2. Refluxos
mellkasi fájdalom szindróma
1. Oesophagitis 2. Strictura 3. Barrett
4. Adenocarcinoma
1. Krónikus köhögés 2. Krónikus
laryngitis 3. Asthma 4. Dentális
erózió
1. Pharyngitis 2. Sinusitis 3. Pulm. fibrosis 4. Otitis media
Az „extraoesophagealis szindróma” a Montreal-osztályozás szerint tehát külön főcsoportot jelent, hangsúlyozva a GERD változatos klinikai megjelenési formáit, egyúttal rendszerbe foglalja ezeket a kórképeket. E mellett az új osztályoszási rendszer előnye, hogy a GERD diagnózisának felállítását egyértelművé teszi, egyszerüsíti a GERD osztályozását a mindennapi gyakorlatban (6).
9
1.2. A GERD epidemiológiája
A GERD napjainkra népbetegséggé vált. Számos, különböző vizsgálómódszert alkalmazó tanulmány készült a GERD prevalenciájának felmérésére. A gyakoriság világszerte változatos, s az adatok alapján a fejlett, nyugat európai társadalmakban 8- 25% között van (7, 8); a kórkép Észak-Amerikában a leggyakoribb, a prevalencia itt 18- 27% közötti értékre tehető (8, 9, 10). El-Serag és munkatársainak vizsgálatában nem mutatkozott különbség a GERD tüneteit tekintve a fehér vagy fekete népességet összehasonlítva, azonban az oesophagitis a fehér rasszon belül gyakrabban fordult elő (10).
Az európai vizsgálatok közül egy svédországi, 3000 beteget felölelő, kérdőíves tanulmányban a gyomorégés/regurgitáció a 6%-ban fordult elő naponta, 14%-ban hetente és 20%-ban kevesebb alkalommal, mint hetente a megelőző 3 hónapban (11).
Spanyolországban végzett, multicentrikus, kérdőíves felmérés szerint a prevalencia 15%-os volt, a testtömegindex bizonyult az egyetlen független kockázati tényezőnek (12). Zagari és munkatársai több mint 1000 betegen végzett olaszországi vizsgálata szerint (kérdőív és endoszkópos vizsgálat) a refluxos tünetek gyakorisága 44.3% volt, 23,7%-uk legalább heti két alkalommal jelzett panaszt. Az oesophagitis gyakorisága 11.8%-os volt; a spanyolországi vizsgálattal szemben azonban a szerzők, nem találtak összefüggést a testtömegindex és a refluxos tünetek/oesophagitis között (13). Egy németországi, közel 9000, 50 évesnél idősebb beteg részvételével zajló vizsgálat adatai szerint a gyomorégés 23,7%-ban fordult elő a megelőző 4 hétben (14). Egy másik, Belgiumban végzett kérdőíves vizsgálat során a megkérdezettek 28%-a panaszolt gyomorégést az elmúlt egy évben, 42%-ban a panasz hetente legalább egy alkalommal fordult elő. A gyomorégést panaszolók 77%-a olyan súlyosnak ítélte a tünetet, amely mindennapi tevékenységükre is negatív hatással volt (15).
A GERD prevalenciája Ázsiában alacsonyabb, mint Nyugat-Európában vagy Észak-Amerikában, azonban az újabb epidemiológiai vizsgálatok alapján úgy tűnik, a GERD itt is gyakoribbá vált (8, 9). Kínában végzett, nagy betegszámú (16078) vizsgálat (GERD tünetek értékelése kérdőív segítségével a Montreal-meghatározás alapján) eredménye szerint a prevalencia 3,1%-os volt (16). Az ázsiai vizsgálatok és ezek
10
szisztematikus elemzése alapján a legalacsonyabb a prevalencia Kelet-Ázsiában (2,5- 9,4%), magasabb Közép-Ázsiában (7,6-19,4%) és Nyugat-Ázsiában (12,5-27,6%) (8, 9, 16-21).
Kevesebb az adat Dél-Amerikából; egy argentin vizsgálat szerint a prevalencia 11,9% (22). Ausztráliában végzett kérdőíves vizsgálat eredménye szerint (gyomorégés/regurgitáció legalább heti egy alkalommal) a prevalencia 12%-osnak adódott (23).
1.3. A GERD kóreredete, kockázati tényezői és tünetei
1.3.1. A GERD kóreredete
A motilitás, LES, TLESR szerepe .
A GERD kóreredete összetett, kialakulásának alapja azonban a nyelőcső kóros motilitása. A nyelés élettani folyamata során perisztaltikus hullám halad végig a nyelőcsövön, amely biztosítja a falat továbbhaladását. A nyelőcső alsó záróizma (lower esophageal sphincter-LES) a perisztaltikus hullám következtében elernyed, így a falat a gyomorba jut. A nyelőcső motilitását, a LES működését elsősorban a vegetatív idegrendszer szabályozza, azonban a folyamat összetett: emésztőrendszeri hormonok, ételek, gyógyszerek egyaránt hatnak a működésre (24). A nyelőcső ép motilitása, a kiegyensúlyozott LES-működés, a folyamatok finom koordinációja alapvető az élettani működéshez. Ismereteink szerint a GERD kóreredetének alapja a motilitászavar, az összehangolt működés zavara, amely tünetek, szövődmények kialakulásához vezethet.
Élettani körülmények között a LES nyugalmi nyomása révén megakadályozza a gyomortartalom visszaáramlását a nyelőcsőbe. Tartós nyomáscsökkenés révén azonban a reflux kockázata fokozott (24). A LES simaizomrostjai paraszimpatikus beidegzés révén mind serkentő, mind gátló szabályozás alatt állnak. Intrinsic myogén tónus biztosítja a LES nyugalmi nyomását. A gátlón rostok aktiválódásának eredményeként a LES tónusa csökken. A serkentő idegek neurotranszmitterei például az acetylkolin vagy a „substance P”, míg a gátlóké a VIP és a nitrogén-monoxid (NO). A LES működését a
11
cruralis diaphragma harántcsíkolt izomrostjai segítik, melyek mint külső sphincter veszik körül a simaizomrostokat („külső LES”) (25).
A LES tartós nyomáscsökkenése növeli a reflux kockázatát. Ez kialakulhat többek között sclerodermában, különböző myopathiák részjelenségeként, gyógyszerek hatására (aminophyllin, nitrát, calcium-antagonisták, foszfodieszterázgátlók), sebészeti beavatkozás kapcsán, de a reflux eredményeként kialakuló oesophagitis is károsítja a LES működést, tovább súlyosbítva a tüneteket. Számos esetben azonban nem derül fény a tartós LES-nyomáscsökkenés okára (25).
A fenti kórfolyamat mellett azonban úgy tűnik egy másik reflexmechanizmus nagyobb jelentőségű a refluxbetegség kóreredetében, ez pedig a „transient lower oesophageal sphincter relaxation” (átmeneti alsó oesophagus sphincter relaxáció, TLESR). Ezen vagus-reflex triggere a gyomor feszülése, melynek eredményeként a spincter ellazul (25). Egészségesekben is előfordul ez a nyeléstől független, spontán relaxáció, azonban a GERD-betegekben a reflux-epizódok jelentős részében játszhat oki szerepet (1). A TLESR mellett fontos tényező a kóreredetben a megnövekedett gyomorvolumen (postprandiálisan, pylorus elzáródás, gyomorürülési zavar esetén) és a növekedett intraabdominalis nyomás (elhízás, terhesség, ascites) (25). Hiatushernia esetén a LES a mellkasba kerül, s a negativ mellűri nyomás kedvez a reflux kialakulásának (1).
A refluxatum, savas reflux
Az egészséges nyelőcső perisztaltikus hulláma révén szinte teljesen kiüríti a refluxatumot („volumen-clearence”). Károsodott perisztaltika esetén viszont - amely a GERD kóreredetének alapja – megnyúlik a nyelőcsőtranzit, így a regurgitált gyomortartalom károsítja a nyelőcső-nyálkahártyát. A károsodás mértéke függ a regurgitált bennék mennyiségétől, összetételétől az epizódok gyakoriságától (24, 25).
Több vizsgálatban próbálták mind direkt, mind indirekt módszerekkel értékelni önmagában a refluxatum térfogatának szerepét a GERD kóreredetében, a tünetképzésben, azonban a technikai nehézségek miatt az eredmények korlátozottak (26). Egy vizsgálatban ultrahangos módszerrel értékelték a nyelőcső-feszülését (közvetett módon a reflux-térfogatot) GERD-betegekben kontroll egyénekhez
12
viszonyítva. Eredményeik szerint a feszülés kifejezettebb volt GERD betegekben, azonban a gyomorégéssel nem mutatatkozott összefüggés (27).
A refluxatum gyomornedvet (sósav, pepszin), duodenumnedvet (epesavak, pancreasnedv) és levegőt tartalmaz. A refluxatum összetétele több tényezőtöl függ: a sav mennyiségét a savtermelésen túl többek között a gyomor-perisztaltika, a gyomortartalom postprandiális összekeveredése, savcsökkentő kezelés befolyásolják. A refluxatum duodenumtartalma növekedhet pl. lassult vékonybélmotilitás esetén (26).
A gyomorsav károsítja a nyelőcsőnyálkahártyát: egy vizsgálatban 25 súlyos, szövődményes GERD beteg (strictura, Barrett nyelőcső, nyelőcsőfekély) manometriás és pH-metriás vizsgálatának eredményét vetették össze szövődménymentes GERD betegekével. A pH<4 időszak a lényegességi szintet meghaladóan hosszabb volt a szövődményes esetekben, a különbség az éjszakai órákban volt még kifejezettebb (28).
Menges és munkatársai GERD betegek két csoportját (oesphagitis és Barrett oesophagus) hasonlították össze. 24 órás pH monitorozás során a savas reflux kifejezettebb volt a Barrett csoportban, összevetve a szövődménymentes oesophagitises betegekkel (29). Nem csak a kifejezett savas reflux, hanem a gyenge savas reflux is okozhat azonban GERD-tüneteket. NERD betegek 50%-ban ugyanis nem nő a kifejezett savas (pH<4) epizódok gyakorisága, ennek ellenére a betegek egy része jól reagál hatékony savszekréciógátló kezelésre, amely a gyenge savas reflux jelentőségére irányítja a figyelmet (26). A sav kóroki szerepének közvetett bizonyítéka a GERD (különösen ERD) kezelésében alkalmazott savszekréciógátlók hatékonysága is.
A savas reflux-szal összefüggésben, az utóbbi években az un. „savas zseb”
jelentősége a figyelem előterébe került. Éhomi állapotban a gyomor pH értéke 1,5-3,5 között van, azonban étkezéseket követően a gyomor nagy részében az étel pufferoló hatása révén 4 felé emelkedhet (26). A reflux epizódok többsége jellemzően postprandialisan jelentkezik, így feltételezhetően ilyenkor kevésbé savas gyomortartalom áramlik vissza a nyelőcsőbe. Fletcher és munkatársainak tanulmánya során 40 beteg kettős (gyomor és nyelőcső) pH vizsgálatát végezték el. Eredményeik szerint a nyelőcső-refluxatum kémhatása sokkal savasabb volt, mint a gyomor corpusé, étkezést követően. Éhomi állapotban azonban nem mutatkozott különbség. A gastrooesophagealis junkció (GEJ) közelében azonosított „savas zseb” területén az étel puffer hatása nem érvényesül, kifejezetten savas kémhatású (median pH 1,6), szemben a
13
corpuséval (pH 4,7, P<0,001) (30). Feltételezhető, hogy a savas zseb egy puffermentes resrvoir-t képez és megteremti a savas reflux lehetőségét. Fontos a savas zseb lokalizációja: igazolták, hogy amennyiben a savas zseb a rekeszizom felett helyezkedik el, vagy eléri a hiatus hernia nyílását, a TLESR epizódok 70-85%-ában egyúttal savas reflux is jelentkezik. Ha azonban a rekeszizom alatt található, akkor a refluxepizódok aránya kevesebb, mint 20% . Fontos, hogy a jelenséget nem csak GERD betegekben, de egészséges önkéntesekben is megfigyelték (31, 32). Következésképpen, minden olyan tényező, amelynek során a savas zseb rekeszizomhoz viszonyított helyzete megváltozik, hatással van a reflux kockázatára. Az egyik ilyen legfontosabb anatómiai tényező a hiatus hernia – ezekben a betegekben a savas zseb gyakrabban volt a rekesz felett megtalálható, mint a kontroll csoportban (76% vs. 22%) (31, 32).
A pepszin proteolitikus enzim, mely vélhetően szintén szerepet játszik a nyálkahártyalaesio kialakításában: savas reflux kedvez az enzim aktiválódásának, mely pH 2-3 között kifejezett (26).
Duodenogastro-oesophagealis (alkáliás) reflux
Kevésbé egyértelmű a refluxatum duodenumnedv-tartalmának jelentősége a GERD kórfolyamatában. Összevetve a savas reflux-szal, egyes vizsgálati adatok szerint a tünetképzésben kisebb a jelentősége (26, 33, 34). Nem teljesen tisztázott a nyálkahártyakárosodásban, a típusos refluxos leasiók kialakításában játszott szerepe sem. Felmerült, hogy a Barrett oesophagus önálló oki tényezője lehet, azonban ennek alátámasztására nincs elég adat (26).
A nyelőcső védekező funkciója
A nyelőcső védekező szerepét jól példázza a Bernstein-teszt során végzett megfigyelés, amely szerint a folyamatosan, akár 30 percen át adagolt pH 1-es sósavoldat sem okoz gyomorégést egészséges egyénekben (35).
A nyelőcsőnyálkahártya védelmének fontos anatómiai, strukturalis eleme a nyelőcső többrétegű epitheliuma. A sejtek közötti „tight junction” a védekezés fontos eleme. Ennek ellenére a refluxatum H+ ionjai képesek az epithelsejtek cytoplazmájába
14
vagy az intercellularis térbe diffundálni. Fehérjék, foszfát és a bikarbonát a puffermechanizmus résztvevői az intracellularis pH fenntartása érdekében, amelyek közül a bikarbonát a legfontosabb. A vérből az extracellularis térbe diffundálva transzportfolyamat eredményeként kerül a cytoplazmába. E mellett de novo is képződik bikarbonát intracellularisan enzimatikus folyamat eredményeként (35).
A sav elleni védelem másik fontos eleme a sejtmembrán ion-transzporterei: több ioncserélő (Na+-H+, Cl--HCO3) transzporter védi a sejtet a felesleges H+ ionoktól (1, 35). A nyelőcső megfelelő vérellátása, mely az áramlás növelése révén alkalmazkodik agresszív noxa esetén, a védelmi rendszer alapja (1, 24, 35). Korábban a nyelőcsőnyálkahártya-védelem fontos elemének tartották a megfelelő testhelyzetet (pl.
az étekezéseket követő gyors lefekvés elősegítheti a refluxot), hangsúlyozva a gravitáció jelentőségét. Az újabb adatok alapján azonban úgy tűnik, hogy ennek kisebb a klinikai jelentősége (26).
A Helicobacter pylori lehetséges szerepe
A Helicobacter pylori különböző, nem csak emésztőrendszeri betegségekben játszott lehetséges kóroki szerepe felfedezése óta a tudományos érdeklődés előterében áll. Az eddigi adatok alapján azonban ellentmondásos a baktérium szerepe a GERD kóreredetében. A H.pylori incidenciája irodalmi adatok szerint 30-90% közötti (többségükben 35%) GERD betegekben, a változatos értékek elsősorban a különböző földrajzi régiók eltérő fertőzöttségéből adódhatnak (36, 37). Feltételezések szerint a Helicobacter pylori az antrum-gastritis, következményes növekedett savelválasztás és a fertőzés eredményeként termelődő NO, citokinek és prosztaglandinok okozta LES nyomás csökkenés révén járul hozzá a GERD kialakulásához (37). A fejlett nyugati társadalmakban azonban a H.pylori prevalenciája csökken, míg a GERD és szövődményeinek aránya nő – mindezek alapján a baktérium GERD-del szembeni
„védő” szerepe is felmerült. Ezt a feltételezést támogatták egyes adatok, amelyek szerint nyombélfekélyben szenvedő H.pylori pozitív betegek eradikációs kezelését követően a GERD gyakorisága nőtt (38).
Grande és munkatársai (37) 184 GERD betegnél végeztek endoszkópos vizsgálatot biopsziával és pH-manometriát. A betegek 46%-a volt H.pylori pozitív, 54%
15
negatív. Eredményeik szerint nem volt összefüggés a reflux-epizódok gyakorisága a LES nyomás, a GERD súlyossága és a Helicobacter status között. Következtetéseik összhangban vannak egy más vizsgálatokkal, ahol szintén nem igazolódott összefüggés a H.pylori fertőzés és GERD között (39, 40). Összefoglalva megállapítható, hogy a jelenlegi adatok alapján nem bizonyítható egyértelmű összefüggés a GERD kialakulása- súlyossága és a H.pylori fertőzés között.
1.3.2. A GERD kockázati tényezői
Több (genetikai és környezeti) tényező merült fel, mint a GERD kialakulásának kockázati tényezője. Ezen tényezők lehetséges oki szerepével kapcsolatban az utóbbi években több vizsgálat született.
1.3.2.1. Genetikai tényezők
A genetikai tényezők szerepére hívják fel a figyelmet azok a megfigyelések, amelyek szerint egyes családokban a GERD halmozottan fordul elő, és GERD betegek első fokú rokonai között szintén gyakoribb a betegség (41). Egy 4480 ikerpár kérdőíves vizsgálatában (ahol a GERD definíciója a gyomorégés/regurgitáció volt, legalább egy alkalommal egy héten az elmúlt egy év során) a monozigóta ikrekben a konkordancia arány nagyobb volt, mint a dizigóta ikrek között (42% vs. 26%, P<0,001) (42). A genetikai összefüggés egyértelműnek tűnik, azonban ennek pontosabb tisztázáshoz további vizsgálatok szükségesek.
1.3.2.2. Életkor és nem
A GERD típusosan középkorban jelentkezik; bár az irodalomban elfogadott, hogy az előfordulási gyakoriság nő az életkorral, ennek ellenére az ezzel kapcsolatos vizsgálatok eredménye ellentmondásos (43, 44, 45). A GERD prevalencia egyes adatok szerint a 70-éves kor előtt éri el a csúcsot, főleg férfiakban (46). A nem és GERD összefüggését elemző vizsgálatok nem igazoltak különbséget a nemek között, ismert azonban, hogy terhesség alatt a refluxos tünetek rosszabbodhatnak (43, 44, 47).
16 1.3.2.3. Gyomorürülési zavar
A lassult gyomorürülés a GERD ismert agresszív tényezője: a gyomor feszülése miatt fokozódik a savelválasztás és nő a TLESR frekvenciája (48). Egy vizsgálatban GERD betegek negyedében igazoltak lassult gyomorürülést (retenció legalább 4 órán át) (49). Bár a GERD betegek többségénél nincs kimutatható gyomorürülési zavar, az eltérés mint járulékos tényező szerepet játszhat a tünetek rosszabbodásában, így kockázati tényezőnek is tekinthető (45).
1.3.2.4. Hiatus hernia
Elfogadott, hogy hiatus hernia esetén a refluxepizódok száma nő. A tünet részben anatómiai okokkal magyarázható: élettani esetben a gastrooesophagealis junkció véd a reflux ellen. Amennyiben az intraabdominalis nyomás hirtelen nő, a cruralis rekeszizom mint „2. sphincter” játszik védő szerepet. Hiatus hernia esetén azonban a rekeszizom és gastrooesophagealis junkció távolabb kerül egymástól, így védő hatása megszűnik. Ezen túlmenően a nagy hiatus hernia a nyelőcső ürülését is károsítja, ezáltal romlik a sav-clearance (45, 50).
1.3.2.5. Gyógyszerek
A GERD kóreredetének ismeretében érthető bizonyos gyógyszerek refluxos tüneteket provokáló hatása (a LES nyomásának csökkentése, a gyomorsavelválasztás serkentése, a TLESR számának növelése). A teophyllin serkenti a gyomorsavelválasztást és csökkenti a LES nyomását. Hasonló hatást fejtenek ki a beta- adrenerg agonisták is. A sumatriptam gátolja az étekezéseket követő TLESR számának csökkenését, s ezáltal postprandialis refluxos tüneteket okozhat. A morphin épp ellenkezőleg, a TLESR számának csökkentése révén mérsékelheti a refluxos tüneteket.
A nitroglycerin, calcium-antagonisták és benzodiazepin származékok csökkentik a LES nyomását (45, 51, 52).
17 1.3.2.6. Obesitas
Az elhízás prevalenciája az elmúlt évtizedekben világszerte növekedett. Több vizsgálat szól a mellett, hogy az elhízás a GERD önálló, független kockázati tényezője, és a kockázat a BMI-vel arányosan nő (53, 54). Egy, az elhízás és GERD összefüggéseit elemző epidemiológiai vizsgálatok metaanalízise szerint (55) mind a túlsúlyosság (BMI 25-30 kg/m2), mind az elhízás (BMI >30 kg/m2) összefügg a GERD tüneteivel (OR:
1,43, 95% CI:1,158-1,774 és OR:1,94, 95% CI: 1,468-2,566); az erozív oesophagitis-sel (OR:1,76, 95% CI: 1,156-2,677 túlsúlyos betegekben) és a nyelőcső adnocarcinomával (OR: 1,52, 95% CI: 1,147-2,009 és OR:2,78, 95% CI: 1,850-4,164). Egy másik, 206 beteget felölelő vizsgálatban az elhízottak (BMI >30 kg/m2) között a savas reflux gyakrabban fordult elő 24 órás pH-metria során (P<0,005) (56). Bár az Egyesült Államokból származó adatok szerint egyértelműen pozitív a BMI és GERD közötti összefüggés, egyes európai adatok eredménye heterogén, amely az etnikai különbségek jelentőségére is felhívja a figyelmet (57, 58). A földrajzi különbségek oka összetett, egyik ok lehet, hogy a BMI és a test-zsírtartalom közti összefüggés változik a különböző etnikai csoportok között (59).
Számos lehetséges kórfolyamat merült fel, amely az obesitas és GERD összefüggését magyarázhatja. Ismert, hogy a zsigeri elhízás, amely haskörfogatnövekedésben nyilvánul meg elősegítheti a GERD kialakulását az intragastricus nyomás (intragastric pressure - IGP) emelése révén (60-62).
Manometriával végzett vizsgálat (60) igazolta, hogy az IGP mind belégzéskor, mind kilégzéskor szignifikánsan nagyobb volt elhízottakban, mint a normál testsúlyúakban.
Az IGP 0,3 Hgmm-rel nőtt egységnyi BMI növekedés esetén. Az eredményeket más vizsgálatban is megerősítették (61).
Egy másik lehetséges magyarázat az elhízott betegek csökkent/lassult sav- clearance-e. Normál testsúlyú és obes, egészséges és GERD betegek manometriával végzett case-control vizsgálata szerint a GERD betegek nyelőcső motilitása kóros volt, ezen túlmenően az elhízott betegek sav-clearance-e is csökkent (58, 63).
Obes betegekben azonban a GERD legfontosabb kóroki tényezője TLESR. A TLESR epizódok fő serkentője a gyomorfeszülés, amely ingerli a gyomor proximalis részén elhelyezkedő feszülési- és nyomásreceptorokat (64). Normál testsúlyú, túlsúlyos
18
és elhízott nem-GERD betegekben végzett vizsgálat során, ahol endoszkópiát, pH- metriát és manometriát végeztek, az elhízott betegekben a TLESR epizódok száma szignifikánsan több alkalommal fordult elő, mint a nem elhízottakban 2 órás postprandialis megfigyelési időszak során. E mellett a savas refluxepizódok aránya is nagyobb volt az elhízottakban. Közvetlen összefüggés igazolódott a növekedett BMI, a TLESR epizódok száma és a TLESR epizódokhoz kapcsolódó savas reflux között (65).
Az obesitas a zsigeri elhízás révén is részt vehet a GERD kialakításában. A zsigeri zsírszövet metabolikus aktivitást mutat, azaz a védő citokinek (pl. adiponectin) szintje csökken, míg a gyulladásos citokinek (pl. TNF-α - tumor-necrosis faktor alfa, interleukin-1β – IL-1β , interleukin-6 - IL-6) szintje nő. Egyes adatok szerint erozív oesophagitisben és Barrett-oesophagus esetén e gyulladásos citokinek aránya nő (58, 66, 67). Eddigi ismerteink alapján bizonyított, hogy az obesitas a GERD kockázati tényezője; a kórfolyamatban az abdominalis elhízás mellett mind mechanikus, mind metabolikus tényezőknek lehet szerepe. Több vizsgálat elemezte az elhízás és GERD tünetek (gyomorégés, savas regurgitáció) kapcsolatát, többségük megerősítette az összefüggést (4. táblázat).
19
4.táblázat Az elhízás és GERD tünetek kapcsolata /Festi (58) alapján/
Tanulmány Módszer Minta nagysága Pozitív összefüggés
Nilsson (47) Kérdőív 65363 Igen
Nandurkar (68) Validált kérdőív 211 Igen
Jacobson (54) Kérdőív 10545 Igen
Nocon (69) Interjú 7124 Igen
Corley (70) Kérdőív 80110 Igen
Nocon (71) Validált kérdőív 6215 Igen
Zheng (72) Kérdőív, telefonos interjú 27717 Igen
Andersen (73) Validált kérdőív 1321 Nem
Lagergren (74) Interjú 820 Nem
20
Az elhízás nem csak a GERD tünetekkel, hanem az oesophagitis-sel is összefügg, amelyet több endoszkópos vizsgálat eredménye is alátámaszt (5.táblázat).
5.táblázat Az elhízás és oesophagitis kapcsolata /Festi (58) alapján/
Tanulmány Módszer Minta nagysága Pozitív összefüggés
Ruhl (75) Felső panendoscopia 12349 Igen
Nocon (71) Felső panendoscopia 6215 Igen
Kim (76) Felső panendoscopia 27319 Igen
Kang (77) Felső panendoscopia 2457 Igen
Lee (78) Felső panendoscopia 3363 Igen
Chung (79) Felső panendoscopia 7078 Igen
Furukava (80) Felső panendoscopia 6010 Nem
Baldi (81) Felső panendoscopia 1542 Nem
A metabolikus szindróma és GERD összefüggésére világít rá egy tanulmány: az abdominalis elhízás és a szérum trigliceridszint a GERD független kockázati tényezőjének bizonyult, sőt CT vizsgálat alapján a zsigeri zsírszövet a GERD független kockázati tényezője (79). Vélhetően a gyulladásos mediátorok játszanak kiemelt szerepet a kórfolyamatban; a zsigeri zsírszövet fokozott lipolízishez és szabad zsírsav képződéshez, inzulinrezisztenciához vezet. Az inzulinrezisztencia a metabolikus szindróma kialakulásában kulcsszerepet játszik, a mediátoroknak a LES nyomás csökkentésében, vagy a nyelőcső savclearance megváltoztatásában lehet szerepük (58).
21
Az obesitas és GERD kapcsolatát erősítik azok a megfigyelések is, amelyek szerint a testúly csökkentése a GERD tünetek javulásához vezet (82), bár ezzel ellentétes eredményű vizsgálatot is közöltek (83). Az endoszkópos vagy sebészeti testsúlycsökkentő beavatkozások is kedvezően befolyásolhatják a GERD-et. A Roux- en-Y bypass e tekintetben igen előnyösnek tűnik (84).
1.3.2.7. Diétás tényezők
A diétás tényezők oki szerepe évtizedek óta az érdeklődés előterében áll; széles körben elterjedt bizonyos ételek-italok refluxt elősegítő, „refluxogén” hatása.
Figyelembe véve, hogy a GERD betegek tünetei gyakran étkezéseket követően jelentkeznek, joggal merül fel a diétás tényezők szerepe. Ennek ellenére, az ezzel kapcsolatos irodalmi adatok ellentmondásosak. Egyes vizsgálatok a LES nyomásának csökkenését, a savas reflux fokozódását írták le zsírgazdag étel, csokoládé fogyasztását követően (58, 85, 86). El-Serag kérdőíves (GERD tünetek, diétás jellemzők) és endoszkópos vizsgálatában pozitív összefüggés igazolódott a növekedett zsírfogyasztás és a GERD tünetek/ erozív oesophagitis között, míg a magas rosttartalmú étrend kedvezőnek bizonyult. Az elfogyasztott zsírok és a GERD tünetek/oesophagitis azonban nem volt független a BMI-től: lényegességi szintet meghaladó eltérés csak az elhízottakban igazolódott (87). Más vizsgálatok azonban a növekedett zsírbevitel és GERD tünetek összefüggését nem erősítették meg (68, 75).
1.3.2.8. Alkohol
Az alkohol emésztőrendszeri hatása függ az elfogyasztott alkohol minőségétől, mennyiségétől és időtartamától. Az alkohol csökkentheti a LES tónusát és reflux epizódokhoz vezethet (45). Állatkísérletes adatok igazolták az alkohol közvetlen nyálkahártyakárosító hatását (88), e mellett azonban az alkohol érzékenyítheti a nyálkahártyát, így a kellemtelen noxát (savas reflux) a beteg sokkal fájdalmasabbnak élheti meg. Az alkohol e mellett a gastrinelválasztás serkentése révén fokozott gyomorsavelválasztást okoz és gátolja a gyomorürülést (45).
22
A hosszú távú alkoholfogyasztás és GERD kapcsolatát viszont ellentmondásos eredményű vizsgálatok jellemzik. Egyes adatok szerint a kockázat fokozott (75), mások viszont nem találtak ilyen összefüggést (69, 72). Mindezek alapján az alkohol hatása nem egyértelmű, vélhetően nem tekinthető önálló, független kockázati tényezőnek.
1.3.2.9. Dohányzás
Epidemiológiai vizsgálatok adatai szerint a dohányzás a GERD kockázati tényezője lehet (89, 90). Kérdőíves vizsgálat pozitív összefüggést mutatott a dohányzás és GERD tünetek között (OR:1,35;95% CI:1,01-1,82) (91). Több kórfolyamat merült fel az összefüggés hátterében: a dohányzás csökkentheti a LES nyomást, csökken a nyáltermelés, ezáltal a nyál savat semlegesítő hatása is mérséklődik és megnyúlik a nyelőcső sav clearance-e (58). E mellett a dohányosokban köhögés-mély belégzés kapcsán ismétlődő intraabdominalis nyomásemelkedés szintén hozzájárulhat a tünetek rosszabbodásához (92). Bernstein tesztet és pH-metriát alkalmazó vizsgálatokban azonban nem igazoltak növekedett savas visszaáramlást nem dohányzókhoz viszonyítva, annak ellenére, hogy dohányosokban a reflux epizódok száma több volt (93, 94). Case-control vizsgálatban a dohányzás elhagyása nem vezetett a GERD tünetek javulásához a leszokást követően (95).
1.3.2.10.Fizikai aktivitás
A megerőltető fizikai aktivitás GERD kialakulásához vezethet, vagy ronthatják a GERD tüneteket, ahogyan egyes vizsgálatokban igazolták (58, 96-108) Atlétákban egyes GERD tünetek gyakrabban fordulnak elő (99). Mindezek alapján felmerült, hogy a fizikai aktivitás a GERD független kockázati tényezője lenne. Az eddigi adatok alapján úgy tűnik, hogy a túlzott, megerőltető aktív sport növeli a GERD kockázatát, azonban a mérsékelt sporttevékenységnek nincs ilyen hatása.
Clark tünetmentes egyénekben a futás, kerékpározás és súlyemelés hatását elemezve a GERD kockázatának növekedését állapította meg, s igazolta, hogy bizonyos sporttevékenység (pl.futás) refluxogén hatása kifejezettebb, mint pl. a kerékpározásé
23
(100). A sporttevékenységgel, fizikai aktivitással kapcsolatos egyes vizsgálatokat foglalja össze a 6. táblázat.
6.táblázat A fizikai aktivitás és GERD kapcsolata /Festi (58) alapján/
Tanulmány Módszer Minta
nagysága Pozitív összefüggés
Clark (100)
pH-metria 1 órás tevékenység (kerékpározás, futás,
súlyemelés)
12 Igen
Peters (101)
pH-metria 50 perces aktivitás
(kerékpár) sport-italok fogyasztása
7 atléta Igen
Collings (96) pH-metria 30 atléta Igen
Padolfino (97)
pH-metria manometria felső panendoscopia
1 órás tevékenység (futás, súlyemelés)
20 Igen
Nandurkar (68) GERD/diétás tényezők
Kérdőív 211 Igen
Ravi (98)
pH-metria, manometria közepes fizikai tevékenység, előtt, alatt
és után
135 Igen
Egy vizsgálatban nem csak a sporttevékenység, hanem a sportolás közben fogyasztott, magas szénhidráttartalmú italok oki szerepe is felmerült (101), összevetve a vízzel. Nem tisztázott, milyen mechanizmus vezet az aktív sporttevékenység során a GERD kialakulásához, s hogy bizonyos típusú sporttevékenység refluxogén hatása miért kifejezettebb. Több ok merült fel, többek között a fizikai aktivitás során észlelt megváltozott nyelőcső-motilitás (102); a nyelőcső kontrakciók frekvenciájának, amplitúdójának és időtartamának csökkenése (103); a fokozott hasúri nyomás gastrooesophagealis junkcióra kifejtett hatása (97); az emésztőrendszeri véráramlás csökkenése/hormonalis hatások/a nyelőcső motoros működésének változása/ a testhelyzet változása (58, 104).
24
A sportolók vizsgálata során nyert tapasztalatok azonban természetesen nem hasonlíthatók a mérsékelt, szokványos fizikai aktivitáshoz, amely ellenkezőleg, védő hatásúnak tűnik GERD-del szemben. Egy nagy populációs vizsgálat adatai szerint (105) a 30 perces fizikai aktivitás csökkentette a GERD tüneteket. Feltehetően a harántcsíkolt izomszövetre kifejtett hatás révén erősödik az antireflux barrier. Az eredményeket más vizsgálatban is megerősítették (69), egyúttal igazolták, hogy a GERD típusos tüneteitől szenvedők kevesebbet mozognak, szemben a tünetmentes egyénekkel.
Feltételezhető, hogy a fizikai aktivitás étkezéshez viszonyított ideje is fontos:
egy közlemény szerint az étkezést követő testmozgás inkább rontja a GERD tüneteket, míg a szabadidőben végzett testmozgásnak nincs ilyen hatása (106).
1.3.2.11. A GERD lehetséges új kockázati tényezője
Cammarota és munkatársai vetették fel,, hogy a GERD tünetei bizonyos foglalkozást végzők között gyakrabban fordulhatnak elő (109, 110).
Multicentrikus vizsgálatuk (110) célja annak elemzése volt, hogy a GERD tünetei milyen gyakoriak hivatásos énekeseknél kontroll egyénekhez viszonyítva.
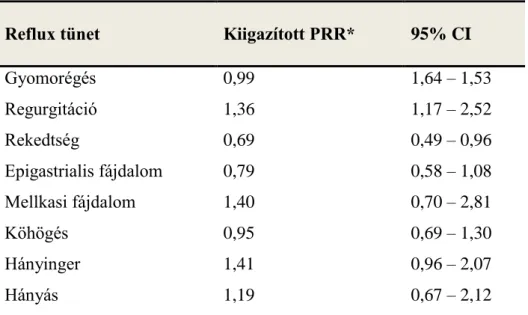
Kilenc olaszországi város 10 kórusának hivatásos operaénekese közül 351 vett részt a vizsgálatban. A kontroll csoportot 578, ugyanazon régióban élő, kornak és nemnek megfelelő személy alkotta. A vizsgálat során a résztvevők kérdőívet töltöttek ki; a személyes adatok, életmódbeli szokások (dohányzás, alkoholfogyasztás, szabadidős fizikai aktivitás, étkezési szokások) mellett a GERD tüneteire kérdeztek rá, úgy mint gyomorégés (retrosternalis égő fájdalom), regurgitáció (savas viszaáramlás a szájüregbe), mellkasi fájdalom (fájdalom/diszkomfort a mellkasban, amely független a gyomorégéstől vagy hasi fájdalomtól), dysphagia, rekedtség, köhögés (köhögési epizódok 4-6 alkalommal naponta). A tünetek gyakoriságát is rögzítették: 1-soha (az elmúlt egy évben), 2-kevesebb, mint 1 alkalommal havonta, 3- egy alkalommal havonta 4- egy alkalommal hetente 5- több alkalommal hetente 6- naponta. A gyomorégést/regurgitációt csak abban az esetben tulajdonították GERD-nek, ha a tünet egy héten több alkalommal is előfordult. Az operaénekeseknél többek között rögzítették hangmagasságukat és a gyakorlással eltöltött időt (óra/hét).
25
A vizsgálat eredménye szerint a hivatásos énekesek között a gyomorégés, regurgitáció, köhögés és rekedtség gyakrabban fordultak elő, mint a kontroll csoportban. A regurgitáció összefüggött az énekléssel eltöltött idővel (P=0,04) és a heti éneklési aktivitással is (P=0,005). A szerzők felvetik, hogy a tünetképzésben feltehetően a fokozott hasprésnek, a növekedett hasűri nyomásnak, a cruralis rekeszizomrostok aktivitásváltozásának lehet szerepe, amely rendszeresen, éveken át ismétlődve a GERD tünetek kialakulásához vagy rosszabbodásához vezethet.
1.3.3. A GERD tünetei
A GERD egyes tünetei annyira jellegzetesek, hogy rendszerint már a beteg alapos kikérdezése révén felállítható a kórisme. Az utóbbi évek szemléletváltását, a tünetvezérelt diagnosztika előtérbe kerülését jellemzi a GERD új felosztása is (Montreal-klasszifikáció) (5): a régi, elsősorban morfológiai alapú beosztás helyett elsősorban tünetorientált szemléletű.
Gyomorégés-„heartburn”, regurgitáció
A GERD „klasszikus” tünetei. A betegek változatos módon írhatják le a gyomorégést, jellemző módon retrosternalis égő érzés formájában jelentkezik, felfelé, az állkapocs felé sugározhat. Testhelyzet (hajolás) vagy bizonyos ételek/italok kiválthatják vagy fokozhatják a tünetet (24). Moayyedi és m.társai által végzett metaanalízis szerint, kérdőíves felmérés alapján a vizsgált népesség 25%-a panaszolt gyomorégést legalább egy alkalommal havonta, 12 %-uk hetente, 5%-nál pedig naponta fordult elő, a nemek között nem volt különbség. (111).
A regurgitáció során kis mennyiségű gyomortartalom áramlik vissza a szájüregbe, általában nem előzi meg hányinger. Alvás során előfordulva aspirációhoz, pneumonia kialakulásához vezethet (24).
Irodalmi adatok szerint a gyomorégés/regurgitáció szenzitivitása 30-76%
közötti, míg specificitása 62-96% között van erosiv oesophagitis tekintetében (112, 113). A gyomorégés/regurgitáció okozta fájdalom kórfolyamata nem teljesen tisztázott.
A gyomorsav mint elsődleges noxa szerepe kétségtelen, azonban különböző gyulladásos
26
mediátorok (interleukin 6,8, vérlemezke-aktiváló faktor,PAF) szerepe is fontos. GERD betegekben a refluxatum a fájdalomreceptorok közvetlen aktiválásához vezethet, amelyet a diffundáló sav tovább fokoz a károsodott nyálkahártya-barrieren keresztül. A fájdalomreceptorokat e mellett a refluxatum okozta nyelőcső-feszülés is aktiválja (114, 115)
Mellkasi fájdalom
A GERD tüneteként jelentkező mellkasi fájdalom, a nem szív-eredetű mellkasi fájdalom, „non-cardiac chest pain, NCCP” leggyakoribb oka. Az NCCP prevalenciája az átlag népességben 25% körül van (116), míg a GERD-hez köthető mellkasi fájdalom prevalenciája 15-40% közötti érték (6). Differenciáldiagnosztikai nehézséget jelenthet a GERD okozta mellkasi fájdalom, különösen, ha a jellemző tünetek (gyomorégés, regurgitáció) nem dominálnak, így koszorúsérbetegség gyanuja merülhet fel. A jelenlegi ajánlás szerint ezért a kardiális okot kell kizárni az emésztőrendszeri kivizsgálás előtt (112). Az elkülönítésben a kockázati tényezők felmérése, anamnézis-társbetegségek jelenléte, a kísérő tünetek értékelése segíthetnek. A kórisme felállításában további nehézséget okozhat a reflux által okozott koszorúérspazmus, amely következményes típusos anginás fájdalmat okoz („linked-angina”) (117).
Dyspepsia, hasi fájdalom, puffadás, hányinger
Irodalmi adatok szerint a dyspepsiás panaszok az átlagos népesség közel 40%- ában fordulnak elő, GERD fennállása esetén a panasz gyakoribb. A hasi fájdalom, puffadás, teltségérzet ezen GERD betegek többségénél megfelelően kezelhető protonpumpa-gátló szerekkel, a hányinger azonben kevésbé (112).
Dysphagia, odynophagia
Mindkét tünet jelentkezhet GERD esetén organikus szűkület nélkül is, azonban a legtöbb esetben szövődményes GERD (strictora, stenosis) vagy egyéb ok (daganat) állhat a háttérben, így az eszközös vizsgálat nem halasztható.
27 Légúti tünetek, fül-orr-gégészeti panaszok
Ezen tünetek a GERD gyakori extraoesophagealis tünetei. Az idült köhögés (8 héten túl fennálló köhögés) hátterében az esetek közel 20%-ában GERD igazolható. Fel kell vetni a GERD lehetőségét ilyen esetben, ha a beteg nem szed köhögést okozó gyógyszert, nem dohányzik, nem asthmás, vagy egyéb környezeti irritáló tényező, postnasalis csorgás kizárható (118). A tünet létrejöttében több kórfolyamat merül fel: a közvetlen légúti irritáció mikroaspiráció következtében, másrészt viszont – s az eddigi adatok alapján úgy tűnik, ez nagyobb jelentőséggel bír – a nyelőcső motilitászavara, a károsodott oesophagus-clearance, a vagus-mediált oesophago-tracheo-bronchialis reflex aktivációja révén okoz köhögést. Az asthma és GERD társulása is ismert: azon asthmás betegeknél, akiknek tünetei étkezést követően rosszabbodnak, vagy nem reagálnak megfelelően az asthamellenes kezelésre fel kell vetni GERD lehetőségét. Hasonlóan, ismert GERD betegeknél, akiknél a későbbiekben asthma jelentkezik, GERD-indukálta kórkép merül fel (118). Egy vizsgálatban asthmás betegek több mint felében igazoltak patológiás refluxot pH-metria során (119). Az idült laryngitis hátterében egyes adatok alapján az esetek ~60%-ában savas reflux áll (118). Rekedtség, torokköszörülés, globus- érzet, torokfájdalom a jellemző panasz. Az ismétlődő sinusitis, otitis media hátterében is felmerül a GERD oki szerepe.
Fogászati eltérések, halithosis
Egy szisztematikus irodalmi áttekintő tanulmány eredményei szerint a fogszuvasodás, halithosis hátterében is lehet a GERD a kóroki tényező (120).
28
1.4. A GERD diagnózisa
A diagnózis a tünetek (elsősorban a típusos gyomorégés/regurgitáció) értékelésével és eszközös vizsgálatok (endoszkópia, manometria, 24 órás pH monitorozás) segítségével, szükség esetén ezek kombinációjával állítható fel. A típusos tünetek mellett igazolt pozitív endoszkópos kép 97%-ban specifikus GERD-re (121).
Fontos hangsúlyozni azonban, hogy a típusos tünetek önmagukban is elegenedőek lehetnek a diagnózis felállításához. Ebben az esetben empirikus gyógyszeres kezelés indokolt savcsökkentő szerrel („PPI-teszt”).
Endoszkópia
Az endoszkópia révén megítélhetők a nyálkahártya-eltérések, az oesophagitis súlyossága,s egyúttal szövettani mintavételre is lehetőség van. Az értékelés során a Los Angeles osztályozás az elfogadott, az endoszkópia specificitása erosiv oesophagitis esetén kimagaslóan nagy (112). Nem hagyható azonban figyelmen kívül az a tény, hogy a típusos refluxos tünetekkel jelentkező betegek többségénél nem igazolható nyálkahártyaeltérés (NERD), s ez az endoszkópia diagnosztikus értékét korlátozza.
Az endoszkópia elvégzése feltétlenül szükséges alarm tünetek esetén (fogyás, anemia, hematemezis, dysphagia), Barrett nyelőcső diagnózisához és a követéshez.
„Screening” endoszkópia javasolható kockázati tényezők fennállása esetén (pl.
túlsúlyos, 50 év feletti beteg GERD panaszokkal). Megfontolandó a vizsgálat idős korban vagy NCCP esetén, ha a beteg nem reagál PPI kezelésre (112). Rutin biopszia elvégézése a diagnózis felállítására típusos tünetek, de normál endoszkópos kép esetén nem javasolt. A rutinszerű, ismételt endoszkópia Barrett nyelőcső vagy új tünetek hiányában enyhe (Los Angeles A-B) erosív oesophagitis esetén nem javasolt, azonban súlyos osophagitis esetén legalább 8 hetes kezelést követően indokolt (112).
24 órás pH monitor
Segítségével közvetlen módon mérhető a savas-epizódok száma, összefüggése a tünetekkel. Több eljárás ismert (wireless kapszulás vagy transnasalis katéteres
29
módszer), leggyakrabban a GERD diagnózisának felállításához használják negatív endoszkópia esetén. Elvégzésére gyógyszeres kezelés ellenére fennálló tünetek miatt is szükség lehet (121). Indikációt jelenthet e mellett NERD betegek tervezett anti-reflux műtéti beavatkozása előtt. A pH monitor szenzitivitása és specificitása is igen nagy (77- 100% és 85-100%) erosiv oesophagitis esetén, az érzékenység NERD esetén azonban alacsonyabb (<71%) (112).
Nyelőcső manometria
Bár a motilitászavar a GERD fő kóroki tényezője, a manometria mégsem javallt módszer a diagnózis felállításához. Ennek oka az lehet, hogy a GERD-ben megfigyelt motilitászavar nem diagnosztikus, nem áll rendelkezésünkre olyan minta, amely alapján pusztán a manometria birtokában a diagnózis egyértelműen kimondható lenne (121).
A vizsgálatnak tervezett műtét előtt lehet szerepe, e mellett az elkülönító kórismében, egyéb motilitászavarok (pl. achalasia, diótörő-oesophagus) kizárására használható.
Nyelőcső radiológiai vizsgálata (barium kontraszt)
A diagnózis felállításához ma már kis szenzitivitása és specificitása miatt nem javallt. Szerepe lehet azonban a GERD szövődményének gyanujakor (pl. strictura, stenosis) vagy dysphagia kivizsgálásakor (112, 121).
Empirikus kezelés, PPI-teszt
Típusos tünetek, alarmtünetek hiánya esetén megerősíti a kórismét a PPI szerekre adott kedvező válasz, a további eszközös vizsgálatok így elkerülhetők. A nem megfelelő terápiás válasz ugyanakkor más diagnózis irányába tereli a figyelmet. Egy 15 vizsgálatot tartalmazó összefoglaló elemzés szerint (122) a teszt szenzitivitása elfogadható (78%), specificitása azonban szerény (54%) amennyiben a pH metriát használták gold standardként.
Korábban elfogadott volt, hogy nem szív-eredetű mellkasi fájdalom esetén (akiknél a kardiális ok kizárható volt) az aggresszív PPI kezelés kedvező hatású,
30
GERD-et feltételezve a tünet hátterében. Egy újabb összefoglaló tanulmány szerint (123) azonban a PPI-re adott kedvező válasz azon betegeknél haladta meg a lényegességi szintet placeboval szemben, akiknél a GERD más objektív módon (endoszkópia, pH monitor) is igazolható volt. A terápiás válasz tekintetében nem volt különbség placeboval szemben azon betegeknél, akiknél más mődszerrel nem tudtak GERD-et igazolni. NCCP esetén ezért a kardiológiai ok kizárását követően a GERD bizonyítására eszközös vizsgálatok indokoltak (112). Légúti extraoesophagealis tünetek esetén azon betegeknél javasolt az empirikus kezelés, akiknél egyidejűleg típusos tüneteik is vannak. Típusos tünet hiányában pH monitor elvégézése javallt a PPI kezelés megkezdése előtt.
Történetileg elfogadott, hogy légúti tünetek esetén nagy dózissal kezdett PPI kezelés indokolt, bár ezen ajánlás nem-kontrollált, obszervációs vizsgálatok eredményein alapul (112).
31
1.5. A GERD szövődményei
Bár a reflux oesophagitis természetes lefolyásával kapcsolatban kevés az adat, a kórfolyamat alapján az oesophagitis tartós fennállása a szövődmények kialakulásának esélyét hordozza. A GERD ismert szövődménye a nyelőcsőfekély, strictura-stenosis, Barrett-oesophagus; ez utóbbi a nyelőcső adenocarcinoma kialakulásának veszélye miatt fontos. Elfogadott, hogy súlyos erosív oesophagitis (Los-Angeles C-D) vagy nem megfelelően kezelt erosív GERD esetén fokozott a kockázat, bár ezzel kapcsolatban kevés az adat (124).
1.5.1. Nyelőcsőfekély
A nyelőcsőfekély az eróziónál mélyebb, a muscularis mucosae réteget elérő defektus. Az odynophagia gyakori tünet, e mellett azonban dysphagia is kialakulhat, függetlenül attól, hogy valódi obstrukció fennáll-e vagy sem. Másfelől súlyos többszörös nyelőcsőfekély is tünetmentes lehet, esetleg a gyomorégés az egyedüli panasz. A diagnózist az endoszkópos vizsgálat, szövettani mintavétel adja: ennek a nyelőcsőráktól való elkülönítésben van jelentősége. A nyelőcsőfekély ritkán súlyos vérzéshez vezethet: egy vizsgálat adatai szerint a felső tápcsatornai vérzések ~5%-ért oesophagitis/nyelőcsőfekély felelős (125). Másik ismert szövődmény a penetratio a mediastinum vagy a légutak felé, amely kialakulhat erosív oesophagitis talaján, vagy Barrett-fekély esetén (126-128). A PPI kezelés hatékony a fekélyek gyógyulásában, sebészi bevatkozásra ritkán indokolt.
1.5.2. Nyelőcső strictura
A benignus nyelőcső-strictura leggyakoribb oka a GERD következményeként kialakuló pepticus strictura. A kórfolyamat összetett: kezdetben az izomszövet összehúzódása és a gyulladást kísérő oedema okoz szűkületet, amely visszafordítható. A folyamat előrehaladtával azonban idült gyulladás, kollagén-lerakódás és fibrosis alakul ki. A pepticus szűkület többnyire rövid (<1 cm), s általában a nyelőcső distalis harmadában alakul ki. A dysphagia a leggyakoribb panasz, de mellkasi fájdalom,
32
regurgitáció, gyomorégés is fennállhatnak (129-131). A kezeletlen, súlyos GERD betegek 7-23%-ában alakul ki pepticus strictura; epidemiológiai adatok szerint az incidencia alacsony, s az 1990-es évektől folymatosan csökken, amely összefügg a PPI szerek növekvő felhasználásával (132, 133).
Anatómiailag 2 típus különíthető el. Az „egyszerű” strictura rövid, egyszeres, endoszkóppal könnyen átjárható, míg az „összetett” strictura hosszabb, megtört és kifejezett szűkületet okoz. A diagnózis nyelés röntgen vizsgálattal és endoszkópia segítségével állítható fel. Ez utóbbi a szövettani mintavétel miatt különösen fontos, hiszen malignus folyamat kizárása elsődleges.
A kezelés sarkalatos pontja a gyulladás csökkentése, az oesophagitis gyógyítása emelt dózisú PPI-vel, e mellett endoszkópos dilatáció és szükség esetén sebészi beavatkozásra is sor kerülhet. Több vizsgálat igazolta, hogy a hatékony savszekréciógátló kezelés nem csak a tünetmentesség elérésében fontos, hanem egyúttal az endoszkópos dilatáció igényét is csökkenti (134, 135). Refrakter stricura esetén a lokalis steroid injekció kedvező hatásúnak bizonyult (136).
1.5.3. Barrett oesophagus
Barrett-oesophagus alakul ki, ha GERD következményeként a nyelőcső laphámját metaplasticus hengerhám foglalja el. E metaplasticus hengerhám DNS károsodása kimutatható, s igazolt, hogy a nyelőcsőadednocarcinomák többsége metaplasticus hengerhámból alakul ki (128, 137, 138). A Barrett nyelőcső a nyelőcső- adenocarcinoma leggyakoribb oka, a prevalencia a nyugati társadalmakban nőtt az elmúlt évtizedekben (139). A Barrett nyelőcső az endoszkópia során felismerhető:
amennyiben a metaplasia hossza>3 cm „long segment” Barrett, ha 3 cm-nél kisebb
„short segment” Barrett nyelőcsőről beszélünk. A GERD tünetek miatt végzett endoszkópia során egyes adatok szerint 3-5%-ban long segment, 10-15%-ban short segment Barrett nyelőcsőre derül fény. Nem tisztázott, hogy a két entitás különbözik-e a pathogenesisben és van-e különbség a nyelőcső-adenocarcinoma kialakulásának kockázatában (128, 140).
A rák kockázat klinikai vizsgálatok adata szerint 0,5%/év, s elfogadott, a Barrett nyelőcső rendszeres endoszkópos ellenőrzése az ismételt többszörös szövettani
33
mintavétel végett, bár nem áll rendelkezésünkre megfelelő, jól kontrollált vizsgálat arra vonatkozóan, hogy az eljárás csökkentené a mortalitást (128). Jelenleg azonban elfogadott, hogy Barrett nyelőcső esetén endoszkópos ellenőrzésre van szükség, a szövettani mintavételnek a dysplasia értékelésében van jelentősége. A jelenlegi ajánlások szerint dysplasia esetén (low grade/high grade megítélése) két patológus értékelése szükséges (141). A malignizálódásának több klinikai és endoszkópos prediktív tényezője ismert: a hiatus hernia mérete, a GERD súlyossága és fennállásának ideje, a Barrett segment hossza vagy a „high-grade” dysplasia (142).
Az endoszkópos követést tekintve elfogadott, hogy amennyiben dysplasia nem igazolható elég a beteget 3-5 év múlva ellenőrizni. Low-grade dysplasia esetén fél-egy év múlva, amennyiben azonban high-grade dysplasia igazolódik és nem történik intervenció 3 hónap múlva indokolt az ismételt vizsgálat. High grade dysplasia esetén a korai endoszkőpos követéssel szemben a jelenlegi állásfoglalás szerint intervenció (radiofrekvenciás abláció, fotodinamiás kezelés, endoszkópos mucosa-resectio) a választandó kezelési mód (141).
34
1.6. A GERD kezelése
1.6.1. Étrend- és életmódváltoztatás
A GERD kezelésében az életmódbeli és étrendi javaslatok széles körben elterjedtek, de kevés megbízható adat áll rendelkezésre ezek eredményességével kapcsolatban. Az elhízás a GERD kockázati tényezőjének tekinthető,s arra is vannak adatok, mely szerint a BMI normál testsúly esetén is összefügg a GERD tünetekkel – a súlygyarapodás kiválthatja vagy ronthatja a meglévő GERD tüneteket (54). A testsúlycsökkentés pedig e tekintetben kedvező hatású (84, 112, 143).
A fej ágyvégének megemelése gyakori tanács, amely elősegíti az oesophagus- clearance-t. Rendelkezésünkre áll olyan vizsgálat, amely az emelt fejvég kedvező hatást igazolta GERD-ben, csökkent a nyelőcső pH4 alatti időtartama (144).
Jelenleg nem áll rendelkezésünkre olyan adat, amely egyértelműen igazolja, hogy a kávé, fűszeres ételek, citrusfélék, csokoládé fogyasztásának abbahagyása javítaná a GERD tüneteit. Mindezek alapján a mindennapi gyakorlatban GERD kapcsán gyakran javasolt szigorú étrendi megszorításoknak nincs létjogosultsága (112), azonban ha a beteg kifejezett összefüggést észlel bizonyos étel és a tünetek megjelenése között, az természetesen figyelembe veendő.
1.6.2. Gyógyszeres kezelés
Prokinetikus szerek
A prokinetikumokat régóta alkalmazzák GERD kezelésében, főleg a LES tónusát emelő, a perisztaltikát kedvezően befolyásoló hatásuk miatt használatosak. A leggyakrabban alkalmazott vegyületek a metoclopramid és domperidon.
A metoclopramid növeli a LES tónusát, de számos központi idegrendszeri mellékhatása ismert (irritabilitás, agitáció, tardiv dyskinesis, depresszió). Amennyiben a tünetek hátterében gastroparesis nem igazolható, alkalmazása a GERD kezelésében nem javasolt. (112). A dopamin agonista domperidon a gyomorürülésre kedvező hatású, azonban GERD-del kapcsolatban kevés az adat. A GABA B receptor agonista, a TLESR-re gátló hatású baclofen alkalmazásának is határt szabnak a gyakori
35
mellékhatások (álmosság, gyengeség, fáradtság), egyelőre hivatalosan nem jóváhagyott szer GERD-ben. Igen hatékonynak bizonyult és korábban a GERD kezelésében elterjedt szer volt a cisaprid, azonban kardiovascularis, arrhytmogén mellékhatásai miatt kivonták a forgalomból (6, 112, 121, 145).
Savelválasztást gátló és savközömbösítő szerek
A GERD elsődlegesen motilitászavaron alapuló kórkép, ugyanakkor a konzervatív, gyógyszeres kezelés alapja mégis a hatékony gyomorsavszekréciógátló kezelés. Az e célra használható H2-receptor antagonista (H2RA) szereket az elmúlt két évtizedben világszerte a korszerű PPI-k váltották fel.
A gyomor fedősejtjei a savelválasztás mellett az intrinsic faktor termelésért is felelősek. A fedősejtek savszekréciójánsk serkentői az acetilkolin (n. vagus), a gyomor
„enterochromaffin like” (ECL) sejtekből származó histamin és a G-sejtek hormonja, a gastrin. A gastrin részben közvetlen módon, a fedősejtek cholecystokinin-B (CCK-B) receptoraira hatva vagy az ECL sejtek histamintermelésén keresztül közvetve fokozza a savelválasztást (146). A végső enzim a H+/K+-ATP-áz, a „protonmpumpa”, amely a savelválasztásért felelős.
Az első, hatékony savgátló gyógyszerek a H2-receptor antagonisták (famotidin, ranitidin, nizatidin) voltak: csökkentik mind a bazális, mind az étkezéssel serkentett savelválasztást (6). NERD esetén napjainkban is szerepük van a kezelésben, amennyiben alkalmazásukkal tünetmentesség érhető el. E mellett hatásosak lehetnek az éjszakai reflux-epizódok kivédésében, kiegészítve a nappal adagolt PPI-t.
A PPI szerek bevezetésével lehetőség nyílt a sokkal hatékonyabb savszekréciógátlásra, szemben H2-receptor antagonistákkal. A gyógyszerek szelektíven és irreverzibilisen gátolják a fedősejt H+/K+-ATPáz enzimjét. Az első vegyület az omeprazol volt, melyet 1989 óta alkalmaznak, később újabb készítmények kerültek forgalomba (pantoprazol, lanzoprazol, rabeprazol, ezomeprazol). Egy metaanalízis adatai szerint 8 hetes PPI kezelés során az erosív oesophagitis 85%-ban meggyógyul, míg H2RA-val ez az arány csak 52% (147). Az intragastricus pH 4 felett tartásának ideje jó összefüggést mutat az oesophagitis gyógyulásával (148-150).