Acta Pharmaceutica Hungarica 84. 1-8 2014.
Önemulgeáló rendszerek formulálása tenzid komponenseinek élő sejtekre gyakorolt hatásának ismeretében
UjHelyi Zoltán, Vecsernyés Miklós, BácskAy ildikó*
Debreceni Egyetem, Gyógyszertechnológiai Tanszék 4032 Debrecen Nagyerdei krt. 98., Magyarország
Levelezési cím: bacskay.ildiko@pharm.unideb.hu
Summary
Ujhelyi, Z., Vecsernyés, M., Bácskay, I.: Formulation and characetization of self-microemulsifying drug delivery systems according to their cytotoxic attributes
The aim of this study was to develop and examine novel drug delivery systems upon the cytotoxic behaviour of their tenside components. Different self-emulsifying combinations have been formulated by water dilution and oil dilution method with vari- ous previously tested tensides and co-tensides [11]. The visual properties registered against the increment of the applied tenside component in Ternary triangular diagrams. Cartesian coordi- nate calculation was applied to select the adequate compositions.
Self-emulsifying drug delivery systems are wildly used for en- hanced bioavailabilty of oraly administrated pharmacons. [12].
Full particulars of topical application of these systems have not been evaluated yet. In our study the cellular effects of the applied amphiphilic tensides on human Caco-2 and HeLa cell monolayers as dependent upon their chemical structures and physicochemi- cal properties have been evaluated. Cytotoxicity investigation was performed on Caco-2 and HeLa cells by MTT method. HeLa cells as in vitro model of cervix and Caco-2 cell monolayers as conve- nient and reliable in vitro models of the gastrointestinal tract have been chosen.
According to the results of the formulation procedures it can be determined that each developed SMEDD mixtures belong to type IIIa or IIIb in the lipid formulation classification system (LFCS) proposed by Pouton [12]. All of the formulated systems were immediately emulsified within the first second of contact with distilled water as dispersion medium and no evidence of phase separation or any instability problem have been observed for at least 72 h. The droplet diameter of dispersed self emulsifying compositions has been evaluated by Dynamic Light Scattering de- vice. We concluded that the increased Transcutol HP concentra- tions lead to an obvious improvement in the optical clarity, which correlates with the determined particle size of the corresponding dispersion. In cytotoxicity test the toxic properties of the applied tensides have not been found as additive parameter. The most toxic component determined the cytotoxicitxy of the SMEDDS.
Our results might ensure useful data for formulation of suit- able SMEDDS with lower active ingredient necessity. Developed SMEDDS might be advantageous in terms of increased bioavail- ability, minimized side effect, and hence the patient compliance.
Keywords: Sedds, Smedds, Cremophor, Labrasol, Transcutol, Caco-2, Hela.
Összefoglalás
Az új hatóanyagok és farmakonjelöltek száma az intenzív farma- kológiai kutatások sikerességének köszönhetően az elmúlt években a sokszorosára emelkedett. Ugyanakkor a klasszikus farmakológiai lehetőségek köre egyre szűkül, így rendkívül nagy szükség van olyan innovatív gyógyszerformák létrehozására, amivel a kívánt terápiás előnyök elérhetővé válnak [1]. Az új fejlesztésű hatóanya- gok jelentős része a Biofarmáciai Osztályozási rend alapján a III.
illetve IV. osztályba sorolható gyógyszeranyag. A farmakon meg- felelő feldolgozása mellett ügyelnünk kell a hatóanyag megfelelő biohasznosulására is [2]. A gyógyszertechnológiai formulálás során felhasznált biofarmáciai szemlélet nagymértékben hoz- zájárul olyan gyógyszerformák megtervezéséhez, amelyek a ko- rábban megismert hatóanyag tulajdonságait kedvezően befolyá- solják [3]. Számos gyógyszertechnológiai lehetőség kínálkozik a nehezen formulálható hatóanyagok szervezetbe juttatásának optimalizálására [4]. A vízben nehezen vagy egyáltalán nem ol- dódó gyógyszeranyagok gasztrointesztinális rendszerbe történő juttatásának előnyös megoldása lehet, különböző önemulgeáló illetve ön-mikroemulgeáló rendszer (SEDDS, SMEDDS) készí- tése [5]. Ezen S(M)EDDS-ek lehetőséget nyújtanak olyan, a BCS IV. osztályába tartozó farmakonok per os adására, melyeket ko- rábban csak parenterálisan tudtunk biztonságosan a szervezetbe juttatni [6]. Mint a legtöbb orálisan alkalmazott hatóanyagleadó rendszer, a különböző lipid alapú összetételek (lipid-based drug delivery systems LBDDS) is, biohasznosulást növelő képességü- ket különböző mechanizmusokon keresztül képesek kifejteni [7].
A rendszerek a disszolúciós lépés megkerülésével a hatóanyago- kat „elő-oldott” (pre-dissolved) állapotba vihetik, emellett csök- kenthetik ezen hatóanyag újbóli kiválását [8]. A P-gp vagy más efflux transzporter mechnaizmusok befolyásolásával a hatóanyag permeabilitása tovább javítható.
A gasztrointesztinális traktusból történő hatóanyag felszívó- dás fokozása kiemelkedően fontos feladat. Azonban érdemes meg- vizsgálni ezen hatóanyagleadó rendszerek biohasznosulást javító képességét más beviteli mód és terápiás módszer esetén is. Például a nőgyógyászati kezelések meghatározó részénél a lokálisan alkal- mazott terápia a mai napig kiemelt jelentőségű [9]. A gyógyszeres kezelés eredményességét ebben az esetben is kedvezőtlenül befo- lyásolja a felszívódási elégtelenség miatt szükségszerűen magas hatóanyag mennyiség [10]. A kísérletes munka során előállított ön-mikroemulgeálódásra képes rendszerek lehetőséget nyújthat- nak a kezelés eredményességének javítására külsőleges felhaszná- lás esetén is.
Kulcsszavak: Sedds, Smedds, Cremophor, Labrasol, Transcutol, Caco-2, Hela.
Bevezetés
A farmakonok alkalmazhatóságának és hatásossá- gának optimalizálásáért alkalmazott önemulgeáló- dásra képes összetételek sajátsága, az igen magas tenzid és kotenzid koncentráció [13]. Az önemulge- áló összetételek vizet nem tartalmaznak, csak olaj- ból és tenzidekből álló izotróp keverékek. Ezen rendszerekből vizes közegbe kerülve minimális energia befektetés hatására, nagy diszperzitásfokú o/v típusú mikroemulzió képződik [14]. A kis ré- szecskeméretű diszperz rendszer kialakítá sához elegendő energiát szolgáltat per os bevétel esetén például a gasztrointesztinális traktus motilitása is [15]. A hatóanyagok olaj/víz megoszlási koefficiense és a kialakult cseppméret módosíthatja a far ma
konok felszabadulását [16]. A vizes közegbe kerülés után a cseppméretet elsődlegesen az alkalmazott tenzid természete és koncentrációja határozza meg.
Egy olaj/nemionos tenzid/hatóanyag fázisdiagra- mot megszerkesztve meghatározható az az összeté- tel, ahol az önemulgeálódás maximálisan végbe- megy [17]. Mindezek alapján kijelenthető, hogy a megfelelő önemulgeáló közeg kiválasztásához szükséges megállapítani a hatóanyag szolubilizá
cióját a különböző komponensekben, az önemulge- áló régió területét a fázisdiagramon, valamint az önemulgálódást követően létrejött cseppek méretét Az önemulgeáló rend szerek alkalmazása a ne
hezen oldódó ható anya gok gyógyszerformában való alkalmazása mellett, lehetőséget nyújthat a bél lumenéből rosszul permeáló hatóanyagok maga- sabb biohasznosu lásának elérésére [16]. Mivel az önemulgeáló rendszerek képzéséhez felhasznált PEG monoészterek önmagukban is képesek befo- lyásolni a biológiai barrierek funkcióit [18]. Vízben rosszul oldódó hatóanyagok formulálása során szé- les körűen és nagy mennyiségben alkalmaznak a PEG mono észtereken kívül más szerkezeti struktú- rájú felü let aktív anyagokat is. Az ilyen rendszerek- kel tör ténő terápia biztonságos alkalmazhatóságá- hoz ezen tenzidek biológiai hatásvizsgálata részle- tes elemzésre szorul [19]. A PeG monoészter struk- túrájú Cremophor® vegyületek mellett fontos meg- vizsgálni az önállóan illetve segédemulgensként használt labrasol® t, mely szerkezetét tekintve mono-, di- és trigliceridek polietilén glikol mono- és diésztereinek definiált keveréke, valamint a koemulgensként széles körben alkalmazott azonos segédanyag családba tartozó különböző propilén glikol származékokat is. A komponensek vizsgála- tával részletes információhoz juthatunk egyegy gyógyszertechnológiai szempontból összeállított
rendszer biológiai hatásáról, illetve a gyógyszer- hordozóban lévő hatóanyag biohaszno su lá sá ról [20]. A bélhámsejteken végzett vizsgálatok hozzá- segítenek a megfelelő technológiai sajátságok eléré- se mellett jobban tolerálható gyógyszerforma kiala- kításához [21]. A cervikális sejtvonalon végzett kí- sérletek eredményei információt szolgáltathatnak az önemulgeáló rendszerek helyi alkalmazásának lehetőségéről, valamint előnyeiről. Amennyiben a rendszer ártalmatlansága bizonyítható, akkor se- gítségükkel az akár szükségszerűen magas terápi- ás dózisban adagolt hatóanyag mennyisége csök- kenthető [22]. Ezáltal a kedvezőtlen mellékhatások gyakorisága illetve súlyossága minimalizálható.
Kísérleti rész
A kísérletsorozatot megalapozó korábbi kísérletek Elvégzett kísérleteinkben vizsgáltuk több amfifil tenzidcsoport (összesen 16 felületaktív anyag tí- pus) Caco2 humán adenocarcinoma eredetű bél- hámsejtekre, HeLa cervix carcinoma sejtekre vala- mint humán erythrocytákra gyakorolt hatását kü- lönböző citotoxicitási tesztek (MTT, LDH, hemo
lízis teszt) segítségével. Ez alapján meghatároztuk a S(M)EDDS formuláláshoz felhasználásra kerülő tenzidek ic50 valamint HC50 értékeit. A magasabb ic50 értékekkel jellemzett tenzidek paracelluláris transzportra gyakorolt hatásának mérésével adato- kat kaptunk a felszívódás fokozó tulajdonságról.
Emellett két diszpenzeres Sigma 700 típusú ten zio
méter segítségével megmértük az anyagok felületi feszültség módosító képessége alapján, a tenzidek kritikus micella képzési koncentrációját. Mivel a tenzidek szolubilizáló képessége függ azok CMC értékétől, a kémiai szerkezetétől valamint a sejtek életképességére gyakorolt hatásuktól, ezért ezen adatok meghatározása után, összefüggéseket álla- pítottunk meg [23]. Ezen adatok ismeretében lehe- tőségünk volt olyan tenzideket kiválasztani, me- lyekből ezen szempontok alapján megfelelő ható- anyag leadó rendszerek formulálhatók.
Kísérlethez felhasznált anyagok
Az Izopropil mirisztátot a Merck Hungary Kft.től vásároltuk. A tenzidként felhasznált Labrasol, lauroglycol Fcc, lauroglicol 90, capryol 90 Capryol PGMC, Transcutol HP a Gattefossé Fran- ciaország kft. termékmintái. A cremophor rH 40 (Kolliphor RH40) a BASF Németország Kft.től ke- rült beszerzésre.
Terner rendszerek jelentősége a formulálás során Az önemulgeáló rendszerek alkotóinak jellemzé- sére használt háromszög diagramokban a kompo- nensek egymásban való kölcsönös oldhatósága el- térő [14]. Minden terner rendszer fázisdiagramján a háromszög csúcspontjai közül kettő a tiszta víz, illetve olaj komponenst jelöli [24]. A harmadik csúcshoz a formulálása során választott tenzid monokomponens vagy keverék rendelhető. Min- den ilyen háromfázisú rendszernél megállapítha- tóak olyan nyomás vagy hőmérséklet értékek, amelynél két összetevő csak részben vagy egyálta- lán nem elegyedik [25]. A harmadik komponens- ként használt felületaktív anyag jelenléte (mivel az részben elegyedik mindkét másik komponenssel) megváltoztatja a két részben elegyedő komponens kölcsönös oldhatóságát. Önemulgeálódó rendsze- rek képződésekor jelentős kémiai reakció nem ját- szódik le, így a rendszerek állapotának jellemzésé- hez a hőmérsékleten és nyomáson kívül az össze- tételre van szükség. Két komponens móltörtjének ismeretében a harmadik komponens móltörtje ki- számítható, a szabadsági fokok száma egy ilyen összetételben négy [26].
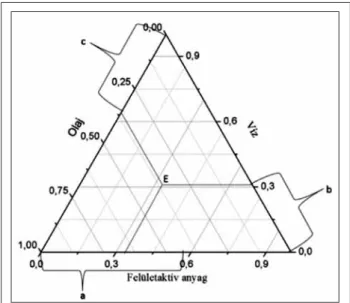
Adott körülmények között ennek megfelelően a rendszer állapotát a két összetétel adat egyértel- műen meghatározza. Ahhoz, hogy egy terner rendszer fázisdiagramját síkban ábrázolhassuk, két paramétert – célszerűen a nyomást és hőmér- sékletet – állandónak kell vennünk. Ez esetben a három komponens által meghatározott összetételt egyenlő oldalú háromszögben ábrázoljuk. A há- romszög oldalain az alkotó komponensek tömeg- százalékát tüntetjük fel. A háromszög diagram kö- rüljárási iránya tetszőlegesen megválasztható, vizsgálatainknál az óramutató járásával ellentétes irányt választottuk. A háromszög belsejében tet- szőlegesen kiválasztott E (mint elegy) pont össze- tételét úgy kapjuk meg, ha a ponton keresztül az oldalakkal párhuzamos egyeneseket rajzolunk és az egyes komponensek tömegszázalékait a megfe- lelő oldalakon leolvassuk [27]. A diagram egyegy oldala a folyadékpáronkénti kétkomponensű rend szerek összetételét adja meg (1. ábra).
Hatóanyag leadó rendszerek képzése Terner rendszerek alkalmazásával
Az önemulgeáló rendszerek képzését, számítógép vezérelt kapcsolt Schott Titronic® 200 automata diszpenzerekkel végeztük. A Gibbsféle fázissza- bályt alkalmazva a három komponensűnek tekintett
rendszert négy állapotjelző megadásával: a hőmér- séklet, a nyomás és két komponens móltört jének ér- tékeivel jellemeztük és a Terner rendszerben három- szög diagramon ábrázoljuk. A kísérletsorozatban vizsgálni kívánt két összetevő minden esetben egy vizes közeg és olajos fázisként izopropyl mirisztát volt, amihez hozzárendeltük a kiválasztott tenzidet vagy tenzid keveréket. A terner rendszerek segítsé- gével Cartesian/Descartesféle koordinátaszámítás- sal megállapítottuk az összetételek homogén hetero- gén vagy konjugált fázis összetételeit, valamint a rendszerek kritikus keveredési pontját. A homogén fázisösszetételek tulajdonképpen az önemulgeáló- dásra, illetve a diszpergált olajcseppek méretétől függően önmikroemulgeálódásra képes rendszerek.
A diszpergált fázis méreteloszlásának vizsgálata dinamikus fényszórás mérés segítségével
A dinamikus fényszórás fotometria (dls) gyors mérési lehetőség a diszpergált olajcseppek számos fontos paraméterének a meghatározásához. A vizsgálatok során a megvilágított diszpergált ré- szecskék által szórt fény analízise történik. A hete- rogén diszperz rendszer vizsgálata tulaj don
képpen a szórt fény időbeli változásának követése, autokorrelációs függvényének felvétele és analizá- lása mellett. A részecskék méreteloszlásának meg- határozásához Brookhaven Fotométert használ- tunk. Az emulziós rendszerek vizsgálatát 60º – 155°os szórási szögeknél végeztük. Minden szög- nél három korrelációs függvényt vettünk fel. A mérési időtartam minden esetben 300 s volt.
1. ábra: Terner rendszer összetételének meghatározása háromszögdiagramon. Az egyes komponensek tömegszázalék
arányai az óramutató járásával ellenkező irányban nőnek
Sejttenyésztés
Az önemulgeálódásra képes hatóanyagleadó rend- szerek élő sejtekre gyakorolt hatását a monolayer kialakítására képes Caco2 (human Causcasian Colon adenocarcinoma) valamint HeLa cervicalis carcinoma sejteken vizsgáltuk [28]. A kísérletek- hez használt Caco2 valamint HeLa sejtvonalat az ecAcc (european collection of cell cultures, Egyesült Királyság) sejtbankon keresztül szerez- tük be. A sejteket letapadó sejtkultúrához alkal- mas sejttenyésztő edényben (Nunc; Dánia), 10(v/v)% inaktivált fötális szarvasmarha szérumot (FBS, SigmaAldrich; Magyarország), 1(v/v)% nem esszenciális aminosavat (SigmaAldrich; Magyar- ország) és 100 mg/ml gentamicint tartalmazó DMEM (Dulbecco’s modified Eagle’s medium, SigmaAldrich; Magyarország) tenyésztő médium folyadékban növesztettük CO2 termosztátban (5%
co2 atmoszférában) 37 °Con 95% páratartalom mellett. A sejteken a tápoldat cserét minden 3. na- pon végeztük. A sejtek passzálásához 0,05 m/v%
tripszin 0,02 m/v % EDTA oldatot [0,5 % g/l trip- szin (SigmaAldrich; Magyarország); 0,2 g/l EDTA (SigmaAldrich; Magyarország)] használtunk. A vizsgálathoz 2245 passzázs szám közötti sejteket használtunk [9].
Sejt-életképességi vizsgálatok MTT teszt
Az MTT teszt során az életképes sejtek mitokondriumai a sárga színű 3(4,5dimetil
thiazol-2-il)-2,5-difenil-tetrazolium-bromidot (MTT) lila színű vízben oldhatatlan formazán kristályokká képesek átalakítani [29]. A vizsgálat- hoz a Caco2 sejteket 7 napig, a HeLa sejteket 4 na- pig az előző pontban ismertetett módszerrel, 96 lyukú tenyésztő plateben (104 sejt/lyuk) növesztet- tük. A növesztés során a 3. napon a médiumot le- cseréltük. A konfluens sejtréteg kialakulását köve-
tően különböző koncentrációjú, PBSben készült tenzid oldatot pipettáztunk a sejtekre. 30 perces inkubálás után, PBSel készült 0,5 mg/ml koncent- rációjú MTT oldatra cseréltük a vizsgálati mintá- kat. Majd 37 °Con 3 órán keresztül inkubáltuk. A felülúszó eltávolítása után a keletkezett formazán kristályokat 150 µl sósavas 2propanollal (2propanol:sósav = 25:1) oldottuk fel. Az oldatok abszorbanciáját FLUOstar Optima Microplate Reader (BMG LABTECH, Németország) segítségé- vel 570 nmen mértük. Korrigálásként kivontuk az 570 nmen mért abszorbancia értékekből a sejttör- melék szuszpenzió, mint háttér 690 nmen mért abszorbancia értékeit. A kísérlet során át nem ala- kult (feltételezhetően a sejttörmelékhez tapadó) festék nem befolyásolta a meghatározást, tekintet- tel arra, hogy a redukálatlan Mtt-nek nincs el- nyelése 570 nm–en. Az így kapott eredményeket, a kezeletlen kontroll minták abszorbancia értékei- hez viszonyítva százalékban fejeztük ki és a tenzid koncentráció függvényében ábrázoltuk [13].
A grafikonok segítségével meghatároztuk az egyes felületaktív anyagokra jellemző IC50 (az a tenzid koncentráció, amelynél az életképes sejtek aránya 50%) értékeket.
Eredmények
Hatóanyag leadó rendszerek képzése Terner rendszerek alkalmazásával
A formulálás során megállapítottuk, hogy a ko- rábban vizsgált felületaktív anyagok közül az ön- emulgeáló rendszerek képzéséhez a labrasol, a Transcutol HP valamint a Cremophor RH40 bizo- nyult megfelelőnek. Ezeket Terner diagramban ábrázolva kiválasztottuk az önmikroemulgeáló rendszerek képzésére legalkalmasabb összetétele- ket (1. táblázat). A rendszerek 1 ml-es mennyiségé- ben 1 ml izopropil mirisztátot kevertünk, majd az így kapott rendszert desztillált vízzel hígítva vizs- gáltuk a képződő emulziós összetételeket. A vizs- I. táblázat A kiválasztott önmikroemulgeáló rendszerek képzésére legalkalmasabb összetételek
Cremophor RH40 Transcutol HP Labrasol
Összetétel 1 33% 33% 33%
Összetétel 2 25% 50% 25%
Összetétel 3 20% 60% 20%
Összetétel 4 20% 40% 40%
Összetétel 5 16% 32% 52%
Összetétel 6 16% 52% 32%
gálat eredményeit pszeudoterner diagramban áb- rázoltuk (2. ábra). A pszeudoterner diagramok eredményei alapján a terápiás rendszerként legelő- nyösebbek a legnagyobb mikroemulzió képzési
„front”tal (maximum microemulsion existing zone) rendelkező 1., 2., valamint 3. (Összetétel 1, Összetétel 2, Összetétel 3) összetételek. Ezek közül is az 1:3:1 arányú Cremophor RH40 Transcutol HP Labrasol keverék a leginkább megfelelő igaz az
olajkomponenshez viszonyított Transcutol HP arány is itt a legmagasabb. A rendszereket ezt kö- vetően VIII. magyar gyógyszerkönyvi stabilitási vizsgálatoknak vetettük alá [30]. A tenzid összeté- telek 6 hónap eltartás során sem mutattak válto- zást [31]. A rendszerek mindegyikébe 1 ml izopropil mirisztátot keverve, majd az így kapott rendszert desztillált vízzel kétszázszorosára hígít- va kapott áttetsző vagy transzluens heterogén
diszperz rendszerek 1 hónap alatt nem mutat- ták a szétválás jeleit.
A diszpergált fázis méreteloszlásának vizsgálata az önemulgeáló
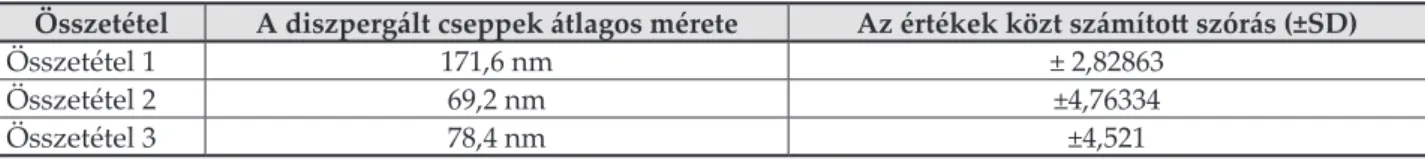
rendszerekben Az összetételekből fent leírt módon képzett emulziós heterogén rendszerekben a disz- pergált olajcseppek mé- rete DLS mérés alapján 171,6 és 69,2 nm között voltak (II. táblázat, 3.
ábra). Az eredmények megfelelnek a mikro- emulzió képződés fel- tételeinek. [32]
A citotoxicitási vizsgála- tok eredményei A rendszerek vizsgála- ta során megállapítha- tó, hogy azok a fizioló- giás kihígulásnak meg- felelő koncentrációban nem okozták a sejtek életképességének meg- változását. Ez a tulaj- donság azonban a kon- centráció emelésével változik. A kapott toxi- citási értékek sorrendi- II. táblázat A diszpergált olajcseppek mérete DLS mérés alapján
Összetétel A diszpergált cseppek átlagos mérete Az értékek közt számított szórás (±SD)
Összetétel 1 171,6 nm ± 2,82863
Összetétel 2 69,2 nm ±4,76334
Összetétel 3 78,4 nm ±4,521
2. ábra: Az összetételekből képződő emulziós rendszerek pszeudoterner diagramjai.
Az árnyékolt terület az ön-mikroemulgeálódásra képes összetételeket jelöli
sége azonos Caco2 valamint HeLa sejtvonalak esetében. A tenzid keverékek toxicitása kon- centrációfüggő, ugyanakkor nem additív tulajdonságként jelentke- zett [33]. Az alkotó tenzidek sejt- életképességre gyakorolt hatását a munkacsoportunk által végzett korábbi kísérletekben megvizs- gáltuk [24]. Az eredményeket összehasonlítva elmondható, hogy a rendszerek toxikus ka- raktere az alkotó komponensek közül a legtoxikusabb tenzid sejtkárosító képességének mérté- kével megegyezik. (4. és 5. ábra).
Statisztikai analízis
A mérések során kapott eredmé- nyeinket statisztikailag a SigmaStat (version 3.1; SPSS, Inc.) segítségével elemeztük. Az ered- ményeink között ez alapján szá- mított átlagukat tüntettük fel ± SD. A csoportok összehasonlítá- sát one WAy AnoVA módszer- rel végeztük, amelyet Tukey’s teszt követett. A kísérleti ered- ményeinket legalább 3 párhuza- mos mérés szolgáltatta, a különb- ségeket p < 0.05 esetén tekintet- tük szignifikánsnak
Következtetések
Kísérletsorozatunkban különbö- ző kémiai szerkezetű és HLB ér- tékkel jellemezhető tenzidekből önemulgeálódásra képes ható
anyagleadó rendszereket képez- tünk. A kutatócsoport által ko- rábban elvégzett kísérleteinkben a formulációhoz felhasználni kí- vánt tenzid csoportokból, azok sejtéletképességre gyakorolt ha- tása alapján, a Labrasolt, a Transcutol HPt, valamint Cre
mophor RH40t választottuk ki az önemulgeáló rendszerek kép- zéséhez. A sejtkárosító hatás meg állapítására a mitokondriális aktivitásváltozást illetve az 3. ábra: A diszpergált olajcseppek méreteloszlása DLS mérés alapján
extra celluláris LDH aktivitásváltozást mértük [34].
A kiválasztott felületaktív anyagok hidrofil alko- tójukban és a zsírsav komponenseik szénatom számában is különböztek. A Labrasol esetében pe- dig a molekula észterezettségi foka is eltérő. Ko- rábbi eredményeink alapján megállapítottuk, hogy a felületaktív anyagok koncentrációfüggően képesek befolyásolni az élő sejtek arányát Caco2 sejtvonalon végzett in vitro kísérletekben [23].
Munkánk során megvizsgáltuk, hogy ezen is- mert toxikus karakterrel jellemezhető tenzidekből
keveréket képezve a sejtká- rosító hatás egyegy kom- ponensre jellemző vagy ad- ditív tulajdonság. Az ön- emulgeáló rendszerek kép- zését automata diszpen- zerek segítségével olaj illet
ve víz dilúciós módszerrel végeztük. A kiválasztott tenzidek különböző arányú keverékét pszeudo terner di- agramban vizsgálva megál- lapítottuk, hogy hat összeté- telben a mikro emulzió kép- ződése jelentős hígulás mel- lett is kifejezett. A pszeudo
terner diagramok ered mé- nyei alapján a terápiás rend- szerként legelőnyösebbek a legnagyobb mikroemulzió képzési „front”tal (maximum micro emul sion existing zo
ne) rendelkező 1.,2., vala- mint 3. (Összetétel 1, Össze- tétel 2 , Összetétel 3) össze- tételek. Ezek közül is az 1:3:1 arányú Cremophor rH40 transcutol HP lab- rasol keverék a leginkább megfelelő [35].
dinamikus fényszóráson alapuló részecskeméret meg- határozás során megállapí- tottuk, hogy ezen előnyös- nek talált összetételek 200 szoros hígításaiban az elosz- latott diszperz fázisú olaj- cseppek mérettartománya a 69172 nmes intervallum- ban vannak. Ez a mérettar- tomány megfelelő a célként kitűzött biohaszno sulást nö- velő összetétel kialakításához. A kialakított ön- emulgeálódó rendszerek alkalmazhatóságát meg- határozza az összetételek stabilitása. Ennek bizto- sítására stabilitási teszteket végeztünk a vízmentes összetételekkel illetve a képződött mik roemulziós rendszerekkel egyaránt. Vizsgálataink során a tenzid összetételek hat hónap során nem mutattak elváltozást. Az olaj komponenst tartalmazó rend- szereket kétszázszorosára hígítva létrejött áttetsző vagy transzluens heterogén diszperz rendszerek 1 hónap alatt nem mutatták a szétválás jeleit.
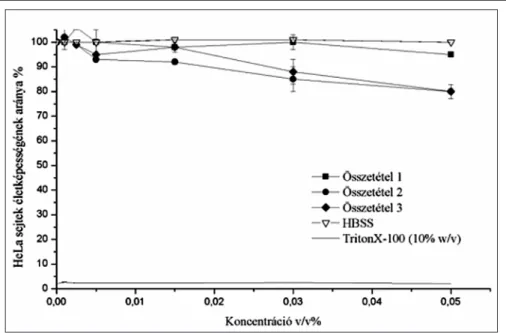
4. ábra: Az 1.,2. valamint 3. Összetétel hígításainak HeLa sejtek életképességre gyakorolt hatása MTT teszt segítségével vizsgálva (p<0,05)
5. ábra: Az 1.,2. valamint 3. Összetétel hígításainak Caco-2 sejtek életképességre gyakorolt hatása MTT teszt segítségével vizsgálva (p<0,05)
Kísérletsorozatunk tervezésekor célul tűztük ki a tenzid keverékek élő szervezetre gyakorolt hatásá- nak vizsgálatát. A gyógyszertechnológiailag meg- felelőnek talált összetételeket MTT sejtéletképességi vizsgálat segítségével karakterizáltuk. A kísérlete- ket HeLa illetve Caco2 sejtvonalon elvégezve a fe- lületaktív anyagok toxikus tulajdonságát nem talál- tuk additív jellemzőnek. Ezen eredményeket az összetételek paracelluláris transzportra gyakorolt hatásának vizsgálatával kiegészítve hasznos adato- kat szolgálhatnak a hatóanyagleadó rendszerek az in vitro valamint in vivo körülmények közötti visel- kedésének megismeréséhez [36].
Kutatási eredményeink újabb igazolásul szol- gálnak a gyógyszertechnológiai segédanyagok széleskörű vizsgálatának szükségszerűségéhez. A kialakított gyógyszerformák technológiai megfele- lősége alapvető, de nem elegendő feltétele a sike- res gyógyszeres terápiának. A biofarmácia szem- lélet elengedhetetlen az új innovatív gyógyszerek kialakításához. Hiszen csak az ilyen szemlélettel kifejlesztett készítmények képesek az optimális gyógyszerhatás elérése céljából csökkenteni a szervezetbe juttatott hatóanyag mennyiségét, elkerülnve a nem kívánatos mellékhatásokat, és a terápiás igényeknek megfelelően, a hatóanyagfel- szabadulását, tervezett módon, a megfelelő helyen és időben, meghatározott sebességgel biztosítani.
Támogatás
A kutatás a táMoP 4.2.4.A/2-11-1-2012-0001 azo- nosító számú Nemzeti Kiválóság Program – Hazai hallgatói, illetve kutatói személyi támogatást biztosító rendszer kidolgozása és működtetése konvergencia prog- ram című kiemelt projekt keretében zajlott. A pro- jekt az Európai Unió támogatásával, az Európai Szociális Alap társfinanszírozásával valósul meg.
irodAloM
1. Kasim, N.A., Whitehouse, M., Ramachandran, C., Ber- mejo, M., Lennernäs, H., Hussain, A.S., Junginger, H.E., Stavchansky, S.A., Midha, K.K., Shah, V.P., Amidon G.L.:
Mol. Pharm., 1, 85-96 (2004).
2. Dévay, A. Antal, I. :A gyógyszeres terápia biofarmáciai alapjai. Medicina, Budapest 4352. (2009).
3. Yang, A.D., Bauer, T.W., Camp, E.R., Somcio, R., Liu, W., Fan, F., Ellis, L.M.,Qiao, L., Zhang, Q., Yan, H., Liu, K.:
cancer, 103, 1561-1570 (2005).
4. Au, JL,: J.Control. Release, 74, 31-46 (2001).
5. Zhu, J.X., Tang, D.,Feng, L., Zheng, Z.G.,Wang, R.S.,Wu, A.G.,Duan, T.T., He B., Zhu, Q.: Drug Dev. Ind. Pharm.
39(3) 499-506 (2013).
6. Sagitani, H., Friberg, S.E.: J. Disper. Sci. Technol. 1(2), 151–164 (1980).
7. Porter, C.J. et al.: Nat. Rev. Drug Discov. 6, 231–248 (2007).
8. Huiling, M., René Holma, B., Anette, M.: Int J Pharm 453, 215– 224 (2013).
9. Gerd, J., BauerschmitzA., K.,Minghui W.,Isabell H.,Denise R. Shaw.,Theresa V. Strong, Renee Desmond, Daniel T. Rein, Peter Dall, David T. Curiel, Akseli Hemminki: Int J Cancer 111(2), 303-309 (2004).
10. Bodner K, Bodner-Adler B, Wierrani F, Kubin A, Szölts- Szölts J, Spängler B, Grünberger W.: Anticancer Research 23(2c), 1785-1788 (2003).
11. Ujhelyi, Z., Fenyvesi F, Váradi J, Fehér P, Kiss T, Veszelka S, Deli MA, Vecsernyés M, Bácskay I.: Eur J Pharm Sci 47, 564–573 (2012).
12. Pouton, C.W.: Eur. J. Pharm. Sci. 29, 278–287 (2006).
13. Cololmbo, D.: Int J Immunopath Pharmacol 203(4), 1177-1183 (2010)
14. Pouton, C.W.: Eur. J. Pharm. Sci. 11(suppl. 2), 93–98 (2000).
15. Gao, P. Rush B.D., Pfund W.P., Huang T., Bauer J.M., Mo- rozowich W., Kuo M.S., Hageman M.J.: J. Pharm. Sci., 92, 2386–2398 (2003).
16. Sagar S.R., Anderson B.D.: Adv Drug Deliv Rev 60, 638–
656 (2008).
17. Sujoy P., Amiya K.J.: Colloids and Surfaces A: Physico- chemical and engineering Aspects 419, 113-124 (2013).
18. Wang C.H. Qiao L., Zhang Q., Yan H., Liu K.: Int. J. Pharm 430(1-2), 372-380 (2012).
19. Menard, N. Tsapis N., Poirier C., Arnauld T., Moine L., Lefoulon F., Péan J.M., Fattal E.: Int. J. Pharm 28, 423(2) 312-20 (2012).
20. Gursoy, N., Garrigue, J.S., Razafindratsita, A., Lambert, G., Benita, S.: J. Pharm. Sci. 92, 2411–2418 (2003).
21. Fischer, S.M., Brandl, M., Fricker, G.: Eur. J. Pharm. Bio- pharm. 79, 416–422 (2011).
22. Eckert L.O, Lentz G.M: Infections of the lower genital tract: Vulva, vagina, cervix, toxic shock syndrome, HIV infections. In: Katz VL, Lentz GM, Lobo RA, Gershen- son DM, eds. Comprehensive Gynecology. (5) 2. (2007) 23. Lalikoglu, M., Bilgin M.,: Fluid Phase Equilibria 371,
50–56 (2014).
24. Altena F.W., Smolders C.A.: Calculation of LiquidLiq- uid Phase separation in a ternary system of a Polymer in a Mixture of a Solvent and a Nonsolvent Macromol- ecules, 15, 1491–1497 (1982).
25. Espinosa, G.P., Scanlon M.G.: Res Intern 53(1), 49-55 (2013).
26. Atkins PW.: Physical Chemistry for the Life Sciences. W H Freeman & co,448-451. (2005)
27. Bigansoli, E., Cavenaghi, L.A., Rossi, R., Brunati, M.C., Nolli, M.L.: Farmaco 54, 594–599 (1999).
28. Mosmann, T.: J. Immunol. Method. 65(1–2), 55–63. 572 (1983)
29. Magyar Gyógyszerkönyv VIII. kiadás Országos Gyó- gyszerészeti intézet, Budapest 2653-2660. (2008) 30. Jones, David: Pharmaceutics Dosage Form and Design
1th edition, Pharmaceutical Press 274-279. (2008) 31. Sjoblom, J.,: Encyclopedic Handbook of Emulsion Tech-
nology, Marcel dekker inc., (2001)
32. Palamakula, A., Khan, M.A.: Int J Pharm. 273(1-2), 63-73 (2004).
33. Sha, X., Yan, G.,Wu, Y., Li, J., Fang, X.: Eur. J. Pharm. Sci.
24, 477-486 (2005).
34. Zhang P, Liu Y, Feng N, Xu J.: Int J Pharm 355(1-2), 269–
76 (2008).
35. Fotakis, G., Timbrell, J.A.: Toxicol. Lett. 160, 171–177 (2006).
Érkezett: 2014. június 15.