RÖVIDÍTÉSEK JEGYZÉKE
BEVEZETÉS – IRODALMI ÁTTEKINTÉS
AZ RNS INTERFERENCIA BEMUTATÁSA
- AZ RNS INTERFERENCIA TÖRTÉNETE
- AZ RNS INTERFERENCIA MECHANIZMUSA ÉS JELLEMZŐI
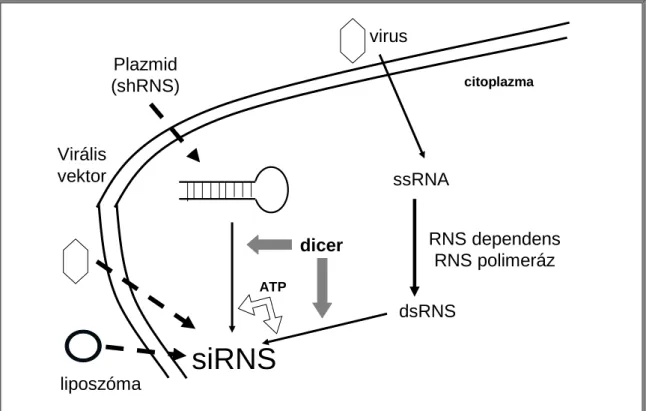
- Az siRNS-ek keletkezése
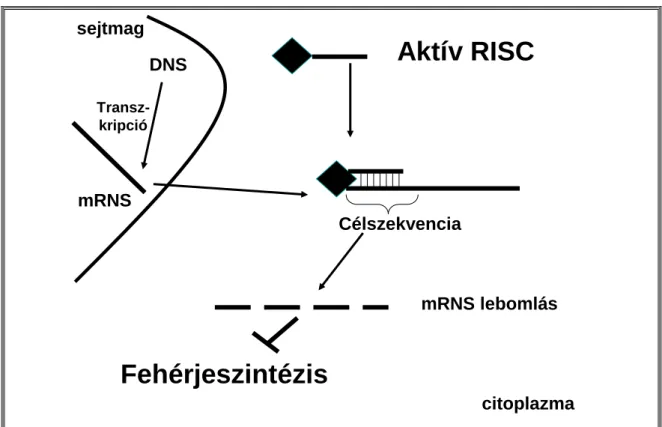
- Az RNS interferencia hatásmechanizmusa
- Az RNS interferancia energiaigénye
- Az RNS interferencia hatásának amplifikálása
- Az RNSi élettartalma
- SiRNS szintézis
- siRNS adatbázisok
- A RÖVID RNS-EK INTRACELLULÁRIS BEVITELÉNEK
- Vírus alapú bejuttatási stratégiák
- Nem-vírus alapú bejuttatási stratégiák
- AZ RNSi GYÓGYÁSZATI ALKALMAZÁSA
- AZ RNS INTERFERENCIA ALKALMAZÁSA
- Az apoptózis szabályozása vese iszkémia-reperfúziós károsodásban (IRI)26
- Az RNSi alkalmazása vesetumorokban
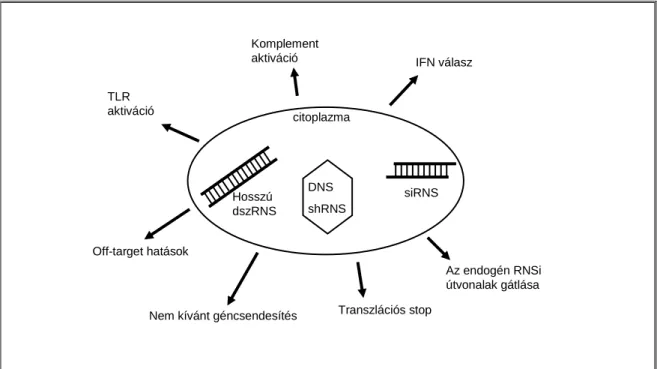
- AZ RNSi LEHETSÉGES MELLÉKHATÁSAI
- Az interferon válasz aktiválása, jelátviteli útvonalai, és az interferonok
- Az Oligoadenilát-szintetáz (OAS) szerepe az antivirális válaszban
- A célgéneken kívüli csendesítés (off-target silencing)
- A veleszületett immunrendszer aktiválódása a Toll-Like Receptorok (TLR-
- A komplement aktiváció
Mindezek eredményeként az siRNS-ek szerkezete ma már gondosan optimalizálva van, ami elengedhetetlen az RNSi specifitása szempontjából. Manapság számos vírus alapú (adenovírus, adeno-asszociált vírus, oncoretrovírus, lentivírus vektorok) és nem vírus alapú (liposzómák, nanorészecskék vagy peptid-lipid transzfekciós eljárások) szállító rendszer létezik az siRNS-ek sejtekbe való eljuttatására. Ha az siRNS-eket intravénásan, nagy térfogatban (az állat keringő vérének 50-100%-a) rövid időn (maximum 10 másodpercen belül) injektálják, a folyadék felhalmozódik a vena cava inferior rendszerében.
Az siRNS transzfekciós reagensek leggyakrabban kationos lipid alapú vegyületek, amelyek "bekapszulázzák" az siRNS-t, így megakadályozzák azok lebomlását és fokozzák a sejtbe való felvételüket, még in vivo is.
KRÓNIKUS VESEBETEGSÉGEK, EZEN BELÜL A LUPUS NEPHRITIS
Az IVIG (2 g/ttkg dózisban) javallatai közé tartoznak az SLE súlyosabb megnyilvánulásai [171,172] vagy a szteroidok vagy a ciklofoszfamid adagjának csökkentése a terápiában [173,174]. Korábbi kutatások eredményei szerint a nefrotoxicitás oka az IVIG készítmények cukorkomponense [184], amely az immunglobulin G tercier szerkezetének stabilizálására szolgál [185, 186].
CÉLKITŰZÉSEK, KÉRDÉSFELTEVÉS
Láthatók-e szervspecifikus változások a hosszan tartó, nagy dózisú, glicin stabilizált IVIG kezelés hatására (vesefunkció, autoantitestszint mérés, szövettani kiértékelés). A hosszú távú, nagy dózisú, glicinnel stabilizált IVIG kezelésnek van-e in vivo toxicitása a cukoroldattal kezelt kontrollcsoporthoz képest?
ANYAG ÉS MÓDSZER
Az interferon választ vizsgáló kísérletünkben alkalmazott anyagok,
- Vizsgálati állatok
- siRNS-ek
- Kezelések
- siRNS kimutatása a szövetekben
- Az állatok leölése
- Az alanin aminotranszferáz (ALAT) és aszpartát aminotranszferáz (ASAT),
- RNS izolálás
- cDNS szintézis
- Kvantitatív valós idejű polimeráz láncreakció (RT-PCR)
- Szövetminták festése és kiértékelése
- Plazma citokin szintek mérése ELISA módszerrel
- Statisztikai elemzések
SiRNS-eket injektáltunk egerekbe módosított in vivo hidrodinamikus injekció (HDI) protokoll segítségével [199], Zhang módszerének megfelelően. Az siRNS-oldat befecskendezése után a kezelt területet 30 másodpercig rögzítjük, hogy megakadályozzuk az injektált oldat visszafolyását. 3, Interferonválasz kiváltására a pozitív kontrollcsoport (n=24) állatainak 0,1 ml sóoldatban oldva 50 μg poliinozin-policitidinsavat (poliI:C) (Sigma, P9582, Budapest, Magyarország) adtak. oldatot (végső koncentráció: 500 μg/ml) és a szakirodalom szerint intraperitoneálisan injektáltuk [200].
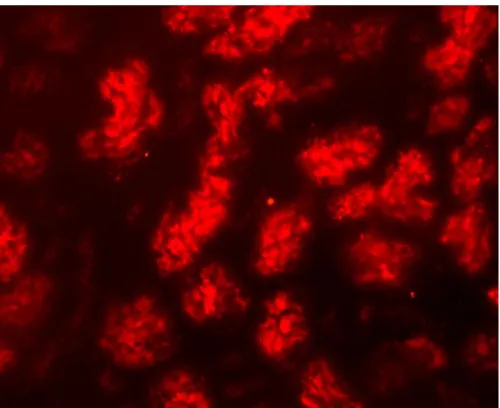
Az irodalomban leírt, nagy térfogatú hidrodinamikus injekció májkárosító hatásának modellezésére a testtömeg 10%-ának megfelelő térfogatú fiziológiás sóoldatot fecskendeztek az állatok farokvénájába 10 másodpercen belül, majd az állatokat leölték. 24 óra elteltével (n=10/csoport). Az siRNS-ek sikeres felvételének és intracelluláris lokalizációjának bizonyítására fluoreszcensen jelölt siRNS-t (BlockiT Alexa Fluor Red Fluorescent Oligo, Invitrogen Budapest) adtunk az állatoknak a fent leírt hidrodinamikus úton, majd a kezelést követően 10-30 perccel a vese, a májból és a lépből. Az állatok egy külön csoportját másfél, 2, 6 és 9 órával az AVHDI-kezelés után leöltük, hogy megmérjük a szervfunkciós paramétereket és a plazma citokinszintjét.
A veséből, májból és lépből kivágott szövetmintákat műanyag fagyasztócsövekbe helyeztük további RNS vizsgálatokhoz, és -80 °C-on tároltuk. A lemezeket ezután egy éjszakán át 4 °C-on (IL-6 és IL-12p40) vagy két órán át szobahőmérsékleten (TNFa) inkubáltuk. További öt mosás után avidin-torma-peroxid oldatot adtunk a lyukakba (100 μl/lyuk), majd további 30 perces inkubálás következett szobahőmérsékleten.
Az IVIG hatásait felmérő kísérletben használt anyagok és módszerek
- A kísérleti állatok
- Az állatok kezelése
- Az állatok leölése
- Szövettani vizsgálatok
- Immunhisztokémiai vizsgálat
- Lupus autoantitest panel vizsgálata
- Statisztikai elemzések
EREDMÉNYEK
Az interferon választ vizsgáló kísérlet eredményei
- A hatékony siRNS felvétel vizsgálata immunfluoreszcens mikroszkóppal
- A fiziológiás sóoldat alacsony volumenű hidrodinamikus injektálása
- Az alacsony volumenű hidrodinamikus injektálás hatására az általunk
- A polyI:C kezelés szervi károsodással járó interferon választ váltott ki
- Az siRNS-ek alacsony volumenű hidrodinamikus injektálása után nem
- A magas volumenű hidrodinamikus injektálás májra gyakorolt hatásainak
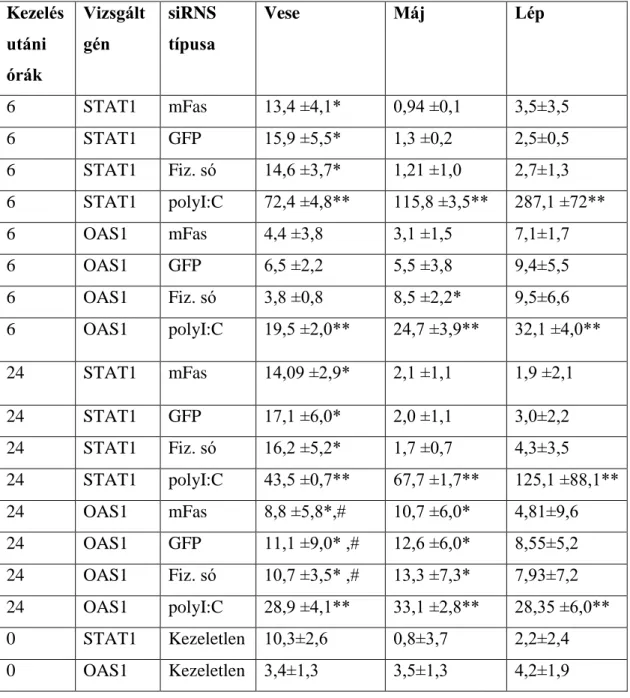
A fiziológiás sóoldat kis térfogatú hidrodinamikus injekciója kismértékben növelte a STAT1 és OAS1 génexpressziót, ami siRNS-ek hozzáadása után nem javult. RT-PCR méréseink szerint a STAT1 és OAS1 génexpresszió szignifikáns növekedését tapasztaltuk a polyI:C 6-tal kezelt pozitív kontroll egereinkben a kezelés után 24 órával. Az siRNS-sel kezelt állatok STAT1 és OAS1 génexpressziója nem mutatott szignifikáns változást a szervtől, az siRNS szekvenciától vagy az időtől függően, összehasonlítva a csak fiziológiás sóoldattal kezelt állatok génexpressziós mintázatával.
Az siRNS-ek fiziológiás sóhoz való hozzáadása tehát nem vezetett további, szignifikáns növekedéshez a STAT1 és OAS1 gének expressziójában. A kis térfogatú hidrodinamikus injekció miatt az általunk vizsgált szisztémás gyulladásos citokinek (IFNβ, TNFα, IL-6 és IL-12p40) és a nem szisztémás gyulladásos citokinek (IFNβ, TNFα, IL-6 és IL) plazmaszintjét - 12p40) nem mutatott szignifikáns növekedést. Ezzel szemben az siRNS-kezelés nem eredményezett szignifikáns növekedést ezen citokinek plazmaszintjében a poliI:C-kezelt csoporthoz képest.
A polyI:C injekció hatására az IL-6 szintje szignifikánsan emelkedett, melynek csúcsa 2 órával a kezelés után következett be, majd koncentrációja gyors csökkenést mutatott. Az siRNS-ek kis térfogatú hidrodinamikus injektálása után szervi működést és szövetkárosodást nem figyeltek meg. Az ALAT aktivitása a kis térfogatú hidrodinamikus injekció után (AVHDI: .. 1 ml) megközelítőleg kétszeresére nőtt a kezeletlen állatokhoz képest (11/A ábra), majd 24 órán belül visszaállt kiindulási értékére.
Az IVIG hatásait felmérő kísérlet eredményei
- A magas dózisú IVIG szisztémás adása enyhítette a bőrbetegséget
- A glomeruláris funkció változása IVIG kezelés hatására MRL/lpr egerekben
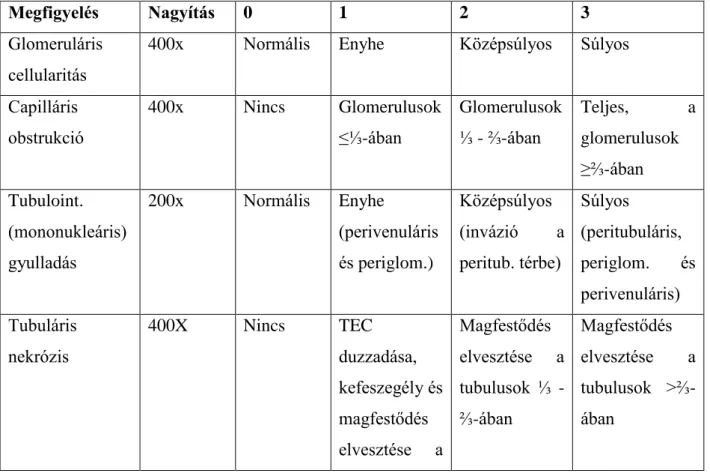
- Tubulointestíciális elváltozások
- A vese hidropikus degenerációjának (ozmotikus nefrózis) vizsgálata a
- Komplement-3 (C3) lerakódás vizsgálata bőrben és vesében
- Plazma autoantitest vizsgálata IVIG kezelt MRL/lpr egerekben ELISA
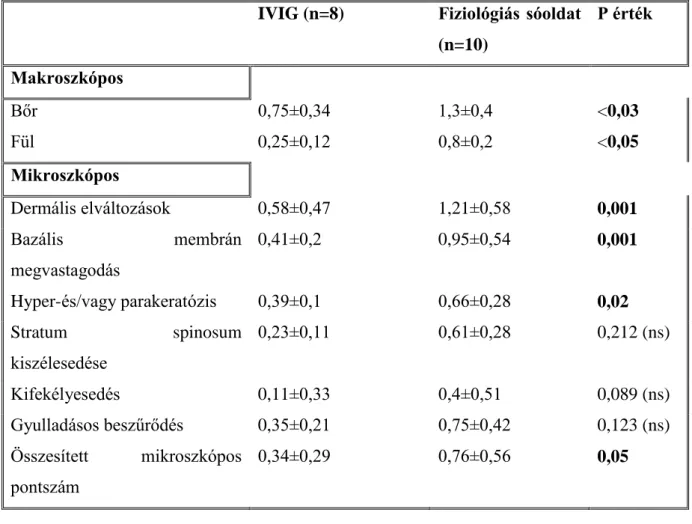
A bőrelváltozások makroszkópos és mikroszkópos értékelésére alkalmazott szemikvantitatív pontozási rendszer alapján azt találtuk, hogy az IVIG kezelés jelentősen enyhítette a bőrtüneteket. Megfigyeltük továbbá, hogy a kontrollcsoport tagjainál általános nyirokcsomó-megnagyobbodás alakult ki, míg a nyirokcsomó-megnagyobbodás kevésbé volt szembetűnő az IVIG-vel kezelt állatokban (nem publikált adatok). Változások a glomeruláris funkcióban IVIG kezelés hatására MRL/lpr egerekben Proliferatív típusú, hipercelluláris lupus kezeletlen MRL/lpr egerekben A kezeletlen MRL/lpr egerekben proliferatív típusú, hipercelluláris lupus nephritis alakult ki.
Az IVIG-vel és sóoldattal kezelt állatok vesetubulusaiban akut gyulladás jeleit (tubularis nekrózis, kiterjedt gyulladással járó tubulitis és ezt követő hámpusztulás) figyelték meg. A maltózzal és szacharózzal kezelt állatok vér karbamid-nitrogénszintje a normál és az MRL/lpr egerek szintje között volt. Plazma autoantitestek vizsgálata IVIG-vel kezelt MRL/lpr egerekben ELISA-val és indirekt immunfluoreszcens módszerrel és indirekt immunfluoreszcens módszerrel.
MEGBESZÉLÉS
A szisztémás siRNS kezelés mellékhatásainak vizsgálata állatmodellekben
Mindezek mellett kísérletünkben a szisztémás siRNS kezelés utáni mellékhatásokat is vizsgáltuk, beleértve az interferon választ is. Később beszámoltak arról, hogy a 19 nukleotid hosszúságú módosítatlan siRNS-ek dózisfüggően indukálhatnak IFNα és TNFα termelést perifériás vér mononukleáris sejtvonalakban (PBMC) [217]. El kell ismerni, az ellenkező állítás is megjelent; amely szerint a kémiailag szintetizált siRNS-ek nem indukáltak IFN-termelést, míg az in vitro (plazmidokkal) átírt siRNS-ek igen [218].
Wesche-Soldato és munkatársai nem találtak szignifikáns növekedést az IFNa és IL-6 szintjében Fas és kaszpáz-8 elleni siRNS-ek szisztémás beadása után [219]. Mindezek tudatában saját kísérletünkben a kis térfogatú hidrodinamikusan beadott siRNS-ek által kiváltott interferonválaszt vizsgáltuk egerekben. A szisztémás gyulladásos marker, a TNFα szintje kísérleteinkben nem mutatott emelkedést a szisztémás siRNS kezelés után, ami azt bizonyítja, hogy az siRNS-ek AVHDI-ja nem vált ki szisztémás gyulladásos választ in vivo.
Heidel és munkatársai kimutatták, hogy a csupasz siRNS-ek egyszeri nagy mennyiségű (2,5 mg/kg) beadása után az IFNα és az IL-12 plazmaszintje nem emelkedett szignifikánsan a polyI:C-vel kezelt pozitív kontrollcsoporthoz képest, ami hiányra utal. interferonválasz [220]. Mivel Sioud et al. leírták, hogy az siRNS-ek komplexképződése fokozhatja a gyulladásos citokinek termelődését (jelentős IL-6 termelést figyeltek meg 6 órával az siRNS kationos liposzóma farokvéna kezelés után [221]), továbbra is előnyben részesítjük a csupasz siRNS-ek használatát. Így nem/nagyon valószínűtlen, hogy az in vivo beadott csupasz siRNS-ek IFN-választ váltanak ki, de maga a hidrodinamikus injekció kismértékben növelheti az ISG expresszióját.
Az intravénás immunglobulin szisztémás lupus erythematodesre kifejtett
Kísérletünkben arra törekedtünk, hogy az IVIG kezelést a betegség legkorábbi megjelenése előtt, illetve visszafordíthatatlan szervkárosodás (bőrhegesedés vagy vesekárosodás) előtt kezdjük meg. Eredményeink azt mutatták, hogy a lupus nephritis lefolyását és súlyosságát a hosszú távú IVIG-kezelés nem befolyásolta: a vér karbamid-nitrogénszintje és a vesekárosodás szöveti előfordulási gyakorisága nem mutatott szignifikáns különbséget az IVIG-vel és fiziológiás sóoldattal kezelt állatoknál. Komplement-3 immunhisztokémiai reakciónk azt mutatta, hogy az IVIG kezelés hatására a bőrben szignifikánsan csökkent a komplement-3 pozitív erek száma a fiziológiás sóoldattal kezelt kontroll csoporthoz képest.
Munkánkhoz hasonlóan Gaedicke [232] és Ballow [233] is kimutatta, hogy az IVIG kezelés enyhíti a lupus bőrmegnyilvánulásait. Annak ellenére, hogy a nagy dózisú IVIG-kezelést most újra alkalmazzák terápiás szerként a szisztémás lupus erythematosusban, az IVIG jótékony hatásai mögött meghúzódó mechanizmusok még mindig nem tisztázottak. Feltételezik, hogy az IVIG telíti az Fc receptorokat, ami az endogén autoantitestek fokozott kiürülését eredményezi [241].
Az IVIG azonban köztudottan modulálja a komplementaktivitást: a nagy dózisú IVIG mind in vitro, mind in vivo megköti a C3a-t és a C5a-t a folyadékfázisban [245], és verseng a születőben lévő C3b-ért [246]. Mindezek alapján megállapítható, hogy egérmodellünkben a humán IVIG kezelés nem befolyásolta az autoantitestek mért értékeit, az IVIG kezelés bőrre gyakorolt jótékony hatását pedig a komplement kötődése okozta. Munkacsoportunk a jövőben mélyebben kívánja vizsgálni az IVIG hatásait, különösen a betegség kezdete után, egér IVIG segítségével.
AZ ÉRTEKEZÉS ÚJ EREDMÉNYEI, KÖVETKEZTETÉSEK
Immunmoduláló és komplement-gátló hatása miatt az IVIG-et korábban szisztémás lupus erythematosusban (SLE) próbálták ki, de az IVIG-stabilizáló cukorkomponensek jelenléte által okozott ozmotikus tubulusok károsodása miatt egyes betegeknél a lupus nephritis progresszióját figyelték meg. , így az IVIG kezelést tilos volt. A már elérhető, nem cukorral stabilizált IVIG elérhetősége az SLE IVIG-terápia újraértelmezését késztette. Kísérletünkben felmértük a nagy dózisú, hosszú távú glicinnel stabilizált IVIG-kezelés hatásait a humán SLE egérmodelljén.
Az MRL/lpr egereket glicinnel stabilizált IVIG-vel vagy sóoldattal (0,2 ml/10 g) kezeltük hetente egyszer 6 hetes és 5 hónapos koruk között. Amikor az állatokat leölték (tehát már makroszkóposak), azt találtuk, hogy az IVIG enyhítette a lupus bőrön való megjelenését. A szövettani értékelés során szignifikáns különbséget figyeltünk meg az IVIG-vel és a fiziológiás sóoldattal kezelt állatok között.
Nem tapasztaltunk változást a vese érintettségében az IVIG kezelés hatására. A glicin stabilizált IVIG kezelés során nem figyeltük meg a tipikus ún Adataink azt mutatják, hogy az IVIG enyhítette a bőr lupust anélkül, hogy vese mellékhatásokat okozott volna.
ÖSSZEFOGLALÁS
SUMMARY
168 Winder A, Molad Y, Ostfeld I, Kenet G, Pinkhas J, Sidi Y: Treatment of systemic lupus erythematosus with prolonged administration of high-dose intravenous immunoglobulin: report of 2 cases. 170 Corvetta A, Della Bitta R, Gabrielli A, Spaeth PJ, Denieli G: Use of high-dose intravenous immunoglobulin in systemic lupus erythematosus: report of three cases. 171 Lafferty TE, Smith JB, Schuster SJ, DeHoratius RJ: Treatment of acquired factor VIII inhibitor with intravenous immunoglobulin in two patients with systemic lupus erythematosus.
172 Sherer Y, Levy Y, Langevitz P, Lorber M, Fabrizzi F, Shoelfeld Y: Successful treatment of systemic lupus erythematosus cerebritis with intravenous immunoglobulin. 173 Boletis JN, Ioannidis JPA, Boki KA, Moutsopoulos HM: Intravenous immunoglobulin compared with cyclophosphamide for proliferative lupus nephritis. 176 Monova D, Belovezhdov N, Altunkova I, Monov S: Intravenous immunoglobulin G in the treatment of patents with chronic glomerulonephritis: clinical experience lasting 15 years.
180 Sati HIA, Ahya R, Watson HG: Incidence and associations of acute renal failure complicating high-dose intravenous immunoglobulin therapy. 224 Boletis JN, Ioannidis JPA, Boki KA, Moutsoppulos HM: Intravenous immunoglobulin compared with cyclophosphamide for proliferative lupus nephritis. 229 Metallidis S, Papaioannu M, Bokolas G, Kollaras P, Gogou V, Nikolaidis P: Acute renal failure after intravenous immunoglobulin therapy in HIV-infected patient.
SAJÁT PUBLIKÁCIÓK JEGYZÉKE
KÖSZÖNETVNYILVÁNÍTÁS

![3. táblázat: A különböző helyre, magas nyomással beadott fluoreszcens siRNS-ek felvételi helyei [ 71 ]](https://thumb-eu.123doks.com/thumbv2/9dokorg/19335863.0/18.892.117.773.621.941/táblázat-különböző-helyre-nyomással-beadott-fluoreszcens-felvételi-helyei.webp)