1. Bevezetés
A kritikus ponthoz közel az anyagok különleges tulajdonságokkal rendelkeznek, amely felhasználható arra, hogy eddig nem létezõ termékeket alkossunk meg, vagy hatékonyabban végezhessünk el egy elválasztási vagy szintetikus feladatot, esetleg csökkentsük a szerves oldószer felhasználást.1 A kritikus pont (nyomás és/vagy hõmérséklet) alatt szubkritikus, míg felett szuperkritikus állapotról beszélünk. Alkalmazás szempontjából a szubkritikus folyadékok és a szuperkritikus fluidumok a jelentõsek, mert ezek viszonylag nagy sûrûsége számottevõ oldóképességgel jár együtt, a hagyományos folyadékokhoz viszonyítva viszkozitásuk viszonylag alacsony és a diffúzió gyors. Mindezek elõnyösek az anyagátbocsátási folyamatok esetében.
Oldószerként a víz, az etanol és a szén-dioxid iparágtól függetlenül korlátozás nélkül alkalmazható. A szén-dioxid azonban az elsõ kettõvel szemben csak atmoszférikusnál nagyobb nyomáson képes jelentõs mennyiségû anyagot oldani, oldószerként jellemzõen szuperkritikus állapotban használják. Ökölszabályként elfogadható, hogy ekkor is apoláris, mérsékelt molekulatömegû komponensek oldódnak jól szén-dioxidban2, bár vannak kivételek, mint pl.
a fluorozott3 polimerek. Az etanolt elterjedten használják adalékoldószerként a szén-dioxid polaritásának növelésére, extrakciós technikáknál max. 15 %-ban.4 Szuperkritikus fluidum kromatográfia mozgófázisaként rendszeresen valójában szubkritikus elegyet használnak, a szén-dioxid módosítójaként nem csak az etanol, hanem szinte bármilyen jellemzõ kromatográfiás oldószer alkalmazott. A szub- és szuperkritikus víz alkalmazásai az utóbbi évtizedben egyre intenzívebben kutatott területekké váltak, a részleges és teljes oxidációtól5 a biomassza cseppfolyósításon vagy elgázosításon6, az extrakción7 keresztül a nanoméretû fémoxidok8 folyamatos elõállításáig számos területen bizonyult hatékonynak. Egyéb szub- és szuperkritikus oldószereket alkalmaznak az olajiparban9 (C3-C5 frakciók) vagy a polimeriparban10-11 (monomerek és elegyeik) egy-egy célfeladat megoldására, de ezek nem tekinthetõek általánosan elterjedtnek.
A Budapesti Mûszaki és Gazdaságtudományi Egyetem (BME) Vegyipari Mûveletek majd Kémiai és Környezeti Folyamatmérnöki Tanszékén 1986 óta a szuperkritikus fluidumokhoz kapcsolódóan folyamatosan aktív kutató-fejlesztõ munka zajlik, amit több mint negyed évszázadon keresztül Simándi Béla professzor neve
fémjelzett. Tanítványaiként törekszünk arra, hogy új lehetõségeken és új megoldások alkalmazásával mutassuk be a szuperkritikus oldószerek sokoldalúságát, valamint az új megoldásokon felül az ok-okozati összefüggéseket is felderítsük.
A nyomás alatti rendszerek alkalmazása akkor lehet gazdaságos és célszerû, ha egyértelmû, jól meghatározható elõnye van az atmoszférikus alternatívával szemben, amennyiben ilyen létezik. Ez az elõnye, a teljesség igénye nélkül, lehet jelentõsen megnövekedett reakciósebesség, kiemelkedõ szelektivitás, új és más módon nem elõállítható termék pl. kompozit vagy kontrollált szemcseméret eloszlás, illetve kisebb környezetterhelés vagy energiaigény. Jelen cikk célja, hogy bemutassa a BME Nagynyomású oldószerek kutatócsoportban az elmúlt öt évben vizsgált legfontosabb területeket, egy-egy érdekesebb példával illusztrálva, és ezzel felkeltse az olvasó érdeklõdését a szub- és szuperkritikus oldószerek alkalmazásában rejlõ lehetõségek és tudományos kihívások iránt.
2. Oldhatóság, sûrûség, olvadáspont csökkenés és viszkozitás mérése nyomás alatt és az eredmények matematikai leírása
Bármely fejlesztés, kutatás megkezdésének, a kísérletek megtervezésének alapvetõ kérdése az, hogy ismertek-e a vizsgált rendszer fizikai-kémiai jellemzõi. Ismert-e egy adott komponens vagy elegy oldhatósága a nyomás és hõmérséklet valamint elegyoldószer esetén a segédoldószer mennyiségének függvényében? Mivel az irodalomban ezek az adatok gyakran nem lelhetõek fel, eddig a szuperkritikus szén-dioxidban és segédoldószerekkel való elegyeiben való oldhatóság, az oldatsûrûség, és -viszkozitás mérésére valamint az esetleges olvadáspont csökkenés megfigyelésére dolgozunk ki mérési technikákat.
2.1. Oldhatóság
Az oldhatóságot statikus illetve dinamikus módszerrel is meg lehet mérni. Dinamikus módszer esetén a szilárd anyagot egy oszlopba töltjük bele, majd ezen az ágyon keresztül állandó nyomáson és hõmérsékleten, kis térfogatárammal áramoltatjuk át a szuperkritikus szén-dioxidot. Az oldószer tömegárama nyomás alatt mérhetõ, a kioldott anyagmennyiséget nyomáscsökkentés és csapdázás után határozzuk meg. A gyakorlatban elsõsorban gyengén oldódó vegyületek oldhatóságnak meghatározására alkalmas. Statikus módszer esetén a mérést egy változtatható térfogatú nagynyomású látóüveges cellában végezzük. A
DOI: 10.24100/MKF.2018.01.78
Hatékonyságnövelés szub- és szuperkritikus oldószerekkel
SZÉKELY Edit
a*aBudapesti Mûszaki és Gazdaságtudományi Egyetem, Kémiai és Környezeti Folyamatmérnöki Tanszék, Mûegyetem rkp. 3., 1111 Budapest, Magyarország
* Tel.:+3614632202 fax:+3614633197; e-mail: sz-edit@mail.bme.hu
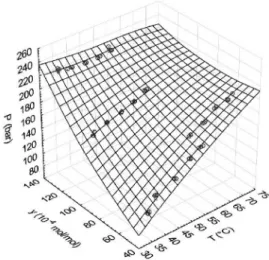
térfogat változtatásával egy adott koncentrációjú oldat opálosodási és kitisztulási nyomása határozható meg állandó hõmérsékleten. Szintén a statikus módszer egy válfaja, amikor egymással egyensúlyban levõ folyadék és fluid fázist hozunk létre a változtatható térfogatú berendezésben, majd mindkét fázisból állandó nyomáson és hõmérsékleten mintát veszünk, amelyek koncentrációját független analitikai módszerrel meghatározzuk. Az 1. ábrán példaként egy prótikus ionos folyadék a di-2-etilhexil-ammónium- 2-etilhexanoát oldhatósága12 látható szén-dioxidban. A felület fölött homogén fluid fázis, a felület alatti körülmények esetében két egyensúlyi fázis alakul ki. Az ábrán látható kis móltört értékek átszámolva azt jelentik, hogy a vegyületnek megfelelõ nyomás és hõmérséklet mellett (pl. 22 MPa 55 °C) 10 tömeg% feletti oldhatósága van. Az eredmény azért meglepõ, mert az ionos folyadékokat a szakirodalom szén-dioxidban oldhatatlannak tekinti.
1. ábra. Szén-dioxid – di-2-etilhexil-ammónium-2-etilhexanoát elegy opálosodási nyomása az ionos folyadék móltört és a hõmérséklet függvényében.
2.2. Sûrûség és viszkozitás
Az elegyek viszkozitásának és sûrûségének az ismerete az elméletin felül gyakorlati szempontból is fontos, hiszen az alapvetõ mûvelettani számításokhoz, egy technológia szimulációjához ezek az adatok szükségesek. A szakirodalomban még a sûrûség esetén is többnyire a tiszta oldószer sûrûségével becslik az elegy összetétel-, nyomás- és hõmérsékletfüggõ sûrûségét, de a szuperkritikus elegyek, oldatok viszkozitásáról elvétve található csak információ.
Kialakítottunk ezért a változtatható térfogatú látóüveges cellához csatlakoztatható nagynyomású esõtestes viszkozimétert. A 2. ábrán a relatív sûrûség, ami az oldat mért sûrûségének és az azonos nyomáson és hõmérsékleten mért tiszta szén-dioxid sûrûségnek a hányadosa, látható a szén-dioxid móltört és a nyomás függvényében szén-dioxid – diaceton-alkohol elegy13 esetében. A diagramon érdemes megfigyelni, hogy a szén-dioxid kritikus nyomásához (7,36 MPa) közel már kis mennyiségû oldott anyagnak is jelentõs hatása lehet a sûrûségre, valamint az oldott anyag-tartalom növekedésével, azaz a szén-dioxid móltört csökkenésével az eltérés jelentõssé válik, az oldat sûrûség többszöröse is lehet a tiszta szén-dioxid sûrûségének.
2. ábra. Diaceton-alkohol – szén-dioxid elegy relatív sûrûsége a szén-dioxid móltört és a nyomás függvényében (változó hõmérséklet mellett)
Az oldatsûrûség mérése lehetõséget teremt arra, hogy az elegyedési moltérfogatot számítani lehessen. Így a sûrûségméréstõl független oldhatósági adatok alapján állapotegyenletek (pl. Peng-Robinson) kölcsönhatási paramétereinek illesztése után a számított és a mért sûrûségértékek összehasonlítása ellenõrzésre ad lehetõséget.
Az oldhatóság matematikai leírása, a szükséges pontossággal, akár empirikus egyenletekkel, de még inkább állapotegyenletekkel lehetõséget teremt arra, hogy professzionális folyamatszimulátorban pl. egy szuperkritikus fluidum extrakció leírható legyen.
2.3. Olvadáspont-csökkenés
Bizonyos anyagok, elsõsorban polimerek és ionos folyadékok olvadáspontja jelentõsen lecsökkenhet szén-dioxid nyomás hatására, aminek oka a szén-dioxid nagymértékû beoldódása a szilárd fázisba. Az olvadáspont-csökkenés valamint a beoldódó szén-dioxid hatására bekövetkezõ viszkozitás csökkenés többek között az oka, hogy az ionos folyadékok és a szuperkritikus szén-dioxid rendszert sokféle feladatra alkalmasnak vélik.
Az olvadáspont-csökkenés jelensége elõnyös a mikronizálásra és kompozitok elõállítására alkalmas PGSS14 (particles from gas saturated solutions) eljárás során is.
3. Reakciók és elválasztómûveletek szén-dioxidban illetve vízben
3.1. Reakciók
A szuperkritikus szén-dioxid alkalmazásának legfontosabb elõnye az alacsony hõmérséklet (min. 31 °C) és mérsékelt nyomás (min. 7,4 MPa), ami kíméletes reakciókörülményeket tesz lehetõvé. Emellett a szén-dioxid ilyen körülmények között inertnek tekinthetõ. Ezzel szemben a szub- és szuperkritikus víz (Tkrit 374 °C, Pkrit 22 MPa) reakcióképes közeg. Az alábbiakban ezzel a két oldószerrel segédoldószerek alkalmazása nélkül elért legújabb eredményeinkbõl mutatok be néhányat.
3.1.1. In situ diasztereomer sóképzés szuperkritikus szén-dioxidban
A Simándi és Fogassy professzorok és munkatársaik által kidolgozott szuperkritikus extrakción alapuló rezolválási eljárás15 alapvetõ feltételezése az volt, hogy a szuperkritikus extrakció szerepe az oldhatatlan diasztereomer só és az elreagálatlan, szén-dioxidban oldható enantiomerkeverék elválasztása. A másfél évtizedes szisztematikus kutatás azonban rávilágított, hogy az elválasztó lépés nyomása és hõmérséklete jelentõsen befolyásolhatja a rezolválás eredményességét.16 A tapasztalatok áttekintése után arra következtettünk, hogy a reakciók egyensúlyi állapota eltérõ, mint a vákuumbepárlással elállított rendszer összetétele.
Más szóval a diasztereomer sóképzési reakció lejátszódhat szuperkritikus szén-dioxid oldószerben is. A különbözõ rendszereken17-20 végzett részletes vizsgálatokból arra következtetésre jutottunk, hogy ha az egyik reagens jól oldódik szén-dioxidban (>1 tömeg%) a másik akárcsak kismértékben, de kimutathatóan oldódik (>0,05 tömeg%) akkor a diasztereomer sóképzési reakció lejátszódik, bár ettõl még nem szükségszerûen enantioszelektív.
Amennyiben az egyik reagens oldhatatlanak tekinthetõ, akkor a reakció megvalósítható idõtartományon belül (<1 hét) nem játszódik le jó konverzióval. Ha mindkét komponens jól oldódik, a reakció rövid idõ alatt (<1 óra) teljes konverziót is elérhet, egyéb esetben több napot vagy hetet is igénybe vehet.
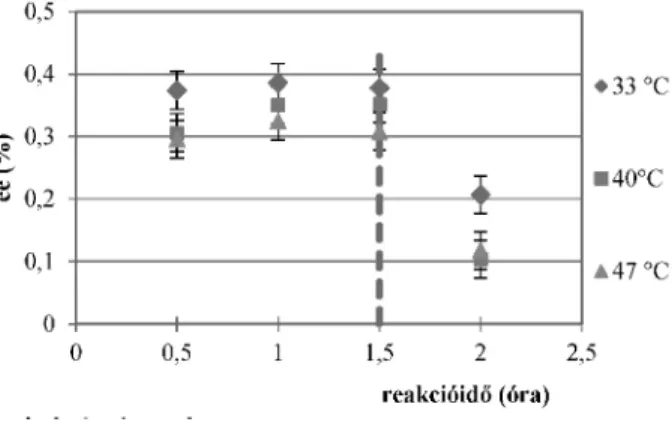
3. ábra. A fluid fázis enantiomer tisztasága cisz-krizantémsav (S)-2- benzilamino-1-butanollal szén-dioxidban végzett in situ rezolválásakor 12,5 MPa nyomáson. Kék függõleges vonal az extrakciós mosás kezdetét jelzi.
Az in situ kristályosításon alapuló rezolválás hatékonyságához azonban nem csak a reakció lejátszódása szükséges, hanem az is, hogy az ezt követõ extrakciós lépés során a diasztereomer kellõképpen stabil legyen. A 3. ábra a cisz-krizantémsav szén-dioxid oldószerben végzett rezolválása esetén mutatja a fluid fázisban mérhetõ enantiomer tisztaságot az idõ függvényében a reakció alatt, illetve a mosási szakasz után.20 Mind a racém vegyület, mind a rezolválószer megfelelõen oldódik a szén-dioxid fázisban, ezért már az elsõ mintavételezés jó enantiomer tisztaságot mutat a fluid fázisban, amibõl következik, hogy enantioszelektív diasztereomer sókiválás történt. A hõmérséklet emelése a diasztereomer só disszociációját elõsegíti, így alacsonyabb fluidfázisbeli enantiomer
tisztaságot eredményez. Látható, hogy a mosás során a diasztereomer só disszociál, ezzel a rezolválás hatékonysága leromlik.
A nyomás növelésével párhuzamosan a fluid fázis sûrûsége és így oldóképessége nõ, ami a cisz-krizantémsav rezolválása esetén nem kedvezõ.
Ezzel szemben például az ibuprofen – R-feniletán-1-amin in situ sóképzése17 20 MPa nyomáson 40-50 °C hõmérsékleten 70-80%-os enantiomer tisztaság mellett kiváló rezolválást tesz lehetõvé, míg 10 MPa nyomáson csak 30% enantiomer tisztaság érhetõ el. A nyomás emelése a reakciósebességet és az egyensúlyi enantiomer tisztaságot egyaránt növeli.
3.1.2. Enzimkatalizált kinetikus rezolválás szuper- kritikus szén-dioxidban
Bizonyos enzimek és enzimkészítmények, elsõsorban a lipázok, megõrzik aktivitásukat szuperkritikus szén-dioxid oldószerben is. Még a lipázok is érzékenyek azonban a nem optimális víztartalomra, vagy a nyomás hirtelen változására.
Éppen ezért az enzimkatalizált reakciót akkor érdemes szuperkritikus szén-dioxidban végezni, ha:
• Lényegesen nagyobb reakciósebesség érhetõ el,
• kiemelkedõ szelektivitás,
• vagy a reakció és a termék-szubsztrát elválasztás összekapcsolása lehetséges és hatékony.
Az elmúlt idõszakban elsõsorban a harmadik területtel, a reakció és a nyomáscsökkentésen alapuló enzim – visszamaradó szubsztrát – termékelválasztással foglalkoztunk. Minden mintapélda esetén rendkívül szelektív és gyors volt az enzimkatalízis, a kihívást az elválasztási lépés reakcióhoz való kapcsolása jelentette.
Abban az esetben például, ha egy szén-dioxidban oldható szubsztrátból oldhatatlan termék keletkezik (pl. aminosav), akkor a reakció után a visszamaradó szubsztrát szén-dioxidos extrakcióval elválasztható, majd az enzimkészítmény felületérõl az aminosav vizes mosással eltávolítható.21 Észterezési reakciók esetén az észterezõ ágens szénlánchosszának optimális megválasztásával nem csak a reakció szelektivitása és sebessége maximalizálható, hanem a termék és a szubsztrát oldhatóság különbsége is megnövelhetõ és így az elválasztás frakcionált nyomáscsökkentéssel lehetõvé válik.22
3.1.3. Részleges oxidáció szuperkritikus vízben A szuperkritikus vizes oxidációt (SCWO) rendszeresen alkalmazzák nehezen vagy csak kockázatosan kezelhetõ ipari szennyvizek kezelésére, mert rövid átlagos tartózkodási idõ mellett (másodperc – perc nagyságrend) teljes bomlás érhetõ el. A rövid szükséges átlagos tartózkodási idõ oka az anyagátbocsátási ellenállás hiánya, hiszen a szuperkritikus víz és az oxigén (levegõ) egymással korlátlanul elegyednek.
Hátrány jelent a nagyfokú korróziós kockázat valamint a nagy nyomás. A SCWO az átlagos tartózkodási idõ vagy az oxigén mennyiségének szabályozásával részlegesen is végrehajtható, amit szintetikus vagy regenerálási célra fel lehet esetleg használni.23 Saját munkánkban összeállítottunk
egy folyamatos részleges szuperkritikus vizes oxidációs berendezést, amelyen elért eredményeket egy tesztrendszeren, a toluol benzoesavvá történõ részleges oxidációjának mintapéldáján mutatom be az 4. ábrán.
A 4. ábra a konverzió és a termelés a 4,7 másodperces átlagos tartózkodási idõ mellett (kb. 48% konverzió, 20% termelés,) azonos napon mért mérések eredményétõl való eltérését mutatja be. Látható, hogy a növekvõ átlagos tartózkodási idõ a konverzió növekedését, de a termelés csökkenését eredményezi, azaz a benzoesav is továbboxidálódik a reakciókörülmények között. Mivel a SCWO rendkívül gyors reakció, a részleges oxidációhoz nagyon precízen, tizedmásodperces nagyságrendben kell szabályozni az átlagos tartózkodási idõt. Ugyanez lehet a módszer elõnye is, hiszen nagy termékmennyiség elõállításához is kis reaktortérfogatok szükségesek.
4. ábra. Az átlagos tartózkodási idõ hatása részleges szuperkritikus vizes oxidáció esetén (körülmények: 400 °C, 30 MPa, 1,5-szeres oxidálószer felesleg) 24
3.1.4. Biomassza bontás szubkritikus vízben
A 3.1.3. alpontban röviden bemutatott részleges szuperkritikus vizes oxidációval megegyezõ körülmények között, de oxigén kizárása mellett végezhetõ biomassza elgázosítás metán vagy hidrogén termelési céllal, illetve ennél kisebb nyomáson (<20 MPa) és alacsonyabb hõmérsékleten (200-350 °C) a biomassza vagy egyéb hulladékok elfolyósítása lehetséges.25 Saját eredményeink szerint 20-40 perc reakcióidõ mellett mezõgazdasági hulladékból akár 40-50 tömeg% bio-olaj is elõállítható.
3.2. Egyéb diffúziókontrollált folyamatok
A szub- és szuperkritikus fluidumok egyik legfontosabb elõnye, hogy a diffúzió ezekben az oldószerekben nagyságrendekkel gyorsabb, mint folyadékokban. Az alábbiakban néhány speciális alkalmazást mutatok be, amely ezt a tulajdonságot használja fel.
3.2.1. Aerogélek
Az aerogélek, akár szilika akár szén aerogélekre gondolunk, elõállításának fontos lépése a polikondenzáció vizes közegben, majd az azt követõ oldószercsere után a pórusokat kitöltõ vizes oldószer lecserélése levegõre úgy, hogy a folyamat közben sosem keletkezik fázishatárfelület a pórusok belsejében. A tématerület László Krisztina professzor (BME) aerogél kutatásaihoz kapcsolódik. A megfelelõ gélszerkezet elõállításának kritikus lépése a
szárítás, ahol a nagynyomású szén-dioxidos extrakció szükséges. Alapvetõen három eljárás létezik:
1. Magát a pórusokat kitöltõ oldószert hevíteni nyomás alatt a kritikus pontja fölé, majd ezt kicserélni nyomás alatt levegõre, ezután csökkenteni a nyomást. Ez a módszer a jellemzõ oldószerek (víz, etanol, metanol, aceton) magas kritikus hõmérséklete miatt általában nem célszerû.
2. A pórusokban levõ a vizet teljesen lecserélni szerves oldószerre, majd a szerves oldószert nyomás alatt folyadék halmazállapotú szén-dioxidra. Amikor már szinte csak folyadék szén-dioxid tölti ki a pórusokat, akkor felmelegíteni (nyomás alatt) a szén-dioxid kritikus pontja fölé a rendszert, majd ezen a hõmérsékleten lecsökkenteni a nyomást.
3. A szén-dioxid kritikus pontjánál magasabb hõmérsékleten szuperkritikus szén-dioxidos extrakcióval elvégezni az oldószercserét, majd állandó hõmérsékleten a nyomás- csökkentést.
Azt tapasztaltuk, hogy a 3. módszer teszi lehetõvé a gélek leggyorsabb szárítását, a legkisebb zsugorodás mellett, aminek az oka az, hogy a szerves oldószer szén-dioxidra való kicserélõdése gyorsabban játszódik le a gyorsabb diffúzió miatt, mint a 2. esetben.26
3.2.2. Szén nanocsövek
A szén nanocsövekbe a kis méretû apoláris üregük miatt nehéz molekulákat belejuttatni. Mivel ez a tér eredendõen nem keverhetõ, a diffúzió lesz a meghatározó a folyamatban.
Kamarás Katalin professzor (MTA Wigner FK SZFI) kutatócsoportjával együttmûködésben alkalmas módszert dolgoztunk ki arra, hogy különbözõ anyagokat (pl.
fullerén27, koronén28, lumineszcens komplex29) a szuperkritikus szén-dioxid diffúziós folyamatokat elõsegítõ tulajdonságát kihasználva a nanocsövek belsejébe rövid idõ alatt bejuttassunk. A módszer érdekessége, hogy ezen anyagok egyike sem oldódik kimutatható mértékben szuperkritikus szén-dioxidban.
3.2.3. Impregnálás
A nanocsöveknél és az aerogéleknél elért sikerek, valamint az irodalomban megtalálható aerogélek, textilek, faanyagok polimerek sikeres impregnálási alkalmazásai arra sarkalltak, hogy polimerek alacsony hõmérsékletû festésénél30 is vizsgáljuk meg a szén-dioxid alkalmazhatóságát. A polimeriparban a szuperkritikus szén-dioxidot a polimerizációs reakció oldószereként, lágyítószerként, habosításra használják.11
Az 5. ábrán szén-dioxidban ditizonnal színezett polikarbonát gyöngyök láthatóak. Látható, hogy az impregnálás idõigényes folyamat. A színintenzitás nõ a növekvõ idõvel.
Ahogy az 5. ábrán is látható, kis mennyiségû segédoldószer alkalmazása is jelentõsen befolyásolhatja egy adott folyamat végeredményét, többnyire az oldhatóságot módosító hatásán keresztül. A festék oldhatóságának növelésével (nyomás növelés, segédoldószer alkalmazása a színezés gyorsul, de hosszabb érintkezési idõnél a polimerhez való affinitás a meghatározó.
5. ábra. Ditizonnal színezett polikarbonát gyöngyök31
4. Elegyoldószerek alkalmazása
4.1. Növényi hatóanyagok kinyerése segédoldószerrel Világszinten ma már sok száz üzemi méretû extrakciós berendezés üzemel. Bizonyos esetekben azonban, mint pl. ha a célunk alkaloidok kinyerése, a szén-dioxid oldóképessége nem elegendõen nagy, legalábbis a szokásos 50 MPa alatti nyomástartományban. Az oldhatóság és az extrakciós sebesség növelésére a segédoldószerek alkalmazása kínál megoldást. Segédoldószerként vizet, etanolt használnak leggyakrabban, mi is ezeket használjuk. Az utóbbi években az érdeklõdésünk középpontjába atmoszférikus és nagynyomású kivonási módszerek kombinációja került, aminek célja egy alapanyagból több különbözõ hatású kivonat elõállítása, ami hatékonyabb alapanyag felhasználást tesz lehetõvé.32,33 A módszer kivonatok frakcionálására is alkalmas. Mintapéldaként a macskakaromra kidolgozott két megoldás sematikus vázlata látható a 6. ábrán. A növény alkaloidjainak immunerõsítõ és antivirális hatást tulajdonítanak. A csersavban dús frakció elegendõen nagy koncentrációjú, hogy alkalmas természetes bõrcserzõszernek.34
6. ábra. Macskakarom kéreg frakcionálása szuperkritikus (SFE) segédoldószeres és atmoszférikus extrakciós technikák kombinálásával.
4.2. Antiszolvens frakcionálás
Az antiszolvens eljárások elve éppen ellentétes a segédoldószer alkalmazásával. Itt a szerves oldószer jó oldószere a komponenseknek, amelyeket a szén-dioxid, mint anitszolvens hozzáadásával csapunk ki. A technikát finom porok elõállítására, mikronizálásra használják. Antiszolvens frakcionálásról akkor beszélünk, amikor a kicsapás mellett
bizonyos komponensek oldatban maradnak és a kicsapást követõ extrakciós lépés során eltávolítjuk az értékesebb komponensek mellõl, így egy lépésben jelentõs mértékben tisztul is a termék.
4.2.1. Kivonatok finomítása
Természetes kivonatok, növényi extraktumok rendkívül sok komponensbõl állnak. Ezek jellemzõen lekvár vagy zselé állagú, nehezen kezelhetõ, többnyire sötét színû ún.
szárazextraktok, amelyeket felhasználás elõtt a legtöbb esetben további feldolgozási, tisztítási lépéseknek kell alávetni.
7. ábra. Fekete nadálytõ kivonat antiszolvens frakcionálása35
A feladat megoldására bizonyos esetekben, elsõsorban poláris oldószerekkel magasabb hõmérsékleten (célszerûen rövid kontaktidõ mellett) elõállított oldatok esetében, az oldószer bepárlása utáni további hagyományos finomítási lépések helyett az azonnali szén-dioxidos antiszolvent frakcionálás alkalmas lehet. A 7. ábrán fekete nadálytõ antiszolvens frakcionálásnak eredményei láthatóak. A cél porszerû, homogén jól adagolható és kezelhetõ kivonat elõállítása, nagy allantointartalommal.
4.2.2. Rezolválás
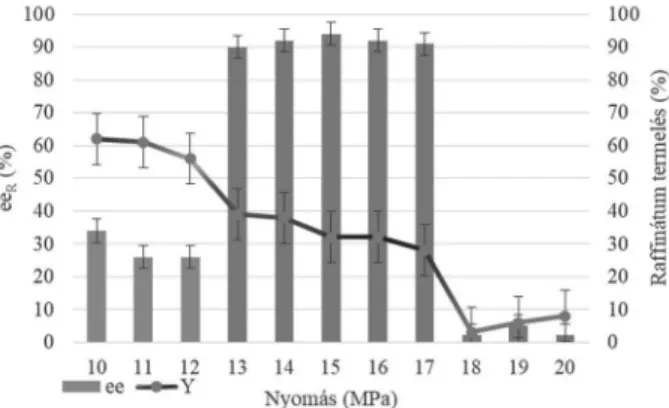
Az antiszolvens frakcionálás alkalmas diasztereomer sóképzésen alapuló rezolválásra is. Más jellegû vegyületeknél alkalmas azonban, mint a csak szén-dioxidot alkalmazó eljárások. Míg a csak szén-dioxidos módszerek csak apoláris racém vegyületek esetén alkalmasak, és primer aminok esetén az alkalmazásuk nem célszerû, az antiszolvens eljárásnak nincsenek ilyen korlátjai. Azonban az antiszolvens módszerhez a diasztereomer sónak sokkal stabilabbank kell lennie, eddig még diasztereomer komplexek esetén nem sikerült alkalmaznunk. A módszer széles mólaránytartományban használható, és a nyomás, hõmérséklet és szerves oldószer / szén-dioxid arány is befolyásolja a rezolválhatóságot a legtöbb esetben. Cisz-permetrinsav (R)-feniletán-1-aminnal36 való antiszolvens rezolválása esetén (8. ábra) 40 °C hõmérsékleten kiemelkedõ enantiomer tisztaságot (ee) értünk el 13-17 MPa között. 17 MPa felett gyakorlatilag nem képzõdött szilárd fázis így enantiomer megkülönböztetés sem lehetett, míg 13 MPa alatt racém diasztereomer só vált ki nagy mennyiségben, eltérõ kristályszerkezetben, mint a középsõ nyomástartományban.
A módszer alkalmazható enantiomerkeverékek továbbtisztítására is, akár a diasztereomer sók
átkristályosításával, akár szén-dioxidban gyengén oldódó enantiomer keverékek esetén közvetlenül is.37
8. ábra. Cisz-permetrinsav (R)-feniletán-1-aminnal való antiszolvens rezolválása esetén a nyomás hatása az enantiomer tisztaságra és a termelésre.
Joggal vetõdik fel azonban az a kérdés, hogy mi az elõnye a nagynyomású antiszolvens frakcionálásnak vagy kristályosításnak az atmoszférikus átkristályosításhoz képest. Amellett, ami az általános tulajdonsága a szub- és szuperkritikus oldószereknek, azaz a nyomással, hõmérséklettel és összetétellel széles határok között változtatható oldóképesség és mint bemutattam a szelektivitás is, az antiszolvens eljárás esetén a kicsapás pillanatszerû.
5. Összefoglalás
A szub- és szuperkritikus oldószerek közös elõnyös tulajdonságai a nyomással, hõmérséklettel és segédoldószer alkalmazása esetén a segédoldószer mennyiségével széles tartományban szabályozottan változtatható sûrûség, oldóképesség. A gyors diffúzió miatt az anyagátbocsátási folyamatok gyorsabbak, mint folyadékokban. A BME Kémiai és Környezeti Folyamatmérnöki Tanszékén a több, mint 30 éves múltra visszatekintõ kutatócsoport elmúlt öt évének munkáiból mutat be mintapéldákat a közlemény a reakcióktól a rezolváláson, extrakción, impregnáláson át az antiszolvens frakcionálásig. A kutatások célja olyan környezetkímélõ, hatékony módszerek és megoldások kifejlesztése az elméleti háttér megértéséhez szükséges alapmérési módszerek kidolgozásától a valós problémák megoldásáig, amely a nagynyomású oldószerek speciális elõnyeit felhasználja.
Köszönetnyilvánítás
A megfogalmazott összegzõ, átfogó értékelések nem születhettek volna meg a kutatócsoport tagjainak áldozatos munkája nélkül. Külön köszönet illeti a hivatkozott saját közlemények összes társszerzõjét valamint a munkát támogató cégeket és szervezeteket (jelenleg OTKA K108979). Ezúton is szeretném kifejezni személyes hálámat és nagyrabecsülésemet Simándi Béla és Fogassy Elemér professzorok iránt, akik a szuperkritikus szén-dioxidban végzett rezolválás kutatásában világszinten elsõk voltak.
Hivatkozások
1. Simándi, B.; Sawinsky, J. Olaj Szappan Kozmetika 1996, 45, 3-11.
2. Székely, E.; Mucsina, G.; Tokai, Zs.; Dudás, J.; Vágó, Á.;
Kalocsai, P.; Törõ, M.; Simándi, B. Szuperkritikus Oldószerek Mûveleti és Analitikai Alkalmazása, Budapest, Magyarország, 2012.05.24. p. 18.
3. Wood, C. D.; Yarbrough, J. C.; Roberts, G.; DeSimone, J.
M. In Supercritical carbon dioxide in polymer reaction engineering; Kemmere, M. F.; Meyer, T. (eds) Wiley-VCH Verlag GmbH., Weinheim 2005.
4. Bertucco, A.; Vetter, G. (eds.), High Pressure Process Technology: Fundamentals and Applications, Amsterdam:
Elsevier, 2001.
5. Marrone, P. A. J. of Supercrit. Fluids 2013, 79, 283-288.
https://doi.org/10.1016/j.supflu.2012.12.020
6. Pavloviè, I.; Knez, Ž.; Škerget, M. J. Agric. Food Chem.
2013, 61, 8003-8025.
https://doi.org/10.1021/jf401008a
7. Gbashi, S.; Adebo, O. A.; Piater, L.; Madala, N. A.; Njobeh, P. B. Sep. Pur. Reviews 2017, 46, 21-34.
https://doi.org/10.1080/15422119.2016.1170035 8. Gruar, R. I.; Tighe, C. J.; Southern, P.; Pankhurst, Q. A.;
Darr, J. A. Ind. Eng. Chem. Res. 2015, 54, 7436-7451.
https://doi.org/10.1021/acs.iecr.5b01817
9. Meyers R. A., Handbook of Petroleum Refining Processes, McGraw-Hill Education 2016.
10. Kemmere, M. F.; Meyer, T. (eds.), Supercritical carbon dioxide in polymer reaction engineering, Wiley-VCH Verlag GmbH., Weinheim 2005.
https://doi.org/10.1002/3527606726
11. Saldivar-Guerra, E.; Vivaldo-Lima, E. Handbook of Polymer Synthesis, Characterization, and Processing, John Wiley & Sons, Hoboken, New Jersey, 2013.
https://doi.org/10.1002/9781118480793
12. Péter-Szabó, B.; Kelemen, Zs.; Dudás, J.; Nyulászi, L.;
Székely, E. Szuperkritikus oldószerek analitikai és mûveleti alkalmazása konferencia. 2015.05.21 p. 37.
13. Lévai, Gy. Dipomamunka, BME, 2013
14. Weidner, E. J. of Supercritical Fluids 2009, 47, 556–565.
https://doi.org/10.1016/j.supflu.2008.11.009
15. Fogassy, E.; Simándi, B.; Ács, M.; Szili, T.; Deák, A.;
Kemény, S.; Sawinsky, J.; Manczinger, J.; Benkéné Lõdy, I.; Varga, K.; Lantos, B. MSZ 212905, 1993.
16. Simándi, B. MTA doktori értekezés, Budapest, 2007.
17. Bánsághi, Gy.; Szekely, E.; Sevillano, D.M.; Juvancz, Z.;
Simandi, B. J. of Supercritical Fluids 2012, 69, 113-116.
https://doi.org/10.1016/j.supflu.2012.05.016
18. Lõrincz, L.; Sohajda, T.; Székely, E. Mûszaki Kémiai Napok 2017: Veszprém, Magyarország,
2017.04.25-2017.04.27.
19. Varga, D.; Bánsághi, Gy.; Martínez Pérez, J. A.; Miskolczi, S.; Hegedûs, L.; Simándi, B.; Székely, E. Chem. Eng.
Technol. 2014, 37, 1885-1890.
https://doi.org/10.1002/ceat.201300720 20. Varga, D. Diplomamunka, BME, 2013.
21. Utczás, M.; Székely, E.; Tasnádi, G.; Monek, É.; Vida, L.;
Forró, E.; Fülöp, F.; Simándi, B. J. Supercritical Fluids 2011, 55, 1019-1022.
https://doi.org/10.1016/j.supflu.2010.10.024
22. Varga, Zs.; Kmecz, I.; Székely, E. 16th European Meeting on Supercritical Fluids, Lisbon, Portugália,
2017.04.25-2017.04.27. p. 118.
The subcritical and supercritical solvents, also called pressurized solvents, are known for their well controllable solvent properties by modifying pressure, temperature and in case of using a mixed solvent by composition as well. One of the major strength of these solvents compared to traditional liquids is the fast diffusion resulting in reduced mass transfer limitation. Our research group at the Department of Chemical and Environmental Process Engineering of Budapest University of Technology and Economics (BME) was established in 1986 and it is dedicated to demonstrate novel application possibilities of pressurized solvents. Our research aims to develop efficient, environmentally benign processes including development of experimental techniques to better understand fundamentals if needed and solving real problems of industry as well. This paper presents some interesting topics and results from our work in the last five years from chemical reactions through optical resolution, extraction, impregnation to antisolvent fractionation to engage the reader with the beauty of the pressurized solvent research field.
Measurement and modelling of solubility, viscosity, density, melting point depression
Before any experimental research could be planned, we need information on the phase equilibrium and on the properties of the phases involved. However, solubilities of even single compounds in pressurized fluids often cannot be found in the literature and that of mixtures is almost never described detailed enough. Thus we developed and validated own dynamic and static solubility measurement techniques for solutes of low and good solubilites as well. In Fig 1. the temperature and composition dependent cloud point pressures are plotted of a protic ionic liquid (IL). We observed upto 10 mass% solubility of the IL in supercritical carbon dioxide, while ILs are in principle regarded as being non-soluble in carbon dioxide. Density and viscosity of a
pressurized solution are often estimated by the known pressure and temperature dependent density and viscosity of the solvent. By systematic measurement of the two properties of solutions, large deviations were found, and example is presented in Fig. 2 for diacetone alcohol – CO2 mixture. An interesting phenomenon is also the melting point depression in presence of carbon dioxide, which can be observed in a view cell.
Applications
Reactions, formulations, extractions were developed in pure pressurized (sub- or supercritical) water and carbon dioxide and in mixtures of carbon dioxide with organic solvents.
Enantioselective enzyme catalyzed kinetic resolutions21-22 and partial diastereomeric salt formation based optical resolutions17-20 are possible and in some cases are efficient in supercritical carbon dioxide. While enantioselectivities and reaction rate might be increased by working at the optimal operational parameters, the major advantage of allying supercritical fluids is the possibility of coupling the reaction with a selective separation as supercritical fluid extraction followed by sequential pressure drop based recovery of the solutes.
Sub- and supercritical water is a useful solvent for fast complete or selective degradation. Supercritical water oxidation is applied for solving difficult waste water purification problems, while partial supercritical water oxidation might lead the degradation intermediers within a seconds’ scale average residence time. By excluding oxygen, under supercritical conditions the hydrothermal gasfication, while under subcritical conditions the hydrothermal liquefaction are promising techniques for biomass based biogas or bio-oil production.
23. Garcia-Verdugo, E.; Fraga-Dubreuil, J.; Hamley, P. A.;
Thomas, W. B.; Whiston, K.; Poliakoff M. Green Chem.
2005, 7, 294–300. https://doi.org/10.1039/b419098j 24. Tárkányi, M., Diplomamunka, BME, 2016.
25. Tekin, K.; Karagoz, S.; Bektao, S. Renewable and Sustainable Energy Reviews 2014, 40, 673–687.
https://doi.org/10.1016/j.rser.2014.07.216
26. Czakkel, O.; Székely, E.; Koczka, B.; Geissler, E.; László, K. Microporous Mesoporous Mater. 2012, 148, 34-42.
https://doi.org/10.1016/j.micromeso.2011.07.008
27. Botos. Á.; Khlobystov, A.N.; Botka, B.; Hackl, R.; Székely, E.; Simándi, B.; Kamarás, K. Phys Status Solidi B 2010, 247, 2743-2745. https://doi.org/10.1002/pssb.201000375 28. Botka, B.; Füstös, M.E.; Klupp, G.; Kocsis, D.; Székely, E.;
Utczás, M.; Simándi, B.; Botos, Á.; Hackl, R.; Kamarás, K.
Phys Status Solidi B. 2012, 249, 2432-2435.
https://doi.org/10.1002/pssb.201200349
29. Maggini, L.; Füstös, M-E.; Chamberlain, T.W.; Cebrián, C.;
Natali, M.; Pietraszkiewicz, M.; Pietraszkiewicz, O.;
Székely, E.; Kamarás, K.; De Cola, L.; Khlobystov, A.N.;
Bonifazi, D. Nanoscale 2014, 6, 2887-2894.
https://doi.org/10.1039/c3nr05876j
30. Varga, D.; Alkin, S.; Gluschitz, P.; Péter-Szabó, B.;
Székely, E.; Gamse, T. J. Supercritical Fluids 2016, 116, 111-116. https://doi.org/10.1016/j.supflu.2016.05.018 31. Kótai, A., Diplomamunka, BME, 2017.
32. Calvo, A.; Morante, J.; Plánder, Sz.; Székely, E. Acta Aliment. Hung. 2017, 46, 27-34.
https://doi.org/10.1556/066.2017.46.1.4
33. Calvo, A.; Dévényi, D.; Kószó, B.; Sanz, S.; Oelbermann, A. L.; Maier, M.; Keve, T.; Komka, K.; Gamse, T.;
Weidner, E.; Székely, E. J. Supercritical Fluids 2017, 125, 50-55. https://doi.org/10.1016/j.supflu.2017.01.018
34. Maier, M.; Oelbermann, A. L.; Renner, M.; Weidner, E. Ind.
Crops Prod. 2017, 99, 19-26.
https://doi.org/10.1016/j.indcrop.2017.01.033 35. Czeczon, Zs., Szakdolgozat, BME, 2017.
36. Bánsághi, Gy.; Lõrincz, L.; Szilágyi, I.M.; Madarász, J.;
Székely, E. Chem. Eng. Technol. 2014, 37, 1417-1421.
https://doi.org/10.1002/ceat.201300718
37. Kõrösi, M.; Madarász, J.; Sohajda, T.; Székely, E.; 16th European Meeting on Supercritical Fluids Lisbon, Portugália, 2017.04.25-2017.04.27. p. 81.
Increasing efficiency with sub- and supercritical solvents
Diffusion controlled processes can be efficiently enhanced by using supercritical fluids. Enzymatic catalysis also sees its benefits, but various impregnations from polymers30-31 (Fig. 5.) to carbon nanotubes27-29, solvent exchange within porous structures as aerogels26 can also become possible if supercritical fluids, mainly carbon dioxide is used to accelerate diffusion within the solid phase.
A supercritical or subcritical fluid, being a non-polar solvent, is often not sufficient alone to obtain the desired separation.
Cosolvents (alcohols, esthers, ketones, water etc.) applied as minor additives enhance the dissolving power of the solvent significantly. On the other hand this may lead in meantime to reduced selectivity.
From a single plant several different bioactive fractions32-33 might be obtained by fine-tuned extractions in series. For example from cat’s claw bark a fraction rich in pentacyclic alcaloids supposed to have immune stimulant and antiviral effects and a fraction rich in tannin applicable in low environmental impact tanning of leather can be obtained by the combination of supercritical carbon dioxide extraction with ethanol cosolvent and hydroalcoholic extraction.
Antisolvent precipitation or fractionation also uses mixtures of an organic and a supercritical solvent, but the main aim is to instantaneously decrease the dissolving power of the organic solvent by adding the antisolvent. Carbon dioxide, either liquid of supercritical is a suitable antisolvent, because it is very well soluble in most of the organic solvents, and above a certain pressure it is typically already completely miscible.
Dry extracts obtained from plants, either obtained by conventional solvent extraction, pressurized liquid extraction or supercritical fluid extraction, are typically gelly, difficult to handle. Antisolvent fractionation of the extract with pressurized carbon dioxide as antisolvent may lead to selective precipitation of the required compounds in a powder form (Fig 7.)
Antisolvent fractionation can also be efficiently applied for selective precipitation of diastereomeric salts. It was found, that while typically the organic solvent to carbon dioxide ratio plays the major role regarding selectivity of the precipitation, in certain cases pressure influences so significantly the solubility and dissociation of the two different diastereomeric salts that it is possible the maximize the difference resulting in outstanding enantioselectivity.36 Furthermore, antisolvent fractionation is also a viable tool of enantiomeric enrichment either by recrystallization of diastereomeric salts, or by selective precipitation of enantiomeric mixture.37
While the purpose of this paper and of especially this English summary was to draw the attention of the reader of the various fields where sub and supercritical fluid might be the best choice, I would like to thank here also all coauthors of the common papers referred their enthusiastic work in this field, all our former and current sponsors from industry and public bodies for believing in this field, and the pioneers of diastereomeric salt based enantioseparation with supercritical extraction, Prof. Simándi and Prof. Fogassy, for being as great persons and researchers as they always have been.