FIZIKAI-KÉMIAI VIZSGÁLATOK A BÁZIKUS MARTINSALAK FeO-TARTALMÁNAK A FÉMFÜRDÖ KÉNTELENlTÉSÉRE
GYAKOROLT HATÁSÁRÓL
SZŰCS LÁSZLÓ
Az acélgyártási szaklapok cikkei az acélfürdő kéntelenedésének vizsgálatai kapcsán igen megoszló véleményeket közölnek a bázikus salak FeO-t arta lmána k a f ür d ő kéntelenítésére gyakorolt hatásáról.
J. Mocek [1] például azt állítja, hogy azok a kutatók, akik az acél kéntelenítését a
[ Fe S ]^ ; F eS ) (1)
reakció szerint képzelik el, a kéntelenítés befolyását függet lennek t a r t j á k a salak FeO-tartalmától, ha a koncentráció 10—25 mólszázalék között van.
J. Chipman és N. J. Grant [2] szerint a salakban levő FeO 3—80% kö- zött nincs hatással a kéntelenítésre. A hatás csak akkor mutatkozik, ha a F eO-tartalom 1% alá süllyed.
Sz. L. Levin [3] véleménye szerint 5—7% FeO-tartalomnál nagyobb FeO-koncentráció má r nincs hatással a kénmegoszlásra.
K. G. Speith [5] CaO-val nem telített salakokra nézve azt találta, hogy változatlan FeO-tartalom és növekvő bázicitás az acél kéntel eníté- sére kedvezőbb feltételeket terem t. Telített salakok esetében mindaddig, amíg a FeO-tartalom el nem éri a 22,5%-ot, nem állapítható meg a F e O befolyása.
Mint látható, a fenti vélemények — noha sok t ekintet ben el té rn ek egymástól — abban megegyeznek, hogy a kis FeO-tartalom kedvező h a - tással van az acélgyártás kénmegoszlására. Ezt a kérdést a következők- ben több oldalról vizsgáljuk meg.
Köztudomású, hogy a bázikus martinsalakok fő alkotó oxidjai a CaO, MgO, MnO, FeO, P2O5 és SÍO2, Grum—Grzs imajló szerint az ilyen össze- tételű salakokban az FeO 5—40% mennyiségben fordulhat elő. A salakok kémiai összetételére vonatkozó vizsgálatok azt mutatták, hogy a bázikus eljárás esetében a salak és az acélfürdő kölcsönhatása következtében
a salak legfontosabb alkotójának, az FeO-nak mennyisége — azonos hőmérsékleten — kizárólagosan a fürdő karbontartalmának (C%) és a salak bázicitásának:
C a O % SÍO2% + P2O5
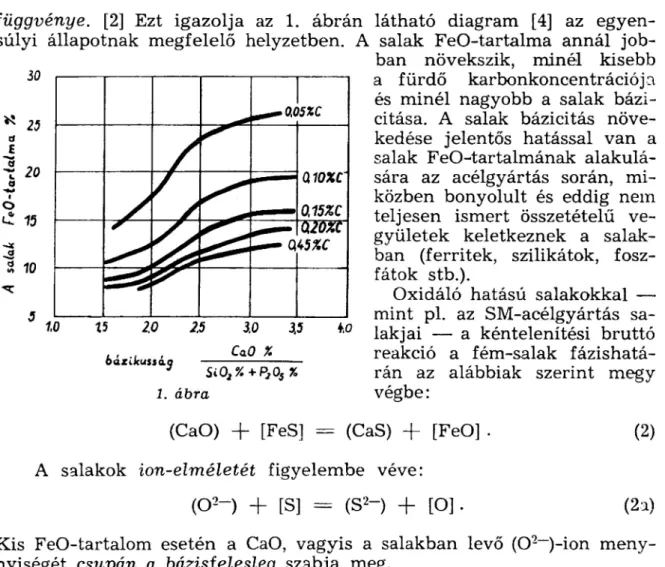
függvénye. [2] Ezt i gaz ol ja az 1. á b r á n lát hat ó di agram [4] az egyen- súlyi állapotnak m egf el e lő hel yzetben. A salak F e O-t ar t al m a a nn ál job- ba n növekszik, mi né l kisebb
i 0 1 a f ü r d ő ka rbonkoncentráci ój a
és m i nél nagyobb a salak bázi- citása. A salak bázicitás növe- kedése jelentős hatással v an a salak Fe O- t a rt al m á nak ala kul á- sára az acélgyártás során, mi- közben bonyolult és eddig nem 15 y — / % t e l j e s e n ismert összetételű ve-
gyül et ek keletkeznek a salak- ban (ferritek, szilikátok, fosz- fátok stb.).
Oxidáló hatású salakokkal — mint pl. az SM-acélgyártás sa- l akjai — a kéntelenítési br u t t ó reakció a fém-s ala k fázi s hat á- SíOj'á+PjOs r, rán az alábbiak szerint meg y
1. ábra végbe:
* 25
a £
1 20
3 10
^0-0,L •5XC
Q10XC'
0.15ZC Q10XC'
0.15ZC
,
MC ÜMXC1,0 15 2,0
bázikussá.g
2.5 3,0 CaO X
3,5 ¥.0
(CaO) + [FeS] = (CaS) - f [FeO] . A salakok ion-elméletét f ig ye lem b e véve:
( 02~ ) + [S] = (S2 _) + [O].
(2)
(2a) Kis Fe O- tar t al om esetén a CaO, vagyis a s al akban levő (02~)-ion m e n y - n y i s é g é t csupán a bázisfelesleg s z a b j a m e g .
K = (S2-) • [O]
(2b) [S] • (O2-)
melyből a ké n megoszlási koefficiense a következőképpen szám ít ható ki:
(S2-) = (P2-)
[
;sf ' IO]
Ha a f ür d ő be n oldott ox i g é n arányos a salakban oldott FeO m enn yi s égé - vel, akkor a kén megoszlási koefficiense ki fejez het ő az [O] = k • (FeO) behelyettesítésé vel :
(S2-) (O2-)
= k' - . (3)
[S] (FeO)
Azonos bázicitás esetén az (O2 -) koncentrációja állandó, ezért a 3. egyen- let logaritmikus alakban a követ kezőképpen í rható f el :
(s
2-)
lg = lg K
S] lg (FeO%) . (3a)
Ez az összefüggés bizonyítja annak a felt ételezésnek a helyességét, hogy Í5Z FeO mennyisége a salakba n befolyásolja a kénmegoszl ás értékét. Ez a törvényszerűség viszont a kutatások szerint [2] csak 1 % FeO-tartalomig
érvényes.
Lényeges továbbá fi gyelembe venn i a következő megál lapításokat:
1. Ha az FeO- tar tal om 1% aíá csökken, akkor az növeli a ké nm eg - oszlási együtt hatót (3a egyenlet).
2. Logaritmikus dia gra mban az 1 % FeO-tart alom alatt a kénmegoszlási
r(S%) koefficiens
100
a .
egyenesen arányos az FeO mol % - o s mennyis égével (2. áb- ra). Ez azt jelenti, hogy az FeE mól % növekedésével a ké nm e g- oszlási koefficiens ért éke állan- dóan csökkenő tendenciát m u - t a t . Fizikai-kémia a l a p o n h a - sonló e r e d m é n y r e j ut o t t ak más kutat ók is [6], akik az előbbi r e a k c i ó r a — „nem ionos" e l m é - leti alapon — az alábbi módon írták fel a tömeghat ás tör vé - nyét :
K (FeO) • (CaS)
(CaO) • [FeS] (4)
0.05 ai mol Z(FeO)-
2. ábra
K = [S]
(S)
mely (feltételezve, hogy a salak összes k ént a rt a l m a CaS, az acé- lé pedig Fe S alakban kötött);, felírható így is:
(CaO) (FeO) * Ebből:
(S)
[S] = K (FeO)
(CaO) (5 y
A kapott összefüggésből az alábbi következtetések vonhatók le:
1. Az (S)/[S] viszony annál nagyobb — vagyis a kéntelenítés annál teljesebb — minél kisebb a salak FeO-t artalma.
2. Ha azt akarnók, ho gy az oldható szulfidok t el jese n CaS-dá alakul- j a n a k át, vagyis a F eS é r t é k e null a felé t en dá l jo n a fém fázi sban, akkor a (4) egyenlet a l ap já n két f el tét el nek kell ki elégülnie:
2.1. a C aO - t a r t a l om na k m axi má l i s nak kell lennie,
2.2. az F e O- t a r t a l m a t m inimálisra kell visszaszorítani a salakban.
Ez a megállapítás bizonyos m é r t é k be n ma gy ará zat o t ad arra, hogy m ié rt é r h e t ü n k el n a g y f o k ú ként el enítést a nagyol vasztóban vagy elektro- kemencében. E m e eljárás ok redu kál ó at mo s z f ér áj á ba n a következő r ea k - ciók me nne k végbe:
[FeS] - f (CaO) + [C] = [Fe] + (CaS) + ICO} (nagyolvasztó) (6) [FeS] + (CaC2) + 2 (FeO) = (CaS) + 3 [Fe] + 2{COS(elektrokemence)(7)
Míg a n ye rs v a s g yá r t á s ko r vagy elekt roacél gyártáskor n agy fokú k é n - telenítést é r h e t ü n k el, addig a Ma rt i n- kem e nc e oxidáló a t m os z f é r áj á b an a kéntelenítés csak az i s m er t m é r v ű lehet, és na g y m é r t é k b e n függ a t ü - zelőanyagok k é n t a r t a l m á t ó l is.
Az FeO szerepe ne m cs a k a fizikai kémia módszereivel m u t a t h a t ó ki,
h a n e m gyakorlati kísérletekkel i s.
F. Harders [6] és mások kísérletei is a l át á m as z t j á k az elméleti ere d- m ény eke t. Ezt a kísérletsorozatot tükrözi a 3. ábra, ahol az látszik, hogy
a z F e O f i g y e l e m b e v é t e l e m i a t t kisebb az üzemi adatok szóródása. A
(S) • (FeO) (CaO)
ér t ékek ne k f üg gv ény é be n való ábrázolásánál jól lá t-
[S] I S i o J
szik ez a te ndencia — vagyis a koordi náta pontok t öm örül ése — ha ug yanezt az összefüggést (FeO) t ar t al om nél kül vizsgál juk a bázicitás f üg g v é ny é b e n (4. ábra).
Az előzők szerint a salak kéntelenítő h at ását úgy k épzel het j ük el, hogy a f é m be n oldott F e S először a salakba megy át. A salakba kerülő és a f ém ben m a r a d ó F e S me nnyi sé gének a viszonyát, am i nt az előzőek- ből t u dj uk , a megoszlási állandó ért éke (L) határozza meg. Eszerint
[FeS]
L = (9)
(FeS)
Ha feltételezzük, hogy az acélban az összes k én ferroszulfid alakjá ban va n jelen, akkor í rh a t j u k , hogy
(FeS) (FeS)
L = - = 0 , 3 6 —— .
8 8 [ vSl ( 1 0 )
32
A salakba jutott FeS az ott t alálható fém oxi dokkal a következő egyen- le te k szerint lép reakcióba:
320
280
IkQ 200
r^ 160
1 20
40
1 1 I 1
+ = Kíséríeíi Sorozat 1
O , _ U _ _ 7 o
—/» — 3
° 0 y
• /
0 o
o /1 4,
<:!
/
/
• /
/ /
/ • o / /
•
/ / /
/ /
/ ' • t • •
•
/ / / /
/ /
*2
/
/
/ / Az 0 gok remi (/őráhotá
öda-i / ra
l / + / o
Az 0 gok remi
(/őrá
hotá
öda-i
ra
1,0 1,5 20 25 3,0 35 4.0 4.3
(Cap)
íSi02)
3. ábra
32,0
28,0
24, 0
20.0
16,0
12,0
8.0
yo
1 1 l + =» Kij^rfeti. sorozat 1
o = — ' — —"— 2
1
• -
r U
- 3
•
/.
•/ . /. » / *
/ /.
• • • // <
/ .
/ o ' o o •
/
<
/
* /
/
0
»00
o 0
/ / /
/
• / /
/ /
/ y a
/
O/U 4"
/ / / s o • V
%0 1,5 2,0 2.5 3.0 3.5 k0 SiO, CaO
4. ábra
( M n O ) + (FeS) ^ (FeO) + (MnS) (CaO) + (FeS) - (FeO) + (CaS) . Elképzelhető még a m agnézi um kéntelenítő hatása is:
(MgO) + (FeS) ^ (FeO) + (MgS).
(11)
( 1 2)
(13) Ezen reakciónak az egyensúlyi állandói a kénmegoszlási koefficienst is figyel em be véve a következők:
K,, =
K,
K1 3 =
(Feo) (MnS) (MnO) [2-S]
(FeO) (CaS) (CaO) [IS]
(FeO) (MgS) (MgO) [2S]
(14)
(15)
(16)
A salakok elemzésekor az összes kén t a r t al m a t meghatározzuk, ez pedig a szulfidok k én t a r t al m á v al a következő összefüggésben va n:
(2S) = 0,36 (FeS) + 0,37 (MnS) + 0 , 4 4 (CaS) + 0,57 (MgS) * (17) Ila ebbe az egyenletbe a fémszulfi dkoncentrációknak a megoszlási ál- landókból, illetőleg az egyens úlyi állandókból ki fej ezhető értékeit b e - hel yettesí t jük, akkor k a p j u k , hogy:
(MnO) (CaO)
(2S) = L + [2'S] + 0,37 • Kl t - - - — - [2B] + 0,44 Kl 2 [2"S] +
(FeO) (FeO)
(MgO)
- f O , 5 7 K1 3 [2S] (18)
(FeO) ebből:
y ^ = L + [K'i (MnO) + K'2 (CaO) + K'3 (MgO)] . (19) E^bben az egyenletben
K'i = 0,37 . K h K<2 = 0,44 . Kj2
K '3 = 0,57 • K1 3. (20)
Az elméleti fizikai-kémiai vizsgálatok tehát egyért el műe n bizonyít- ják, hogy az acélfürdő er edm énye s kéntelenítés éhez elengedhetetl enül szükséges, hogy a F eO -t a rt a l om minél kisebb legyen.
A kérdés további vizsgálatát termodinamikai számításokkal kí ván om megvilágítani.
Az alapreakció s é m á j a :
F e S + CaO ^ CaS + FeO (21)
A [7] és [8] adatai a l a p j á n a fenti vegyületek zfG°i527 0 C értékei a kö - vetkezők:
FeS : zlG°1 5 2 7 °c = —15 790 cal/mól, CaO : AG° 1 5 2 7 °c = —112 100 cal/mól,
CaS : /ÍG°1 5 2 7 o c = —98 705 cal/mól,
FeO : z!G° 1 5 2 7 °c = —36 000 cal/mól. (22) A bizonyítás pontosságáért érdemes a (21) reakciót az alsó nyíl i r á n y á- ba n vizsgálni, vagyis azt, hog y az FeO képes-e reakcióba lépni a CaS-dal
és így annak kéntelenítő hat ását meggátolni. A számítások szerint:
AGS = (AG°FeS + AG"CaC) (/íG°CaS + AG° Feo) AGV° = ( — 15 790 — 11 2 100) — ( — 98 7 0 5 — 3 6 0 00 )
AGV° = + 6 8 1 5 cal/mól (23)
A te rm odinami ka i norm ál potenciál pozitív értéke azt jelenti, hogy az alapreakció az alsó nyíl i r ányá b an nem játszódhat le.
Noha a ter m odi na mi ka i no rm á l potenciál (/1G°) f e nt számított értékei
kémiailag tiszta vegyületekre vonatkoznak (22), a n n y i m é g i s m e g á l l a p í t -
ható, hogy a fenti reakció (21) az alsó nyíl i r á n y á ba n nem játszódhat le.
Ezért az is feltételezhető, hogy az FeO-val telíte tt bázikus sal akban az;
F e O negatív — azaz ként elenítést visszaszorító — ha tása nem érvénye-
sülhet.
Termodinamikai számításokkal is ú j a b b adat ot szerezt ünk te hát a ké rdés eldöntéséhez. Enne k ala pj án joggal feltételezhető, hogy a salak átlagos FeO mennyis é ge (10—25%) a S—M-acél ként el ení tés ének fo lya- m a t á r a nincs káros hatással.
1400 1388 ^
A Fe O- ta rt al mú salak ként e- lenítő hat ás ának tárgyal ásakor n e m hagyható fi geyl me n kívül
a FeO—FeS összetett rendszer
egyensúlyi viszonyainak t ár - gyalása sem. Az 5. ábrából [9]
leolvasható, hogy a két vegyü - let (FeO és FeS) kb. 40 súly- százalék F eO -t art a lomn ál 940 C°-on olvadó e nt ekt i kum ot képez (B) és fol yé kony halmaz- állapotban k orlátl anul oldódik egymás ban (I. sz. terület). így az acélgyártás közepes h őm ér - sékleten (1527 Cc) a magas FeO me nnyis ég a ként ele ní tés re k ü -
lönösebb pozitív hat ás t ne m 0
gyakorolhat. TeS
Az eddigiek kiegészítéseként, n é h á n y kutatási e r e d m é n y [10]
.alapján képl et szerűen kí váno m dok ument ál ni megoszlási viszonyszámra:
1200 ws-
1100 1000
900
800
1.
y4
/ \
IILD
8
!
v.3
20 40 60 EO 100
FeO
5. ábra
1. H. Schenk (1934)
(S) _ (CaO) 1 [S] ~~ (FeO) K
a FeO hatását a (S)/[SJ
(24)
ahol: (CaO) = „szabad" mé sz ta rt al om súly % - b a n . (FeO) = ,,szabad" F e O- t a rt a l om súly % - b a n .
2. L. S. Darken és B. M. harsén (1 9 4 2) :
CaO
FeO - + C [Mn%] (23)
ahol: Ng = a salakban levő mólok összege A, B és C = kísérletileg kapott állandók.
3. F . Harders, H. Grewe és W. Oelsen ( 195 1)
1 (26)
[S] (FeO)
Ezek utá n legyen szabad l evonni a szükséges végkövetkeztetéseket : 1. Számítások (fizikai-kémiai és termodinami kai) azt igazolják, hogy
a S i e m e n s — M a r t i n - s a l a k F e O - t a r t a l m a nem minden összetételnél hatás- talan a k é n t e l e n í t é s r e .
2. Valószínű, hogy a kis F e O - t a r t a l m a k (0—1%-ig) bí rna k jelentő- sebb befolyással a ként el e nít é sr e (3a. összefüggés).
3. A jó ként elenít és érdekébe n a salaknak minimális Fe O- tar t a l om
m e l l e t t nagyfokú bázicitással kell rendelkeznie.
Ezekben k í v á n t a m összefoglalni irodalmi kut atá sai m és t e rm o di na - mikai számításaim e r e d m é n y e k é n t adódó következtet éseimet a bázikus sal akban levő F e O- na k a S—M-acélgyártás ként elenítő f ol ya m at ár a gya- korolt hatásáról.
[1] J. Mocek. Huth. Listy. (1959) 5. pp. 405—409.
[2] ,J. Chi pman. La M e ta ll ur gi a Itialiana. 1952. 44. k. 10 pp 502—511.
[3] A. J. Oszipov. V. F. Szuvorov, L. A. S w a r c m a n Szovremenei P r o bl e m ü Metal- lurgii Moszkva. 1958. pp: 369—379.
[4] T rubin—Oj ks z: Acélkohászat Moszkva, 1954.
[5] K. G. S pei th: Der derzeitige S t a n d der Metaillurgie des S—M ve rf a hr ens . Berg- u n d H ü t t e nm á n n i s c h e Mona ts ch eft e 5. sz. 94—1020. 108. évf.
[6] Harde rs. Grewe, Oelsen, Stahl u n d Eisen 1951. szept. 13. 937—986.
[7] S. Si mon F rau Gy. Benkő. Acta Techn ik a 44. 1964.
[8] W. Liange: Die t he r m o d i na m i s c he n Eigenschaften der Metalloxide.
[9] Kerpely—Hajtó.—Horváth: Va skohászat i folya matok és fizikai ké m i á j u k . Bu - dapest, 1953.
[10] Die neue Hütt e 1955. I. szám.
I R O D A L O M