Válasz Dr. Haracska Lajos bírálói véleményére
Köszönöm a bírálónak dolgozatom gondos és precíz bírálatát. A bírálatban feltett kérdések a dolgozatban tárgyalt problémák további alapos végiggondolására ösztönöztek, és a közeljövőre tervezett munkáinkhoz is hasznos kiindulópontokat adtak. A feltett kérdésekre adott válaszaim a következők:
1. A miozinra mért kinetikai paramétereket mennyire befolyásolhatják a reakciókörülmények, pl. ionerősség vagy pH. Ezzel kapcsolatban felvetődik az a kérdés is, hogy mennyire összehasonlíthatóak a különböző miozin formák kinetikai paraméterei, ha azokat nem teljesen azonos kísérleti körülmények között állapították meg – mint pl. az 1-es táblázatban közöltek, amelyek egy része támaszkodik csak saját mérésekre, míg a többi az irodalomból nyert érték.
Az 1-2. táblázatokban közölt, saját és más laborokban meghatározott adatok a tudományterületen kialakult általános konszenzusnak megfelelő mérési körülmények között kerültek meghatározásra 25°C-on, pH 7-en, 75-125 mM ionerősségű oldatban. E konszenzus az élettani körülmények lehetőség szerinti reprodukálása, illetve az izolált fehérjék stabilitása által diktált gyakorlati szempontok nyomán alakult ki. A 14. cikkünkben közölt temperature- jump/stopped-flow módszer alkalmas humán enzimek 37°C-on történő vizsgálatára is, a humán miozinok ilyen körülmények között történő átfogó jellemzése azonban még nem történt meg.
A miozinok ismertetett nagyfokú funkcionális és biokémiai változatossága ellenére – érdekes módon – a kinetikai ciklus egyes részlépései jellegzetesen hasonló függést mutatnak a különböző izoenzimek esetében. Erre példaként hozható az aktin-affinitás jelentős ionerősség- függése, főleg az ún. gyenge aktinkötő (miozin.ATP, illetve miozin.ADP.Pi) állapotokban.
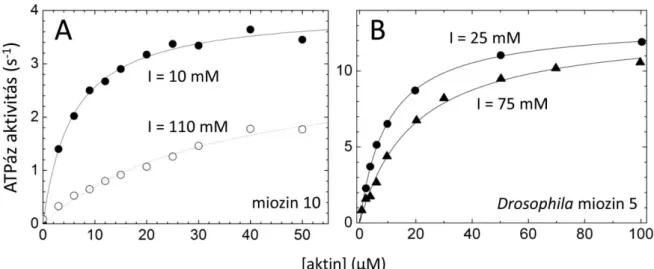
Ennek jellegzetes következménye, hogy a miozin steady-state ATPázának aktin-aktiválására jellemző, félmaximális aktiválást előidéző aktin-koncentráció (KATPáz) értéke jelentősen nő az ionerő növekedésével, míg a maximális aktivitás nem vagy jóval kisebb mértékben változik.
Ennek példáját mutatja két különböző miozin esetén az alábbi 1. ábra, amelynek adatai a 7.
EÖTVÖS LORÁND TUDOMÁNYEGYETEM TERMÉSZETTUDOMÁNYI KAR
BIOKÉMIAI TANSZÉK
1. ábra: Szarvasmarha miozin 10 (A) és Drosophila melanogaster miozin 5 (B) szubfragmentum-1 konstrukciók steady-state ATPáz aktivitásának aktin-aktivációja különböző ionerősségű (I) oldatban (25°C, pH 7).
Hiperbolikus illesztéssel kapott maximális aktivitás (kcat) és KATPáz értékek: miozin 10: 4,0 s-1 és 5,7 µM (I = 10 mM); 3,0 s-1 és 33 µM (I = 110 mM); Drosophila miozin 5: 13 s-1 és 9,9 µM (I = 25 mM), 13 s-1 és 19 µM (I
= 75 mM). (Forrás: 7. és 10. saját cikkek)
A pH jelentősen befolyásolja a miozinhoz kötötten lezajló ATP-hidrolízislépés egyensúlyi állandóját (K3 a dolgozat 16. ábráján), amire a quenched-flow mérésekben (pl. 18. ábra a dolgozatban) látható „Pi burst” amplitúdójának változásából következtethetünk. Bagshaw és Trentham úttörő cikkében (76. hivatkozás a dolgozatban) a vázizom miozin 2 hidrolízis- lépésének egyensúlyi állandója pH 8-on 9-nek adódott, míg későbbi, alacsonyabb pH-n végzett mérésekben ez az érték jóval alacsonyabbnak mutatkozott (6. saját cikkünkben például K3 = 0.35-öt határoztunk meg pH 7-en).
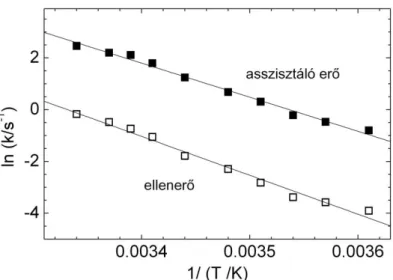
A magas terhelési arányú, processzív vagy erőtartó miozinokban az aktomiozinról történő ADP-felszabadulás, amely a haladási sebesség illetve az erőtartási hatékonyság alapvető meghatározója, NM2 izoformák esetében széles ionerősség-tartományban (10-110 mM) állandó (nem publikált saját adatok). Sarlós Kata doktorandusszal a folyamat hőmérséklet- függését is megvizsgáltuk a 17. cikkünkben ismertetett módszerrel, mechanikailag terhelt NM2A fejek esetén. E nem publikált adataink (alábbi 2. ábra) azt jelzik, hogy az ADP- felszabadulási kinetika terhelés-függése kis mértékben függ a hőmérséklettől: az asszisztáló illetve ellenerő hatása alatt álló fejekről történő ADP-felszabadulási sebességi állandók hányadosa a 4°C-on tapasztalt 22-ről 26°C-on 14-re csökken, ami a fejek flexibilitásának növekedésére utal.
2. ábra: Aktin-kötött, asszisztáló illetve ellenerő hatása alatt álló NM2A fejekről történő ADP-felszabadulás sebességi állandóinak Arrhenius-ábrázolása. A folyamat látszólagos aktiválási energiája asszisztáló erő esetén 109 kJ/mol-nak, ellenerő esetén 125 kJ/mol-nak adódott. (Nem publikált saját adatok)
Általánosságban elmondható, hogy a dolgozatban hangsúlyosan tárgyalt, az egyes miozin izoformák mechanisztikus paraméterei közötti különbségek lényegesen nagyobbak, mint amit a fiziko-kémiai körülmények ésszerű mértékű változtatása okoz egy adott izoforma esetében.
Emellett számos esetben előfordult az is, hogy a mérési körülmények változtatása a működési mechanizmus valamely fontos vonását fedte fel. Ennek egyik példája, hogy a 18. cikkünkben vizsgált Dictyostelium miozin 2 mutánsokban a katalitikusan aktív konformáció kialakulásának egyensúlyi állandója az ATP-hidrolízis kémiai lépésével párhuzamos hőmérséklet-függést mutatott, ami a két folyamat kapcsoltágára világított rá. Egy másik esetben az aktinkötés során bekövetkező szerkezet-változások közötti energetikai különbségeket sikerült felfednünk különböző miozinok aktinkötésének hőmérséklet- illetve ionerősség-függésének vizsgálatával (27. cikk).
2. A dolgozatból világossá vált, hogy a miozinok aktuális élettani szerepe jól tükröződik kinetikai jellemzőikben. Felfedezhető-e hasonló kapcsolat a DNS helikázok kinetikai jellemzői és funkciói között. Ha ez még nem ismert, milyen hipotézis lehetne felállítani erre pl. egy replikációs és egy rekombinációs helikáz összehasonlítása kapcsán.
A helikázok enzimatikus sajátságai és biológiai szerepei közötti összefüggés módszeres elemzése érdekes módon még hiányzik a szakirodalomból. Harami Gábor doktorandusszal írandó tervezett összefoglaló cikkünkhöz kigyűjtöttük annak a tizenöt, változatos biológiai
két aktivitásra jellemző sebesség- és futáshossz-értékek közel megegyeznek, míg a replikációs helikázoknál a szálszétválasztásra jellemző értékek alacsonyabbak a transzlokációsaknál. Ez a viselkedés arra utal, hogy a hibajavító helikázok aktív duplex-destabilizáló mechanizmust használnak, míg a replikációs helikázok esetében a mechanizmus részben passzív sajátságokat mutat (3C ábra).
3.ábra: Helikázok biokémiai sajátságai és biológiai funkciója közötti összefüggések előzetes elemzése (publikálatlan összefoglalás). A: A kétszálú DNS-szálszétválasztás várható processzív futáshossza (Pu, bp) és a szálszétválasztási sebesség (ku, bp/s) közötti összefüggés. B: A replikálandó genom(szakasz) mérete (Leff, bp) és a szálszétválasztás várható futáshossza (Pu, bp) közötti összefüggés. C: A kétszálú DNS-szálszétválasztás és az egyszálú DNS-en történő transzlokáció kinetikai paramétereinek hányadosai közötti összefüggés a futáshossz (Pu/Pt) és a sebesség (ku/kt) összevetésével. A biológiai funkció szerinti színkód (A ábra) mindhárom panel esetén azonos. Az ábrán az alábbi helikázok adatai szerepelnek: NS3 (hepatitis C vírus), T7gp4 (T7 bakteriofág), UvrD (E. coli), PcrA (B. stearothermophilus), T4gp41 (T4 bakteriofág), TraI (E. coli), DnaB (E. coli), NPH-II (vaccinia vírus), BLM (humán), AddAB (B. fragilis), RecBCD (E. coli), RecG (E. coli), Rho (E. coli), RecQ (E.
coli), RecD2 (D. radiodurans). Források: 24. saját cikk, publikálatlan saját adatok (RecQ); illetve 111., 205-207., 211. hivatkozások a dolgozatban, valamint:
Yu J, Cheng W, Bustamante C, Oster G. Coupling translocation with nucleic acid unwinding by NS3 helicase. J Mol Biol 2010;404(3):439-455.
Rajagopal V, Gurjar M, Levin MK, Patel SS. The protease domain increases the translocation stepping efficiency of the hepatitis C virus NS3-4A helicase. J Biol Chem 2010;285(23):17821-17832.
Dumont S, Cheng W, Serebrov V, Beran RK, Tinoco I, Pyle AM, et al. RNA translocation and unwinding mechanism of HCV NS3 helicase and its coordination by ATP. Nature 2006;439(7072):105-108.
Kim DE, Narayan M, Patel SS. T7 DNA helicase: a molecular motor that processively and unidirectionally translocates along single-stranded DNA. J Mol Biol 2002;321(5):807-819.
Johnson DS, Bai L, Smith BY, Patel SS, Wang MD. Single-molecule studies reveal dynamics of DNA unwinding by the ring-shaped T7 helicase. Cell 2007;129(7):1299-1309.
Jeong YJ, Levin MK, Patel SS. The DNA-unwinding mechanism of the ring helicase of bacteriophage T7. Proc Natl Acad Sci U S A 2004;101(19):7264-7269.
Dessinges MN, Lionnet T, Xi XG, Bensimon D, Croquette V. Single-molecule assay reveals strand switching and enhanced processivity of UvrD. Proc Natl Acad Sci U S A 2004;101(17):6439-6444.
Niedziela-Majka A, Chesnik MA, Tomko EJ, Lohman TM. Bacillus stearothermophilus PcrA monomer is a single-stranded DNA translocase but not a processive helicase in vitro. J Biol Chem 2007;282(37):27076- 27085.
Slatter AF, Thomas CD, Webb MR. PcrA helicase tightly couples ATP hydrolysis to unwinding double-stranded DNA, modulated by the initiator protein for plasmid replication, RepD. Biochemistry 2009;48(27):6326- 6334.
Lionnet T, Spiering MM, Benkovic SJ, Bensimon D, Croquette V. Real-time observation of bacteriophage T4 gp41 helicase reveals an unwinding mechanism. Proc Natl Acad Sci U S A 2007;104(50):19790-19795.
Young MC, Schultz DE, Ring D, von Hippel PH. Kinetic parameters of the translocation of bacteriophage T4 gene 41 protein helicase on single-stranded DNA. J Mol Biol 1994;235(5):1447-1458.
Sikora B, Eoff RL, Matson SW, Raney KD. DNA unwinding by Escherichia coli DNA helicase I (TraI) provides evidence for a processive monomeric molecular motor. J Biol Chem 2006;281(47):36110-36116.
Ribeck N, Kaplan DL, Bruck I, Saleh OA. DnaB helicase activity is modulated by DNA geometry and force.
Biophys J 2010;99(7):2170-2179.
Galletto R, Jezewska MJ, Bujalowski W. Unzipping mechanism of the double-stranded DNA unwinding by a hexameric helicase: quantitative analysis of the rate of the dsDNA unwinding, processivity and kinetic step- size of the Escherichia coli DnaB helicase using rapid quench-flow method. J Mol Biol 2004;343(1):83-99.
Brendza KM, Cheng W, Fischer CJ, Chesnik MA, Niedziela-Majka A, Lohman TM, et al. Autoinhibition of Escherichia coli Rep monomer helicase activity by its 2B subdomain. Proc Natl Acad Sci U S A 2005;102(29):10076-10081.
Jankowsky E, Gross CH, Shuman S, Pyle AM. The DExH protein NPH-II is a processive and directional motor for unwinding RNA. Nature 2000;403(6768):447-451.
Patel SS, Donmez I. Mechanisms of helicases. J Biol Chem 2006;281(27):18265-18268.
Reuter M, Parry F, Dryden DTF, Blakely GW. Single-molecule imaging of Bacteroides fragilis AddAB reveals the highly processive translocation of a single motor helicase. Nucleic Acids Res 2010;38(11):3721-3731.
Roman LJ, Eggleston AK, Kowalczykowski SC. Processivity of the DNA helicase activity of Escherichia coli recBCD enzyme. J Biol Chem 1992;267(6):4207-4214.
Walmacq C, Rahmouni AR, Boudvillain M. Influence of substrate composition on the helicase activity of transcription termination factor Rho: reduced processivity of Rho hexamers during unwinding of RNA-DNA hybrid regions. J Mol Biol 2004;342(2):403-420.
Zhang XD, Dou SX, Xie P, Hu JS, Wang PY, Xi XG, et al. Escherichia coli RecQ is a rapid, efficient, and monomeric helicase. J Biol Chem 2006;281(18):12655-12663.
Saikrishnan K, Powell B, Cook NJ, Webb MR, Wigley DB. Mechanistic basis of 5'-3' translocation in SF1B helicases. Cell 2009;137(5):849-859.
Shadrick WR, Julin DA. Kinetics of DNA unwinding by the RecD2 helicase from Deinococcus radiodurans. J Biol Chem 2010;285(23):17292-17300.
3. Számos DNS helikáz in vivo más fehérjékkel képzett komplexben található pl. a BLM helikáz élesztő homológja az Sgs1 helikáz a Top3-val míg az Srs2 a SUMO-PCNA-vel formál komplexet. Mennyiben befolyásolhatják a helikázok fehérje-fehérje interakciói kinetikai tulajdonságaikat? Alkalmas-e a jelölt jelenlegi kísérleti rendszere az ilyen jellegű kérdések megválaszolására.
al. (2000) J. Biol. Chem. 275:23500, Harmon et al. (2001) J. Biol. Chem. 276:232). A fehérjék közötti együttműködés mechanizmusa azonban legnagyobbrészt felderítetlen.
Előzetes eredményeink azt sugallják, hogy az SSB fehérje az E. coli RecQ helikáz mechanokémiai működését közvetlenül nem változtatja meg, hanem egyes DNS-szerkezeti elemek felismerését, és ezen keresztül a bonyolultabb DNS-struktúrák hatékony átalakítását segíti elő. A közeljövőben tervezzük annak vizsgálatát is, hogy az E. coli illetve humán topoizomeráz 3 homológok hogyan befolyásolják az adott fajból származó RecQ-helikázok mechanokémiai működését, illetve hogy ez a hatás hogyan járul hozzá a fehérjekomplexek biológiai funkcióinak betöltéséhez.
Ismeretes, hogy számos különböző helikáz képes a Rad51 rekombináz nukleoprotein szálak lebontására (pl. Wu et al. (2001) J. Biol. Chem. 276:19375, Krejci et al. (2003)Nature 423:305). Ezt a folyamatot jelenleg a rekombináció minőségellenőrzésének egyik kulcseseményeként tartják számon. Jelenlegi vizsgálatainkban fordított irányú hatást is sikerült kimutatnunk: azt találjuk, hogy a Rad51 fehérje jelenléte jelentősen megnöveli a D- hurok-szerkezetek helikázok által katalizált lebontásának hatékonyságát.
Budapest, 2012. január 25.
Kovács Mihály