RADIOAKTÍV KONTAMINÁCIÓS FOLYAMATOK VIZSGÁLATA SZERKEZETI ANYAG FELÜLETEKEN
Doktori (PhD) értekezés
Pannon Egyetem
Kémia Doktori Iskola
Készítette:
Kádár László Péter okleveles vegyészmérnök
Témavezető:
Dr. Varga Kálmán egyetemi tanár
Pannon Egyetem Radiokémiai és Radioökológiai Intézet Veszprém
2009
RADIOAKTÍV KONTAMINÁCIÓS FOLYAMATOK VIZSGÁLATA SZERKEZETI ANYAG FELÜLETEKEN
Értekezés doktori (PhD) fokozat elnyerése érdekében Írta: Kádár László Péter
Készült a Pannon Egyetem Kémia Doktori iskolája keretében
Témavezető: Dr. Varga Kálmán
Elfogadásra javaslom (igen / nem)
...
(aláírás) A jelölt a doktori szigorlaton …... % -ot ért el,
Veszprém, ...
...
A Szigorlati bizottság elnöke Az értekezést bírálóként elfogadásra javaslom:
Bíráló neve: …... …... igen /nem
……….
(aláírás) Bíráló neve: …... …... igen /nem
……….
(aláírás)
***Bíráló neve: …... …... igen /nem
……….
(aláírás) A jelölt az értekezés nyilvános vitáján …...% - ot ért el
Veszprém,……….
...
a Bíráló Bizottság elnöke A doktori (PhD) oklevél minősítése…...
………
Az EDT elnöke
KIVONAT
RADIOAKTÍV KONTAMINÁCIÓS FOLYAMATOK VIZSGÁLATA SZERKEZETI ANYAG FELÜLETEKEN
Kádár László Péter
A disszertáció átfogó képet nyújt a nyomottvizes reaktorblokkok biztonságos üzemvitele szempontjából kiemelkedő fontosságú primerköri szerkezeti anyagok (korrózióálló acél, Zr-Nb ötvözet) kontaminációs és korróziós sajátságairól urán és transzurán (Pu, Am Cm) nuklidokkal szennyezett bórsavas oldatokban. A 2003. április 10-én a paksi atomerőmű 2. reaktorblokkjában történt üzemzavarral összefüggésben alapvető jelentőségű a pihentető medencébe kerülő radionuklidok mennyiségének (aktivitásának) becslése, a szennyeződés mértékének és kinetikájának megismerése szerkezeti anyagfelületeken.
A szerző urán és transzurán (Pu, Am, Cm) akkumulációjának mértékét, kinetikáját és mechanizmusát vizsgálta primerköri szerkezeti anyagok felületén bórsavas modelloldatból és erőművi oldatmintából laboratóriumi körülmények között. A megkötődési folyamatok alapvető összefüggéseinek tanulmányozása során alfa-spektrometriás, ICP-MS és felületvizsgálati (SEM-EDX, voltammetria, XPS) módszereket alkalmazott.
A vizsgálatok során kapott eredmények igazolják, hogy a kontamináló oldat pH-ja és a felületek korróziós állapota jelentős mértékben befolyásolja az urán- és transzurán (Pu, Am, Cm) akkumuláció mértékét. A vizsgált felületek kontaminálhatóságának jelentős eltérése az egyes felületeket borító oxidrétegek eltérő morfológiájával (érdességével), összetételével, illetve vastagságával magyarázható.
ABSTRACT
INVESTIGATION OF RADIOACTIVE CONTAMINATION PROCESSES ON STRUCTURAL MATERIAL SURFACES
Péter László Kádár
In the dissertation, the contamination and corrosion processes of the structural materials (stainless steels, Zr-Nb alloys) utilized at pressurized water reactors in boric acid coolant contaminated by uranium and transuranium (Pu, Am, Cm) nuclides were presented and discussed. As a consequence of the breakdown on April 10, 2003 of the reactor block 2 of Paks Nuclear Power Plant (PNPP) it was of special importance to estimate the amount of the above radionuclides in the fuel-transfer pond as well as the extent and kinetics of the contamination phenomena on structural material surfaces.
The extent, kinetic and mechanism of the uranium and transuranium accumulation (Pu, Am, Cm) on structural material surfaces was studied in boric acid model solutions and industrial sample of primary coolant under laboratory conditions. Apha-spectrometric, ICP- MS and surface analytic (SEM-EDX, XPS) and electrochemical (voltammetric) methods were used to determinate the basic relationships for the accumulation processes.
The experimental results reveal that the extent and the kinetics of uranium and transuranium (Pu, Am, Cm) accumulations are primarily influenced by the pH of the boric acid solution and the corrosion state of the steel surfaces. The contamination processes are strongly dependent on the chemical structure and composition of the oxide layer formed on the surfaces.
AUSZUG
UNTERSUCHUNG RADIOAKTIVER KONTAMINACIONSPROZESSE AN OBERFLÄCHEN DER KONSTRUKTIONSMATERIALEN
Péter László Kádár
Die Dissertation gibt einen Überblick über einen für den sicheren Betrieb der Druckwasserreaktoren bedeutenden Korrosions- und Kontaminationseigenheiten der Konstruktionswerkstoffe (korrosionbeständiger Stahl, Zr-Nb Legierung) des Primärkreises, mit Uran und Transuran (Pu, Am, Cm) kontaminierten Radionukliden im borsäurige Lösung.
Wegen dem an 10. April 2003 ereignetes Betriebstörung der Reaktorblock Nummer 2. im AKW Paks ist ganz wichtig, die Grösse (Aktivität) der Radionukliden in Gärbecken zu schätzen, und der Grad und Kinetik der Kontamination an/auf Oberflächen der Konstruktionsmaterialien kennen zu lernen.
Der Autor hat den Grad, Kinetik und Mechanismus des Uran und Transuran (Pu, Am, Cm) Akkumulation an Oberflächen der Konstruktionswerkstoffe (korrosionsbeständiger Stahl, Zr-Nb Legierung) des Primärkreises in borsäurigen Modelllösung und im Lösungmuster von AKW unter Laboratoriumbedingungen geprüft. Bei der Analyse der grundsätzlichen Zusammenhänge der Akkumulation hat der Autor alpha-spektrometrische, ICP-MS und oberflächige (SEM-EDX, Voltammetrie, XPS) Prüfungsmethoden angewendet.
Die Resultate bewähren das dass der pH-Wert der Kontaminationslösung und die Korrosionszustand der Oberflächen ein deutlicher Einfluss auf den Grad der Akkumulation des Urans und Transurans (Pu, Am, Cm) haben. Die deutlichen Unterschiede bei der Kontaminationsfähigkeit der geprüften Oberflächen ist mit der Morphologie (Rauheit), Zusammensetzung und Dicke der Oxydenschicht an den Oberflächen zu erklären.
RADIOAKTÍV KONTAMINÁCIÓS FOLYAMATOK VIZSGÁLATA SZERKEZETI ANYAG FELÜLETEKEN
Tartalomjegyzék
I. BEVEZETÉS...3
II. CÉLKITŰZÉSEK, A FELADATOK MEGFOGALMAZÁSA...4
III. IRODALMI ÁTTEKINTÉS ...7
III.1. Kontaminációs folyamatok urán és transzurán (Pu, Am, Cm) elemeket tartalmazó vizes oldatokban ...7
III.1.1. Az urán- és transzurán (Pu, Am, Cm) elemek kémiája ...7
III.1.1.1. A kontamináció jellegét és mértékét befolyásoló tényezők és azok kapcsolatrendszere: ...7
III.1.1.2.Az urán és transzurán (Pu, Am, Cm) specieszek kémiai formáit befolyásoló paraméterek vizes oldatokban:... 8
III.1.2. Az urán és transzurán (Pu, Am, Cm) izotópok szorpciója acélfelületen...13
III.1.2.1. Az ausztenites acél felületi sajátságainak és korróziós tulajdonságainak áttekintése ...13
III.1.2.2. Urán és transzurán (Pu, Am, Cm) specieszek szorpciója ausztenites acélfelületeken ...17
III.1.3. Az urán- és transzurán (Pu, Am, Cm) izotópok szorpciója Zr+Nb ötvözetek felületén...29
III.1.3.1. Az Zr+Nb ötvözetek felületi sajátságainak és korróziós tulajdonságainak áttekintése ...29
III.1.3.2. Urán és transzurán (Pu, Am, Cm) specieszek szorpciója Zr+Nb ötvözetek felületén...37
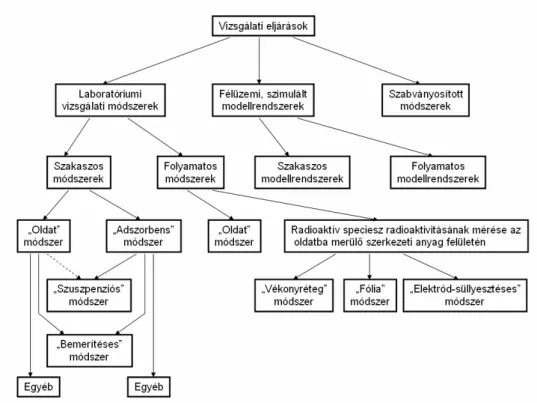
III.2. A kontaminációs folyamatok laboratóriumi vizsgálatának módszertani kérdései...46
IV. KÍSÉRLETI RÉSZ ...50
IV.1. A vizsgált szerkezeti anyagok...51
IV.2. A kontaminációs vizsgálatok végrehajtása ...51
IV.2.1. Az alkalmazott modellrendszer ismertetése...51
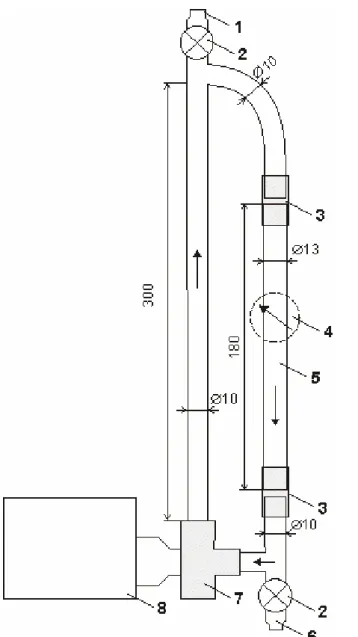
IV.2.1.1. Dinamikus cirkulációs modellrendszer acélfelületek vizsgálatára...51
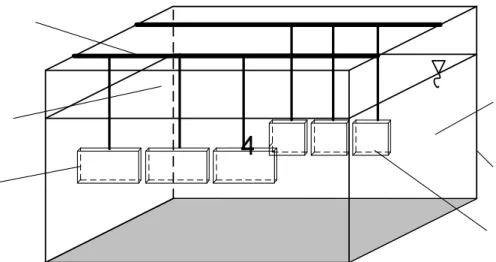
IV.2.1.2. Statikus modellrendszer Zr-Nb ötvözet felületek vizsgálatára...56
IV.2.2. Az adszorpciós vizsgálatok ismertetése...57
IV.2.2.1. A dinamikus adszorpciós-deszorpciós vizsgálatok ismertetése ...57
IV.2.2.1.1. Az urán-akkumuláció vizsgálata modelloldatban ...57
IV.2.2.1.2. Az urán- és transzurán (Pu, Am, Cm) akkumuláció vizsgálata erőművi oldatmintában...58
IV.2.2.2. A statikus szorpciós vizsgálatok ismertetése ...61
IV.3. Vizsgálati és számítási-értékelési eljárások ...66
IV.3.1. A szorpciós jellemzők meghatározására kidolgozott számítási modellek ismertetése...66
IV.3.1.1. A dinamikus szorpciós vizsgálatok számítási-értékelési eljárásainak ismertetése...66
IV.3.1.2. A statikus szorpciós vizsgálatok számítási-értékelési eljárásainak ismertetése ...68
IV.3.2. Alfa-spektrometriás elemzések...71
IV.3.3. Speciációs vizsgálatok ...72
IV.3.4. ICP-MS vizsgálatok...73
IV.3.5. Felületvizsgálati eljárások...78
IV.3.5.1. XPS mérések...78
IV.3.5.2. Felületek és metalográfiai csiszolatok kombinált SEM-EDX vizsgálata...79
IV.3.5.3. Felületek korróziós állapotának tanulmányozása voltammetriás eljárással ...80
V. KÍSÉRLETI EREDMÉNYEK ÉS ÉRTÉKELÉSÜK ...82
V.1. Vizsgálatok dinamikus cirkulációs modellrendszerben ...82
V.1.1. Módszertani kérdések áttekintése...82
V.1.2 Urán-akkumuláció tanulmányozása ausztenites acélcső felületeken bórsavas modelloldatban [132-133] ..83
V.1.2.1. Felületi szennyezettség és a bórsavas oldat vizsgálata alfa- spektrometriás módszerrel...83
V.1.2.2. Felületvizsgálati eredmények...89
V.1.3. Urán- és transzurán (Pu, Am, Cm) akkumuláció tanulmányozása ausztenites acélcső felületeken erőművi oldatmintában [138-139]... 92
V.1.3.1. Az adszorpciós és speciációs vizsgálatok eredményeinek összehasonlító értékelése ...92
V.1.3.2. Felületvizsgálati eredmények...98
V.2. Urán- akkumuláció tanulmányozása Zr-Nb ötvözetek felületén statikus modellrendszerben...103
V.2.1. Módszertani megfontolások ...103
V.2.2. Szorpciós vizsgálatok eredményei ...105
V.2.3. Felületvizsgálati eredmények...109
VI. ÖSSZEFOGLALÁS ...115
VII. IRODALOMJEGYZÉK ...119
VIII. A DOKTORI (PHD) ÉRTEKEZÉS TÉZISEI ...126
IX. THESES OF THE PHD DISSERTATION ...129
X. ÉRTEKEZÉS ALAPJÁT KÉPEZŐ TUDOMÁNYOS KÖZLEMÉNYEK JEGYZÉKE...132
Függelék... 136
Köszönetnyilvánítás...181
I. BEVEZETÉS
A Föld népességének folyamatos növekedése és a gazdasági növekedés a globális energiaigények folyamatos emelkedését vetíti előre. Szakértői vélemények szerint az elkövetkező évtizedekben a globális energiafogyasztás jelentős mértékű növekedése várható.
Az energiatermelés a jövőben valószínűleg olyan primer energiaforrások felé tolódik el, amelyek gazdaságilag versenyképesek, környezetvédelmi szempontból biztosítják a fenntarthatóságot és ellátási láncuk biztonságos. A fenntartható fejlődés követelményeivel összhangban az energetikai szektornak reálisan olyan energiaforrások használata felé kell elmozdulnia, amelyeknek alacsony a széndioxid kibocsátása. Az atomenergia eleget tesz ennek a követelménynek, s így egyes becslések szerint az atomenergia részaránya az energiatermelésben több mint a triplájára emelkedik a 2010-től 2030-ig terjedő időszakban [1].
Hazánkban a ma meglévő 9000 MW névleges villamos teljesítőképességű erőműparkból másfél évtized után legfeljebb csak 5000 MW maradhat versenyképes a villamos energiapiacon, tehát az erőműpark fejlesztése indokolt. Az ország energiaellátásában a Paksi Atomerőmű Zrt. döntő szerepet vállal, a hazai villamosenergia-szükségletnek kb.
40%-a e forrásból származik. A paksi atomerőmű 4 db VVER-440/213 típusú reaktorral rendelkezik. Tematikus vizsgálatok igazolták, hogy a reaktor blokkok megfelelő műszaki állapotban vannak a korábban 30 évre tervezett élettartam további 20 évvel történő meghosszabbításához. A foszilis energiaforrások korlátozott rendelkezésre állása, a külföldi energiahordozó (elsősorban gáz) ellátás bizonytalansága, valamint az erőműpark elöregedése előrevetíti a nukleáris erőművi kapacitás növelését, azaz új atomerőművi blokkok építését. A kapcsolódó elvi engedélyezési folyamatban az Országgyülés a közelmúltban nagy többséggel pozitív döntést hozott. Mindezek alapján reálisan feltételezhető, hogy a nyomottvizes atomerőművi reaktorok még több évtizeden keresztül meghatározó szerepet játszanak hazánk villamosenergia ellátásában.
A nyomottvizes reaktorblokkok biztonságos üzemvitele szempontjából a primerköri szerkezeti anyagok korróziós-eróziós folyamatainak, a kontamináció-dekontamináció és korrózió-korrózióvédelem komplex kapcsolatrendszerének ismerete kiemelkedő fontosságú.
Ezt igazolják a paksi atomerőműben 2003. április 10-én bekövetkezett súlyos üzemzavar előzményei. A 2002. évben az erőmű 1-3. reaktorblokkjainak primer hűtőkörében jelentős
mennyiségű Fe-oxid lerakódást mutattak ki. A fűtőelem kazetták felületein képződött korróziótermék-lerakódások rontották a reaktorblokkok teljesítményét, így 2003-ban a 2.
blokk fűtőelem kazettáinak külső tartályos tisztítására került sor. A tisztítás során 2003. április 10-én 3. fokozatú súlyos üzemzavar következett be, melynek során az erőmű 2.
reaktorblokkjának különböző technológiai egységeit (1. akna, pihentető medence) a számottevő mennyiségű urán és transzurán (Pu, Cm) szennyezte. A 2006. októberében megkezdődött és 2007. januárjában sikeresen befejeződött - sérült-fűtőelem átrakási (tokozási) munkálatokkal összefüggésben az urán és transzurán nuklidok, valamint egyes hasadványtermékek kontaminációs (adszorpciós-deszorpciós) folyamatainak ismerete megkülönböztetett jelentőséggel bírt. Az 1. akna bórsavas közegébe bejutott urán- és transzurán nuklidok, valamint hasadványtermékek különböző kémiai formában (molekuláris, kolloid és/vagy diszperz) fordultak elő. Az átrakási munkálatok kapcsán alapvetően fontos a pihentető medencébe kerülő radionuklidok mennyiségének (aktivitásának) becslése, a szennyeződés mértékének és kinetikájának megismerése szerkezeti anyagfelületeken. Az urán- és transzurán akkumuláció mechanizmusáról és kinetikájáról a fontosabb szerkezeti anyagok (korrózióálló acélok, Zr-Nb ötvözetek) felületén ugyanis nem áll rendelkezésre a vonatkozó szakirodalomban kielégítő információ.
II. CÉLKITŰZÉSEK, A FELADATOK MEGFOGALMAZÁSA
A Bevezetésben vázolt előzmények ismeretében négy hazai intézet együttműködésének keretében, a Pannon Egyetem Radiokémiai és Radioökológia Intézetének témavezetésével 2005. évben átfogó kutatási project indult „Urán és transzurán (Pu, Am, Cm) elemek kémiája és a transzurán (Pu, Cm) izotópok akkumulációjának vizsgálata primerköri szerkezeti anyag felületeken” című munka elvégzésére. A kutatásokat a Paksi Atomerőmű Zrt finanszírozta.
A 2006-2009. időszakban PhD ösztöndíjasként kapcsolódtam be a fenti kutatási programba.
Elsődleges célom az urán nuklidok feldúsulására jellemző kinetikai és mechanisztikus összefüggések tematikus vizsgálata volt különböző szerkezeti anyagok. (korrózióálló acél és Zr-Nb ötvözet) felületén. További célként fogalmazódott meg az, hogy megismerjem néhány fontos transzurán (Pu, Am, Cm) akkumulációjának mértékét, kinetikáját és mechanizmusát az említett korrózióálló acélmintákon.
A vázolt célkitűzéssel megvalósítása érdekében három éves, szisztematikus kutatási programot állítottunk össze, amelynek főbb részfeladatai az alábbiakban foglalhatók össze:
a. A szakirodalmi adatok feldolgozása az alábbi témakörökben:
Az urán- és transzurán (Pu, Am, Cm) elemek kémiájának (analitikai kémia, kolloidkémia, elektrokémia) összehasonlító áttekintése bórsavas oldatokban. Az urán- és transzurán (Pu, Cm) elemek domináns kémiai formáinak és azok relatív szorpciós képességének jellemzése az aktív zóna szerkezeti anyagainak (elsősorban korrózióálló acél, Fe-oxidok és Zr-Nb ötvözet) felületén.
b. Az urán-akkumuláció (szorpció-deszorpció) mértékének, és a megkötődési folyamat alapvető összefüggéseinek tanulmányozása modellrendszerben a primerkör meghatározó szerkezeti anyaga, a 08X18H10T (GOSZT 5632-61) típusú ausztenites korrózióálló acél felületén. E részfeladat magába foglalta az urán-feldúsulás idő- és pH-függésének vizsgálatát dinamikus modellrendszerben, bórsavas hőhordozó modelloldatában a Paksi Atomerőmű Zrt. által biztosított – 2. blokki gőzfejlesztőből (GF) kivágott - ausztenites acél hőátadócső felületeken. Feladatként jelentkezett továbbá az urán felületi többletkoncentrációjának egy - az urán acélfelületi és oldatfázisbeli aktivitás koncentrációjának az alfa-spektrometriás detektálásán alapuló – meghatározására alkalmas modell és számítási algoritmus kidolgozása. A szorpciós folyamat mechanizmusának megismerése érdekében az acélcsőminták belső felületének passzív állapotát, morfológiáját és kémiai összetételét voltammetriás és SEM-EDX eljárással vizsgáltuk; a megkötődött urán oxidációs állapotát (kémiai formáját) röntgengerjesztéses fotoelektron-spektroszkópiai (XPS) módszerrel azonosítottuk.
c. Az urán- és transzurán (Pu, Am, Cm) akkumuláció (szorpció-deszorpció) mértékének és kinetikájának vizsgálata urán- és transzurán-szennyezőket tartalmazó – a Paksi Atomerőmű Zrt. által biztosított - oldatmintából korrózióálló acélfelületeken dinamikus modellrendszerben.
d. Az urán-akkumuláció (szorpció-deszorpció) mértékének és kinetikájának vizsgálata urán- és transzurán-szennyezőket tartalmazó – a Paksi Atomerőmű Zrt. által biztosított - oldatmintából Zr-Nb ötvözetek felületén statikus modellrendszerben.
A c.) és d.) részfeladat magában foglalta:
- Az urán- és transzurán (Pu, Am, Cm) akkumuláció mértékének és időfüggésének tanulmányozását Paksi Atomerőmű Zrt. által biztosított primerköri szerkezeti anyag minták felületén.
- Az urán- és transzurán (Pu, Am, Cm) deszorpció időfüggésének tanulmányozását Paksi Atomerőmű Zrt. által biztosított primerköri szerkezeti anyag minták felületén.
- Az urán és transzurán elemek felületi és oldatfázisbeli kémiai koncentrációjának, a különféle specieszek (részecske, kolloid és oldott (anionos és kationos)) oldatfázisbeli megoszlásának illetve aktivitás koncentrációjának meghatározására alkalmas kémiai elválasztási (ioncserés) eljárás, valamint ICP-MS és alfa-spektrometriás detektálási módszer alkalmazását.
- A primerköri szerkezeti anyag felületek felületkémiai és korróziós vizsgálatát (SEM-EDX, voltammetria, és XPS).
- Az oldatmintákba beoldódott korróziótermékek (Fe, Cr, Ni, Zr, Nb) kémiai koncentrációjának meghatározását a kezelési idő függvényében ICP-OES módszerrel.
III. IRODALMI ÁTTEKINTÉS
III.1. Kontaminációs folyamatok urán és transzurán (Pu, Am, Cm) elemeket tartalmazó vizes oldatokban
III.1.1. Az urán- és transzurán (Pu, Am, Cm) elemek kémiája
III.1.1.1. A kontamináció jellegét és mértékét befolyásoló tényezők és azok kapcsolatrendszere:
Az irodalomkutatás eredményei alapján az urán és transzurán elemek kontaminációjának mértékét és jellegét befolyásoló fontosabb tényezőket és azok kapcsolatrendszerét a III.1.
ábrán foglaltuk össze. A III.1. ábra egyértelműen alátámasztja, hogy az oldatkémia (vízkémia) döntő hatással van a szennyező speciesek megjelenési formájára, illetve a kontaminált felület felületkémiai és korróziós jellemzőire. Az említett paraméterek együttesen határozzák meg a szerkezeti anyag felületek kontaminációjának típusát, mértékét és mechanizmusát. Másként fogalmazva az oldatkémiai jellemzők megszabják a szennyező komponensek domináns megjelenési formáit az oldatfázisban, és befolyásolják a szilárd fázis és a szilárd/folyadék határfelület jellemzőit. A felsorolt tényezők ugyanakkor döntő hatással vannak a kontamináció folyamatára, amely lehet adszorpció, kemiszorpció, csapadékleválás, vagy kolloidkiválás.
Az erőművi vízkémia (pl. primerköri vízkémia) alapvető feladata tehát, hogy biztosítsa:
- a szennyező anyag műszakilag elérhető minimális koncentrációját és kedvező kémiai formáját (lehetőleg oldott, minimális diszperz- és kolloidfázis jelenlétében),
- az alkalmazott szerkezeti anyagok minimális vagy a minimálishoz közeli, ill. tervezett mértékű elektrokémiai korrózióját, s így
- a szerkezeti anyag felületek radioaktív kontaminációjának (illetve rekontaminációjának) minimális szintjét.
III.1. ábra: Az urán és transzurán (Pu, Am, Cm) nuklidok kontaminációjának jellegét és mértékét befolyásoló tényezők és azok kapcsolatrendszere fémes szerkezeti anyag/ vizes oldat
heterogén rendszerben
III.1.1.2.Az urán és transzurán (Pu, Am, Cm) specieszek kémiai formáit befolyásoló paraméterek vizes oldatokban:
- Oxidációs állapot, redox potenciál
Az aktinidák vizes oldatokban különböző oxidációs állapotokban fordulnak elő [2-4], leggyakoribbak a III-VI állapotok. Vizes oldatokban az U legstabilabb formája a VI oxidációs állapotú UO22+, az Am és Cm esetében a III oxidációs állapotú Am3+ ill. Cm3+ a legstabilabb.
Az Am erősen oxidatív közegben V és VI oxidációs állapotúvá alakul, a Cm nem oxidálható.
Vizes oldatokban a Pu III, IV, V és VI állapotokban is előfordulhat Pu3+, Pu4+, PuO2+ illetve PuO22+ kationként, melyek a közel azonos redoxpotenciálok miatt egymás mellett is létezhetnek [2, 5]. Az aktinidák kémiai hasonlósága elsősorban azonos oxidációs állapotokban mutatkozik meg. Az oxidációs állapot megváltozhat a redoxpotenciál változásakor, ami bekövetkezhet az oldatfázis kémiai összetételének, az oldott oxigén koncentrációjának, illetve a pH változására.
- Komplexképzés
Az aktinida kationok erős Lewis savak, amelyek számos komplexet képeznek [2, 6].
Ezek közül a legstabilabbak az erős Lewis bázisú ligandumokkal képzett komplexek. A kötések elektrosztatikus jellegűek, ezért a komplexek stabilitása az aktinidák és a ligandumok effektív töltésének növekedésével nő. A különböző oxidációs állapotú aktinida (An)
komplexek esetében tehát a stabilitás általában (ha nincs egyéb, pl. sztérikus hatás) a következő sorrendben csökken:
An4+>AnO22+>An3+>AnO2+
Azonos oxidációs állapotban az aktinidák effektív töltése az aktinida kation méretének csökkenésével, tehát az aktinida kontrakció miatt a tömegszám növekedésével nő. Így a komplexek stabilitása - azonos oxidációs állapotban - elméletileg a következő sorrend szerint csökken:
Pu>Np>U>Th,
ugyanakkor, az effektív töltés kisebb különbségei mellett egyéb hatások miatt a sorrend eltérően is alakulhat.
A komplexek stabilitását a ligandum szerkezete is befolyásolja. Stabil aktinida komplexek a kemény donor atomokat tartalmazó ionokkal/molekulákkal alakulnak ki. Az aktinidák igen erős hidroxid-komplex képzők. Szervetlen ionokkal alkotott komplexeik stabilitása – az effektív töltéseknek megfelelően - általában az alábbi sorrendben változik:
PO43- > CO32- > SO42- > NO3-
Halogenidekkel képzett komplexek között a fluorid a legstabilabb:
F- >> Cl- > Br- > I-
Az f-elemek számos komplexet/kelátot képeznek szerves ligandumokkal.
Viselkedésüket vizes oldatokban döntően befolyásolja az aktinidák hidrolízise, a hidroxil-komplexek stabilitása [2, 5, 7], továbbá ezek oldhatósága. A hidrolízis a gyengén savas oldatoktól a tömény lúgos oldatokig végbemegy a III, IV és VI oxidációs állapotban, a semleges vagy lúgos oldatokban gyakran az aktinidáknak ez a legfontosabb komplexképzési reakciója. A nagy effektív töltésű ionok különböző koordinációs számú, mono és polinukleáris (dimer és polimer) hidroxid komplexeket is képeznek. Az aktinidák hidroxidjai gyakran rosszul oldódnak. A vizsgált aktinidák hidroxil-komplexei között a legstabilabbak a Pu(IV) komplexek [8], melyek már pH=0 és 1 közt is képződnek. Egyben ezeknek az oldhatósága a legkisebb. Az uranil(VI) hidroxil-komplexei pH=3-nál jelennek meg, és szintén számos polinukleáris komplex képződik. Az Am és Cm(III) képezi a kevésbé stabil komplexeket, pH 7 körül azonban így is domináló specieszekké válnak. Az aktinidák számos
stabil komplexet képeznek karbonát ionokkal (vízben oldott CO2), illetve vegyes hidroxo- karbonát komplexeket képeznek többnyire semleges/lúgos közegben.
- Oldhatóság, csapadék- és kolloidképzés
A hidroxil-komplexek általában nagyon rosszul oldódnak semleges vagy lúgos közegben, de savas tartományban is kiválhatnak vagy polimerként valódi kolloidot képezhetnek (elsősorban a IV oxidációs állapotú aktinidák) [2, 5]. A rossz oldhatóság a IV és III oxidációs állapotú komplexek jellemzője (hidroxil, fluorid) szemben a magasabb oxidációs állapotú formákkal. A valódi kolloidokon kívül az aktinidák megkötődhetnek kolloid formájú szennyezőkön is pszeudo-kolloidokat képezve.
- Radiolitikus folyamatok, diszproporcionálódás
Autoradiolízis általában tömény oldatokban következik be (Pu koncentráció > 1 mol·dm-3), de a rövid felezési idejű, nagy fajlagos aktivitású aktinidáknál, mint pl. a 242Cm nagyságrendekkel kisebb koncentrációban is jelentős lehet az autoradiolízis. Radiolízis nagy összaktivitás-koncetrációjú közegben is lejátszódik. A keletkező radiolízis termékek redox reakciókat válthatnak ki.
Szintén nagyobb koncentrációknál jellemző folyamat a diszproporcionálódás közbenső oxidációs állapotokban. Így a Pu(V) átalakul Pu(IV) és Pu(VI) formává, megváltoztatva ezzel egyéb fizikai-kémiai jellemzőket, pl. csökkentve a Pu oldhatóságát.
Az aktinidák megjelenési formáit vizes oldatokban - az egyensúlyi és stabilitási állandók alapján - hidrokémiai programokkal számolni lehet.
Számításokat végeztünk a VisualMINTEQ programmal arra vonatkozóan, hogy a PA 2. blokki 1. akna hűtővizének vizsgált összetétele mellett milyen az urán, plutónium, amerícium és kűrium specieszek megoszlása a vizes oldatban [9]. A számításokhoz az alábbi bemenő paraméterek használtuk fel:
- Bórsav koncentráció: c= 20 g·dm-3 (pH=4,2),
A számítások szerint a bórsav nem képez komplexet egyik aktinidával sem. Így a 20 g·dm-3 bórsav koncentráció a specieszek számítását nem befolyásolja, de a bórsav határozza meg az oldat pH-ját és a bórsav-szorpció a felületeken csökkentheti az aktinidák megkötődését.
- Ionerősség: I=0,01,
- Urán koncentráció: cU =3·10-6 mol·dm-3 (0,76 mg U·dm-3),
- Urán speciesz: UO22+,
- Redoxpotenciál: Eh=918 mV
Feltételeztük, hogy a redoxpotenciált a legnagyobb koncentrációjú kation, az oldott urán határozza meg.
- Pu koncentráció: cPu =1·10-8 mol·dm-3 (6000 Bq 239Pu·dm-3) - Cm koncentráció: cCm =2·10-11 mol·dm-3 (20000 Bq 244Cm·dm-3)
Feltételezzük, hogy az Am speciesek megoszlása megegyezik a Cm-éval, mert az adott redoxpotenciál mellett az Am(III) nem oxidálódik, így a Cm(III)-mal azonos oxidációs állapotú.
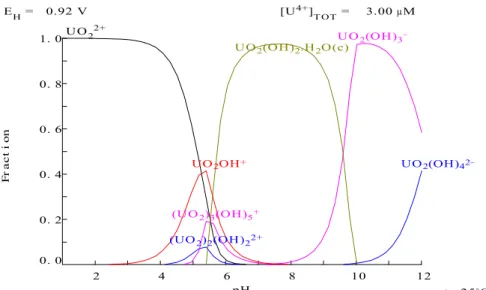
Az urán, plutónium és amerícium speciesek számított megoszlását a pH-függvényében rendre a III.2-III.4. ábrák szemléltetik. Minden nuklid a 3 leggyakoribb kémiai formáját táblázatosan is összefoglaltuk (III.1. táblázat).
III.1. táblázat: Az U, Pu és Cm (Am) specieszek VisualMINTEQ programmal becsült megoszlása [9].
Speciesz Koncentráció
(mol·dm-3)
U UO22+ 2,93·10-6
UO2(OH) + 5,76·10-8
(UO2) 2(OH)2 2+ 5,59·10-9
Pu PuO2+ 6,66·10-9
PuO22+ 3,03·10-9
PuO2(OH) + 3,03·10-10
Cm Cm3+ 1,99·10-11
Cm(OH)2+ 8,67·10-14
Cm(OH)2+ 9,17·10-18
2 4 6 8 10 12 0. 0
0. 2 0. 4 0. 6 0. 8 1. 0
Fraction
pH UO22+
(UO2)2(OH)22+
(UO2)3(OH)5+
UO2(OH)3−
UO2(OH)42−
EH = 0.92 V [U4+]T OT = 3.00 μM
UO2(OH)2.H2O(c)
UO2OH+
t= 25°C
III.2. ábra: Az urán specieszek százalékos megoszlása a pH függvényében
2 4 6 8 10 12
0. 0 0. 2 0. 4 0. 6 0. 8 1. 0
Fraction
pH
PuO2(OH)2
PuO2(OH)3− PuO2OH+
EH = 0.92 V [Pu3+]T OT = 10.00 nM
PuO2(cr)
t= 25 C°
III.3. ábra: A plutónium specieszek százalékos megoszlása a pH függvényében
2 4 6 8 10 12
0. 0 0. 2 0. 4 0. 6 0. 8 1. 0
Fraction
pH Am3+
A mO H2+
A mO2+
EH = 0.92 V [Am3+]T OT = 0.02 nM
Am(O H)2+
t= 25 C°
III.4. ábra: Az amerícium specieszek százalékos megoszlása a pH függvényében
Az enyhén savas és - az U(VI) jelenléte következtében - oxidatív közegben a vártnak megfelelően az urán VI oxidációs állapotú uranil-kationként, a Pu részben V és részben VI oxidációs állapotú kationként, az Am és Cm pedig III oxidációs állapotú kationként fordul elő. Egyik izotóp esetében sem jelentős a hidrolízis. Ha a számításokat pH=7 mellett a fenti bemenő paraméterekkel megismételjük, akkor az U, a Pu és a Cm esetében is a hidroxil komplexek lesznek dominánsak: (UO2)3(OH)5 +, PuO2(OH) +, Cm(OH)2+. A Pu esetében az oxidációs állapot is megváltozik, (VI) lesz.
III.1.2. Az urán és transzurán (Pu, Am, Cm) izotópok szorpciója acélfelületen
III.1.2.1. Az ausztenites acél felületi sajátságainak és korróziós tulajdonságainak áttekintése
A szakirodalom szerint ausztenites korrózióálló acélok primerköri hőhordozóval érintkező felületén üzemi körülmények között általában kettős (duplex) szerkezetű oxidréteg alakul ki [10-12]. A védő-oxidréteg vastagsága üzemidőtől függően elérheti a 10-12 μm-t is.
Az alsó védőréteg, mely szorosan a fémfelületre tapad, tömör, zárt felületű. Az alapfémből közvetlenül oxidáció révén keletkezik (Schikkor reakció [13]). Az üzemelés közben az oxidréteg Cr és Ni tartalma nő. Ez a krómban dús réteg mikrokristályos szerkezetű, a krómot főleg 3-as oxidációs fokú oxid (Cr2O3) formában tartalmazza. A felső réteg reduktív vízüzem esetén főként magnetitet (Fe3O4) és esetleg csekély mennyiségű hematitot (Fe2O3) tartalmaz.
Ez nem az alapfémből keletkezik, hanem a hőhordozó közvetítésével kerül rá a felületre.
A magnetit kristályszerkezeti szempontból FeO·Fe2O3 spinellnek felel meg, amelyben a kétértékű vasat helyettesítheti egyéb fémion (pl. Ni2+, Mn2+, Zn2+, Co2+), valamint a háromértékű vas is helyettesíthető Cr3+-al. Ezzel magyarázható, hogy mind a felületközeli tartományban, mind a passzív réteg mélyebb régióiban különféle spinell-szerkezetű vegyes oxidok találhatók (CrxNiyFe3-x-yO4, ahol 0≤x+y≤3). A magnetit, valamint a felületközeli tartományban képződő nem-sztöchiometrikus összetételű nikkel-ferrit (nikkellel szubsztituált magnetit (NixFe3-xO4, ahol x≤1, vagy CoyNixFe3-x-yO4, ahol y+x≤1 és y<<x)) oldhatósága már a magas hőmérsékletű bórsavas hőhordozóban is számottevő. Ugyanakkor a mélyebb oxidrétegekben keletkező vas-kromit (FeO·Cr2O3), valamint annak kobalttal és nikkellel szubsztituált változata (CoyNixFe1-x-yCr2O4, ahol x+y≤1 és y<<x) meghatározó szerepet játszik a felületi oxidréteg védőképességében, mivel a kromitok oldhatósága reduktív vízüzem esetén még magas hőmérsékleten is rendkívül alacsony. Oxigén-tartalmú hűtőközegben, vagy
oxidálószerek jelenlétében azonban a kromitok megbomlanak, az oxidfilmben lejátszódik a Cr(III)→Cr(VI) oxidációs folyamat és vízoldható CrO42--ionok keletkeznek [14].
A PWR (VVER)-típusú atomerőművekben normál bórsavas vízüzemet feltételezve a korrózió következő megjelenési formáival kell számolni az ausztenites acélfelületeken [14- 17]:
- Egyenletes korrózió
- Nem egyenletes (lyuk, rés, bemaródási) korrózió
- Szelektív korrózió (feszültségi korrózió és kristályközi korrózió)
Egyenletes korrózióról akkor beszélünk, ha az egész fémfelület közel azonos mértékben korrodálódik, egyenletesen vékonyodik el. Az ausztenites acéloknak az egyenletes felületi korrózióval szemben kiváló ellenálló képességük van. Megállapított tény, hogy agresszív ionokat nem tartalmazó vizes oldatban pH 4-10 között passzívan viselkednek, mivel a korróziós termékekből – a fentiekben említett - védőréteg alakul ki, ami megakadályozza a fém további oldódását. Egyenletes korróziós károsodásuk minimális; 280-350 oC hőmérsékletű vízben, statikus körülmények között az egyenletes korrózió sebessége 0,8-4,0 μm/év [14]. Üzemi berendezésekben a sugárterhelés és a hűtőközegáramlás hatására a korrózió sebessége kissé növekszik, de 600 ºC hőmérsékletig az ausztenites acélok korrózióállósága megfelelő [14]. Egy a közelmúltban publikált összefoglaló munka szerint [18] a nukleáris iparban alkalmazott kiváló védőképességű ausztenites korrózióálló acélok átlagos korróziósebessége normál üzemmenet esetén nem haladja meg az 1 μm/év értéket (0,3 μm/év < vk < 1,03 μm/év). Sokkal jellemzőbb a nem egyenletes és szelektív korrózióra való hajlamuk.
A helyi, vagy lokális korrózió esetén a tönkrement fém mennyisége ugyan kicsi, de a meghatározott helyekre összpontosuló károsodás az egész berendezés tönkremenetelét (kilyukadását, törését) okozhatja. A helyi korrózió egyik legveszélyesebb fajtája a lyukkorrózió, mely során a fémfelület egyes pontjain lyukak keletkeznek.
A lyukkorróziónak három fajtája ismert: a pontkorrózió (pitting), amelynél kis átmérőjű, tűszúrásszerű lyukak, a foltkorrózió, amelynél nagyobb átmérőjű, de kisebb mélységű bemaródások, s a szivacsos korrózió, amelynél mély, szabálytalan alakú bemaródások képződnek. A lyukkorróziós károsodás valószínűségét a kloridion-koncentráció növekedése
(általában a közegben és lokalizáltan), az oxigén-tartalom vagy egyéb oxidáló szerek mennyiségének növelése, a hőmérséklet emelkedése, valamint a makro- és mikroszerkezeti inhomogenitások és hibák (pl. zárványok, repedések, különböző szennyeződések, folytonossági hibák) fokozzák [19-21]. A helyi korrózió különösen nagymértékű olyan áramlásmentes helyeken, ahol a vizes oldat betöményedhet és így szennyezőinek koncentrációja növekszik.
Klorid tartalmú vizekben az ausztenites acélokat a réskorrózió is veszélyezteti. (A reaktorvízben maximálisan csak 0,1 mg·kg-1 klorid-koncentráció engedhető meg.) Ez a folyamat végeredményben, egy résben kialakult lyukkorrózió. Előidézéséhez kisebb klorid- koncentráció szükséges, mint ami a lyukkorrózió megindulását előidézi. Különösen veszélyeztetett helyek a nem vezető anyag és a fém között kialakuló szűk felületek, ahol a gátolt diffúzió miatt a kloridionok feldúsúlhatnak és a korróziótermékek lerakódhatnak. A résben a korróziótermékek kialakulása folytán a pH is csökken. A fém és a rajta található lerakódások között is kialakulhat a réskorrózió.
A feszültségkorrózió hatására az acélban repedések keletkeznek, ezért a krómnikkel- ötvözetek és az ausztenites acélok feszültségkorrózióját korróziós repedésnek is szokás nevezni [14-15, 22]. Mértéke sok tényezőtől függ, például az acélban fellépő üzemi (munka-) feszültség nagyságától, a hőhordozó összetételétől, az acélok feszültségállapotától és a felületi védőréteg jellemzőitől. Irodalmi adatok igazolják [14, 23-29], hogy az ausztenites acélok feszültségkorrózióra való hajlamát a fém szerkezete is jelentősen befolyásolja. Különböző hatások (hidegmegmunkálás, hegesztés és egyéb specifikus hatások (köszörülés, csiszolás, őrlés, adszorbeált gázok hatása, nagyenergiájú radioaktív vagy gyorsított töltött részecskékkel történő besugárzás)) eredményeként bekövetkezhet a paramágneses ausztenit fázis (γ-fázis) ferromágneses ferritté vagy martenzitté (α-fázis) alakulása, amely kedvezőtlenül módosíthatja az alapfém metallográfiai és korróziós sajátságait. Jelentős klorid- és oxigéntartalmú közegben 10%-nyi vagy annál több ferritet tartalmazó ausztenites acélokat számottevő mértében károsítja a feszültségkorrózió [14, 22]. Az ausztenites acél korróziós ellenálló képessége a ferrit-tartalom növekedésével jelentősen csökken. A nagyobb térfogatú α-fázis jelentős mennyiségének képződése - különösen, ha az összefüggő hálózatot képez a kristályszemcsék határfelületén - drasztikusan megnöveli a korróziós repedések kialakulásának valószínűségét. Az α-fázis megjelenése módosítja az acél mechanikai
tulajdonságait is: növeli a szilárdságát, keménységét, de erőteljesen csökkenti a szívósságát.
Ezt a jelenséget öregedésnek nevezzük.
Különösen veszélyes, ha az ausztenites acélok feszültségkorróziós aktivátorok (F-, Cl-, SO4- és Na-ionok) jelenlétében nagy hőmérsékletű és oxigént tartalmazó vizes oldattal érintkeznek, mert az a berendezések gyors tönkremenetelét okozhatja [30]. A harmincas évek óta ismert, hogy az ausztenites korrózióálló acélokból készült csöves hőcserélők viszonylag nagy klorid-ion tartalmú vizek esetén hajlamosak a feszültségkorrózióra, ha a fém hőmérséklete meghaladja a 60 oC-ot. Azóta számos publikáció foglalkozott a kérdéssel, de a jelenség mechanizmusára vonatkozó elméletek máig sem egységesek. Kétféle megközelítés ismert a feszültség-szorpciós és az anódos vagy aktív utas (active-path) mechanizmus [31]. A feszültség-szorpciós mechanizmus szerint a klorid-ion kemiszorpciója fellazítja a fématomok közötti kötéseket, ami húzó igénybevételkor a repedés mechanikai úton történő terjedését eredményezi. Az orosz kísérleti adatok szerint a 08X18H10T ausztenites acél feszültségkorrózióját elindító érték a klorid-ion 10 mg·m-2 = 1 μg·cm-2 felületi koncentrációja.
Az anódos mechanizmus szerint a gőzfejlesztő víz az anionok koncentrálódása miatt olyan mértékben savassá válik (pH < 3-4), amely felgyorsítja az anódos fémoldódást, s a repedések terjedése a csúcsoknál bekövetkező anódos fémoldódás következménye. A repedések terjedésének egyik feltétele, hogy elegendő mennyiségű oxidáló anyag (pl. a réz korróziótermékekből keletkező oxigén) hatoljon be a repedésbe, és a redukált termékek eltávozhassanak a repedésből.
Az ausztenites acéloknál kristályközi korrózió is jelentkezhet, mely során a kristályokat összetartó erő gyengül, az anyag elridegedik, törékennyé válik, s hatására kristályhatármenti repedések keletkeznek [32]. A kristályközi korrózió kialakulásának magyarázatára a szakirodalomban többféle elmélet létezik [17, 23, 25]. Az erre való hajlamot előidéző elektrokémiai heterogenitást a legtöbb elmélet szerint az acél hűtése során az 550- 650 oC hőmérsékleten tartott acélból kiváló valamely új fázis (pl. karbid, ferrit) megjelenésével hozzák kapcsolatba. Mivel ezek az ausztenites acélnál nagyobb mennyiségű krómot tartalmaznak, körülöttük az anódos zónákban a krómtartalom csökken. Olyan elképzelések is vannak, amely szerint az új fázis krómban szegényebb (pl. vaskarbid), amely elektronnegatívabb az ötvözet többi részénél, s ezért anódként fog viselkedni. A kristályhatárok lecsökkent korróziós ellenállását a fázisátalakulások következtében fellépő mechanikai feszültségekkel is magyarázzák. Ilyen feszültség léphet fel pl. a γ→α átalakulásnál, ahol az α-fázis létrejöttét a térfogat jelentékeny csökkenése kíséri. Meg kell
jegyezni, hogy a nagy széntartalmú acélok sokkal érzékenyebbek a kristályközi korrózióra, mivel a szén fokozott mértékben diffundál a szemcsék felületére. A legjobb védekezés a kristályközi korrózióval szemben, ha az ausztenites rozsdamentes acélokat titánnal vagy nióbiummal ötvözik, stabilizálják.
III.1.2.2. Urán és transzurán (Pu, Am, Cm) specieszek szorpciója ausztenites acélfelületeken
Az urán-vegyületek, főleg a leginkább stabilis hatos oxidációs állapotot jelentő uranil- kation szorpcióját szilárd felületeken főleg földtani környezetben vizsgálták. Az acélon ill.
cirkóniumon, cirkónium-nióbium ötvözeten történő szorpció vizsgálatával rendkívül kevés közlemény foglalkozik. Az urán-szorpció általános elvei azonban jól adaptálhatók az egyéb szilárd felületeken végzett vizsgálatokból és felhasználhatók az acél ill. cirkónium felületeken történő szorpció becslésére. Különösen hasznos információt nyújtanak a különböző vas- oxidokon és a cirkónium-oxidon kapott eredmények, hiszen a kérdéses fémek felületén ugyancsak oxidrétegek találhatók.
Az ionok szorpcióját, így az uranilion szorpcióját is, az utóbbi 1-2 évtizedben leggyakrabban az ún. felületi komplexképződési modell alapján értelmezik. A modellben meghatározó szerepet játszanak az oldatban jelenlevő specieszek kémiai formái, illetve a felületen kialakuló töltéssel rendelkező kötőhelyek. Ha nincs specifikus adszorpció, akkor az ellentétes töltések közti elektrosztatikus kölcsönhatások (ún. nem-specifikus adszorpciós folyamatok) alapvetően befolyásolják a feldúsulás mértékét; azaz a kationok a negatív töltésű felületi csoportokon, az anionok pedig a pozitív töltésű felületi csoportokon kötődhetnek meg és képezhetnek felületi komplexet.
A felületi komplexképződési modellt eredetileg oxid–felületekre fejlesztették ki [33], de később ásványokra, kőzetekre is alkalmazták. A modell abból a feltételezésből indul ki, hogy az oxid/vizes oldat határfelületeken felületi OH-csoportok alakulnak ki, amelyek a pH- tól függően protont vehetnek, fel vagy adhatnak le, azaz protonálódhatnak vagy deprotonálódhatnak. A protonálódás révén pozitív, a deprotonálódáskor negatív felületi csoportok alakulnak ki, amelyek anionokat ill. kationokat köthetnek meg a vizes oldatból.
A felületi csoportok (-SOH) protonálódási ill. deprotonálódási folyamatait, valamint a keletkező felületi komplexek stabilitási állandóit (ún. "intrinsic stability constants") a (1)-(2) egyenletekkel írhatjuk le. A stabilitási állandók felírásánál figyelembe kell venni a felületi elektromos munkát is.
+
+ ⇔−
+
−SOH H SOH2 ,
[ ]
[ ] [ ]
⎟⎠
⎜ ⎞
⎝
⎛− Ψ
=
+
+
RT H F
SOH KSOH SOH
exp
2
2 (1)
− + ⇔−
−
−SOH H SO ,
[ ] ( )
[
SOH]
RT H F
SO KSO
⎟⎠
⎜ ⎞
⎝
⎛ Ψ
−
=
+
−
−
exp
(2) Ahol: F a Faraday-szám, ψ a felületi potenciál, R a gázállandó, T pedig a hőmérséklet (oK). A szögletes zárójelben az egyes specieszek koncentrációját tüntetjük fel.
A felületi potenciál értékének számítására a különböző kettős réteg modelleket alkalmazhatjuk, attól függően, hogy az oldatban milyen az ionerősség. Amennyiben az ionerősség nagy, azaz a kettős réteg síknak tekinthető, akkor az ún. konstans kapacitás modellt alkalmazhatjuk, ahol a felületi potenciál a következőképpen becsülhető [34]:
SmC
0F
Ψ = σ (3)
ahol σ0 a felületi töltéssűrűség, S a fajlagos felület (m2·g-1), m a szorbens koncentrációja (g·
dm-3), C a kettős réteg kapacitása. σ0 a potenciometrikus titrálással határozható meg az alábbi módon [33]:
( [ ] )
S H c
F H − +
= +
σ0 (4)
Ahol: F a Faraday–állandó, cH+ az adagolt hidrogénion teljes mennyisége a potenciometrikus titrálás során, [H+] a hidrogénion koncentrációja az oldatban.
Kis ionerősségeknél a diffúz kettősréteg modellel számolnak (Guy-Chapman modell).
A legbonyolultabb alkalmazási lehetőség az ún. három réteg modell (lásd III.5. ábra), amely megengedi az alkalmazott alapelektrolit felületi reakcióját is [35]. A különböző modelleknél lehetséges folyamatokat a III.2a. és III.2b. táblázatokban foglaltam össze.
Fontos paraméter a szorbens felület nulla töltéspontjának megfelelő pH-érték, ahol a pozitív és negatív töltésű felületi helyek száma megegyezik:
2
2+ − −
= SOH SO
pzc
pK
pH pK (5)
A szorpciós folyamatok leírásához ismerni kell tehát a szorbensre vonatkozó felületi paramétereket, valamint a lehetséges specieszek stabilitási állandóit az oldatban. Ezeket a modell alkalmazásánál bemenő paraméterként adjuk meg. Ugyancsak bemenő paraméterként használjuk a szorpciós adatokat, ezek segítségével számolhatjuk ki a megkötött felületi
specieszekre vonatkozó stabilitási állandókat és felületi koncentrációkat különböző paraméterek, pl. a pH függvényében.
III.5. ábra: A három réteg modell vázlata [33] alapján. M reprezentálja a kationokat, A pedig az anionokat. OHP jelenti a külső Helmholtz-síkot, amely itt megegyezik a nyírási síkkal. ahol
a potenciált definiáljuk [36]
A felületi komplexképződési modell felhasználására paraméterbecslő és modellező számítógépes programok állnak rendelkezésre (pl. FITEQL, MINTEQA, PHREEQX, stb.), amelyek a stabilitási állandók, a töltésmérlegek és anyagmérlegek alapján a kezelő által beadott modellre vonatkozóan becslik a kívánt mennyiségeket (stabilitási állandókat, koncentrációkat). Segítségükkel meghatározhatók azok a felületi komplexek, amelyek felelősek lehetnek a szorpcióért. A felületi komplexek létét természetesen független vizsgálatokkal (pl. spektroszkópiai módszerekkel) igazolni kell.
III.2a. táblázat:Felületi komplexképződési reakciók és modellek paraméterei
Diffúz réteg Konstans kapacitás Három réteg
+
+ ⇔−
+
−SOH H SOH2
−
+ ⇔ −
−
−SOH H SO
+ +
+ ⇔− +
+
−SOH M SOM H
+ −
−
⇔ +
−SOH L SL OH nem megengedett
(
zF RTh
I d
d =−0,1174 sin Ψ /2
σ
)
σd
σ =
− 0 Ψd
= Ψ0
felületi komplexek stabilitási állandói
felületi csoportok száma
Protolitikus reakció mint diffúz réteg
Felületi komplexképződési
reakció
Koordinációs komplexek mint diffúz réteg Ionpár komplexek
nem megengedett Töltés-potenciál
összefüggés
0 1 0 =CΨ σ
Becsült modellparaméterek
felületi komplexek stabilitási állandói felületi csoportok száma
kapacitás
mint diffúz réteg
mint diffúz réteg
+ +
−
+ ⇔− − +
+
−SOH Cat SO Cat H
− + +
−+ ⇔− −
+
−SOH An H SOH2 An
(
zF RT)
h
I d
d =−0,1174 sin Ψ /2
σ
1 0
0 ( β)C
σ = Ψ −Ψ
C σd
σ
σ0 + β =(Ψ0 −Ψβ) 2 =− felületi komplexek stabilitási állandói
felületi csoportok száma kapacitás
III.2b. táblázat: Felületi töltés és tömegmérleg egyenletek a felületi komplexképződési modellben különböző kettősréteg modellek alkalmazása esetén [35]
Modell Felületi töltés egyensúly egyenleteia
Felületi kötőhelyek mennyiségét leíró egyenletek
Diffúz réteg σ0=B([SOH2+]-(SO-]) ST=[SOH]+[SOH2+]+[SO-]+[SL]+[SOMe+] Konstans
kapacitás
mint diffúz réteg mint diffúz réteg
Három rétegb σ0=B([SOH2+]+[SOH2+-
An]+[SOMe2+]-(SO-]-[SO--Cat+]) σβ=B([SO--Cat+]-[SOH2+-An])
ST=[SOH]+[SOH2+]+[SO-]+[SOH2+- An]+[SO-Cat+]+[SL]+[SOMe+]
a A B a felületi töltés átszámítás mol dm-3-ről Cm-2-re, B=F/mS.
b A töltésegyenletek a megfelelő síkokra vonatkoznak. Például a [SO--Cat+] felületi specieszre egy negatív töltés a 0 síkra (felület síkja), egy pozitív töltés pedig a β-síkra (Stern-réteg) minden egyes specieszre.
Az urán(VI)-specieszek megkötődését az alábbi vas-oxidokon, illetve hidroxidokon vizsgálták:
- goetit (α-FeOOH) [37, 38]
- lepidokrokit (γ-FeOOH) [37]
- maghemit,γ-Fe2O3, előállítása magnetit 250 °C-on történő kiizzításával [37]
- ferrihidrit (Fe2O3.H2O) [37, 39-40]
- magnetit (Fe3O4) [37, 41]
- zöldrozsda, javasolt összetétel 4Fe(OH)2.2FeOOH.FeSO4.XH20 [37]
- korróziós termék (97 %-ban hidratált Fe(II)-oxid) [42]
- 12X18H10T acél [43]
- 1010 szénacél [44]
A szorpció mértékét a vas-oxid felület korróziója (oldódása) és az ezzel összfüggésben képződő aktív helyek száma és töltése, valamint az oldatban levő specieszek (elsősorban a hidrolízis termékek) együttesen határozzák meg. A vizsgált vas-oxidok nulla töltéspontjának pH-értékét (pzc) a III.3. táblázatban tüntettem fel (ahol ilyen adatot találtunk). A pzc-nél kisebb pH-nál a felületen a pozitív töltésű specieszek vannak túlsúlyban, tehát ezek révén anionok megkötődése valószínűsíthető. A pzc-nél nagyobb pH-értékek esetén a felületi csoportok túlnyomóan negatívak, amelyeken kationok kötődhetnek meg.
III.3. táblázat: Vas-oxidok nullatöltéspontja
Oxid pzc
Goetit 8,3 [35]
Lepidokrokit Maghemit
Ferrihidrit 7,6 [40]
magnetit 7,1 [41]
Amint azt korábban említettem, vizes oldatokban az uranil-ion pH<3,5 esetén található meg pozitív töltésű UO22+-ionként. Megközelítőleg pH=3,5 fölött kezdődik meg az uranilionok hidrolízise. Levegő jelenlétében a pH növekedésével először hidroxidok képződnek, majd pH>5,5-nél hidroxo-karbonát-komplex keletkezik. Ugyanakkor számolnunk kell az uranil-hidroxid (schoepit, UO2(OH)2·H2O) kiválásával is szilárd fázisként
(5,3<pH<7,3). A pH további növekedésével negatív töltésű oldott karbonát-komplexek válnak dominánsá az oldatfázisban.
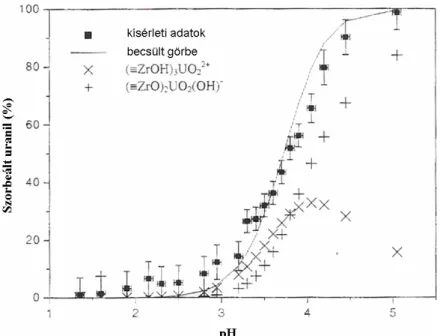
A III.6. ábrán egy a vas-oxidokra jellemző U-szorpció vs. pH görbét mutatunk be, látható, hogy alacsony pH-értékeknél (pH < 4), ahol a vas-oxidok felületi töltése és az oldatban levő uranil-specieszek töltése egyaránt pozitív, az uranilion gyakorlatilag nem kötődik meg a felületen. pH=4 és 5,5 között szorpciós élet találunk, azaz az uranil-tartalmú specieszek szorpciója jelentősen megemelkedik. A szorpció mértéke gyakorlatilag független az ionerősségtől, ami belső szférás komplexképződésre utal [41].
III.6. ábra: Az uranil-tartalmú specieszek szorpciójának jellemző pH-
függése [41].
Szorpciós élek különböző ionerősségeknél:
▲I=0,1 mol·dm-3 , szorpciós ideje 1 nap, Δ I=0,1 mol·dm-3, szorpciós ideje 4 óra,
* I=0,1 mol·dm-3, szorpciós ideje 3 hónap,
□ I=0,1 mol·dm-3, szorpciós ideje 4 óra;
○ I=0,001 mol·dm-3, szorpciós ideje 4 óra.
A modellezés alapján számított értékeket a vonalak jelzik. Szilárd magnetit/oldat arány 2 g·dm-3; az uranil-koncentráció c=4,4·10-7 mol·dm-3.
A III.2. ábráról láthatjuk, hogy a szorpciós élnek megfelelő tartomány éppen az a pH- tartomány, ahol az oldatban végbemegy az uranilionok intenzív hidrolízise. Ez a pozitív töltésű és semleges hidroxo-komplexek keletkezésének tartománya. A vas-oxidok,(- hidroxidok) felületi töltése itt még szintén pozitív (a pzc alatt vagyunk). Feltehetően tehát nem az elektrosztatikus kölcsönhatások, hanem az oldatfázisban keletkező U(VI)-hidroxo- komplexek (elsősorban az oldott és kolloid méretű UO2(OH)2o) specifikus adszorpciója szabja meg az urán akkumuláció mértékét. E specifikus adszorpciós folyamatot a felületi komplexképződési modell alkalmazói különböző felületi komplexek kialakulásával írtak le [41]. Röntgendiffrakciós vizsgálatok alapján az uranil-hidroxid (schoepit, UO2(OH)2·H2O) kiválása is valószínűsíthető; a kivált schoepit erősen a felülethez kötött, onnan nehéz eltávolítani [38]. Hosszabb szorpciós idő (3 hónap) eltelte után lényegesen nagyobb mértékű U-akkumuláció detektálható, ami az uranilionok redukciójával és a redukciós termékek megkötődésével magyarázható. Az uranil-ionokat ugyanis a korróziós folyamatok eredményeként keletkező Fe(II)-specieszek vas-oxidok jelenlétében redukálják, és rosszul oldódó urán-dioxid válik ki a felületen. A pH>8 esetén az uranil szorpciója ismét erősen
csökken. Ez azzal magyarázható, hogy a szorbensek felületi töltése itt már negatív, az UO2(OH)2o mennyisége visszaszorul az oldatfázisban és a dominánssá váló negatív töltésű komplexeket az oxidfelület már nem képes megkötni.
Azokban a vizsgálatokban, ahol szorbensként korróziós termékeket használtak, de a rendszerben jelen volt a fém vas, az urán +4 oxidációs állapotúvá történő redukcióját figyelték meg [42]. Ez az urán(IV)-dioxid képződésével és akkumulációjával jár együtt még a savas pH-kon is. Az urán(VI)-specieszek tehát redukcióval is szilárd fázisba kerülhetnek. Az adszorpciós kísérletek során tehát rendkívül nehéz megkülönböztetni az adszorpciót, a felületi kicsapódást (leválást), illetve a redukciót követő kiválást. Acél felületeken, különösen korróziós termékek jelenlétében mindhárom folyamattal számolni kell.
Meg kell jegyezni, hogy a fém Fe-al történő redukciót felhasználják az urán eltávolítására talajvizekből [45]. A redukció során akár 40 000 monorétegnek megfelelő vastagságban található az urán tartalmú csapadék a vas felületén.
A Pu specieszek reverzibilis vagy irreverzibilis módon kötődhetnek meg szilárd felületeken. Az adszorpció létrejöhet rövid hatótávolságú erők hatására, mint a kovalens kötések, hidrogén hidak. Ezek a folyamatok gyakran irreverzibilisek, mint a csapadék- kiválás. A szorpció létrejöhet nagy hatótávolságú erők hatására, mint az elektrosztatikus és a van der Waals kölcsönhatás. Ezek a folyamatok általában gyorsak és reverzibilisek, mint pl.
az ioncsere.
A Pu specieszek szorpciós tulajdonságát különböző felületeken sokan vizsgálták mind a hagyományos szorpciós izotermák (Gibbs, Freundlich, Langmuir) felvételével és ennek lineáris szakaszára érvényes megoszlási hányadosok Kd meghatározásával, mind pedig a felületi komplexképződési modellel. Az előbbi módszerben a mért/publikált Kd
értékek azonos szorbens-oldott speciesz rendszerre is akár nagyságrenddel különbözhetnek.
A felületi komplexképződési modellben az adszorpciót a töltéssel rendelkező felületi kötőhelyek és az oldott specieszek közti komplexképződésként értelmezik és ennek a reakciónak az egyensúlyi állandójával jellemzik. A modell(ek) szerint a felületeken kettős illetve hármas réteg alakul ki. Ennek a módszernek a hátránya, hogy a feltételezett komplexképzési reakciók nagyszámú paraméterét kell kevés kísérleti adathoz illeszteni.
A megoszlási hányadosok mérésével a Pu specieszek relatív szorpciós sorrendjét határozták meg. Megállapították, hogy a szorpciós hajlam megfelel az effektív töltések, és így a komplexképzés sorrendjének: Pu(IV)>Pu(III)~Pu(VI)>Pu(V). A Pu szorpciós tulajdonságait gyakran a geológiai viselkedés tanulmányozásához határozzák meg.
A szorbensek felületi rétegének jellemzéséhez meghatározták a felületek nulla töltéséhez tartozó pH értékeket (pHZPC). A III.4. táblázatban példaként néhány jellemző érték láthtó.
III.4. táblázat: Szorbensek tipikus felületi zéró töltéspontjára jellemző pH-értékek Szilárd fázis pHZPC
Amof Fe(OH)3 8,5-8,8
Goethit (α-FeOOH) 8,3 Szint. gőtit 8 Term. hematit (α-Fe2O3) 4,2-6,9
Szint. hematit 8
Magnetit (Fe3O4) 7,1
Amorf SiO 3,5-3,9
Kvarc (SiO) 1-3
MnOx 1,5-7,3
Gibbszit (α-Al(OH)3 10
A Pu specieszekre meghatározott felületi komplexképzési állandókat a III.5.
táblázatban tartalmazza. Megállapítható, hogy a Pu hidroxil komplei közül a IV oxidációs állapotú, a karbonátos komplexei közül a VI és a IV oxidációs állapotú Pu komplexek kötődnek a felületekhez legerősebben. A szorpciós folyamatokat a szokásos kémiai és elektrokémiai paraméterek mellett (pH, hőmérséklet, koncentrációk) gyakran befolyásolja a felület aktuális kialakítása, elsősorban a fajlagos felület. Megfigyelték, hogy bizonyos felületi komplexekben a Pu oxidációs állapota megváltozik. Így pl. MnO2-on a Pu(IV) és Pu(V) oxidálódik Pu(VI)-á. Goethit esetében pedig a magasabb oxidációs állapotú ionok redukálódnak Pu(IV)-é.
III.5. táblázat: Felületi komplexképződési reakciók egyensúlyi állandói talajokon és üledékeken
Reakció log10Kint
Pu3+ SOH + Pu3+ + H2O = SOPu(OH)+ + 2H+ SOH + Pu3+ + 2H2O = SOPu(OH)22+ + 3H+
-1,5 -9,1 Pu4+ SOH + Pu4+ + H2O = SOPu(OH)3+ + 2H+
SOH + Pu4+ + 2H2O = SOPu(OH)22+ + 3H+ SOH + Pu4+ + 3H2O = SOPu(OH)3+ + 4H+ SOH + Pu4+ + 4H2O = SOPu(OH)40 + 5H+
SOH + Pu4+ + 4H2O + CO32- = SOH2Pu(OH)4CO32- + 3H+
2,5 -2,0 -5,9 -12,0
8,0
PuO2+ SOH + PuO2+ = SOPuO20 + H+ -3,0
PuO22+ SOH + PuO22+ + H2O = SOPuO2(OH)0 + 2H+ SOH + PuO22+ + 2H2O = SOPuO2(OH)22- + 3H+ SOH + PuO22+ + 3CO32- + H+ = SOH2PuO2(CO3)34-
-4,5 -12,2
33,5
![III.9. ábra: A Zircaloy ötvözetek korróziójának kinetikája sematikusan [53]](https://thumb-eu.123doks.com/thumbv2/9dokorg/873231.46974/37.892.227.671.188.487/iii-ábra-zircaloy-ötvözetek-korróziójának-kinetikája-sematikusan.webp)
![III.12. ábra: VVER reaktor körülményeket modellező oldatban 2, 7, 14 és 28 napig oxidált Zr-1%Nb minták keresztmetszeti csiszolatainak SEM-felvételei [54]](https://thumb-eu.123doks.com/thumbv2/9dokorg/873231.46974/39.892.206.691.249.488/reaktor-körülményeket-modellező-oldatban-oxidált-keresztmetszeti-csiszolatainak-felvételei.webp)