VEGYÉSZMÉRNÖKI TUDOMÁNYOK ÉS ANYAGTUDOMÁNYOK
MEMBRÁNOK ALKALMAZÁSI LEHET
DOKTORI (PhD) ÉRTEKEZÉS
SZENTGYÖRGYI ESZTER OKL. KÖRNY
BÉLAFINÉ Dr. BAKÓ KATALIN TUDOMÁNYOS F
MŰSZAKI KÉMIAI KUTATÓ INTÉZET PANNON EGYETEM
VEGYÉSZMÉRNÖKI TUDOMÁNYOK ÉS ANYAGTUDOMÁNYOK DOKTORI ISKOLA
MEMBRÁNOK ALKALMAZÁSI LEHET Ő SÉGEI EL Ő ÁLLÍTÁSNÁL
DOKTORI (PhD) ÉRTEKEZÉS KÉSZÍTETTE:
SZENTGYÖRGYI ESZTER OKL. KÖRNYEZETMÉRNÖK
TÉMAVEZETŐ:
BÉLAFINÉ Dr. BAKÓ KATALIN TUDOMÁNYOS FŐMUNKATÁRS
PANNON EGYETEM
ŰSZAKI KÉMIAI KUTATÓ INTÉZET 2010
VEGYÉSZMÉRNÖKI TUDOMÁNYOK ÉS ANYAGTUDOMÁNYOK
SÉGEI A BIOGÁZ
2
MEMBRÁNOK ALKALMAZÁSI LEHET Ő SÉGEI A BIOGÁZ EL Ő ÁLLÍTÁSNÁL
Értekezés doktori (PhD) fokozat elnyerése érdekében Írta:
Szentgyörgyi Eszter, okleveles környezetmérnök
Készült a Pannon Egyetem Vegyészmérnöki tudományok és Anyagtudományok Doktori Iskolája keretében
Témavezető: Bélafiné Dr. Bakó Katalin, tudományos főmunkatárs Elfogadásra javaslom (igen / nem)
(aláírás) A jelölt a doktori szigorlaton ...%-ot ért el,
Az értekezést bírálóként elfogadásra javaslom:
Bíráló neve: …... …... igen /nem
……….
(aláírás) Bíráló neve: …... …...) igen /nem
……….
(aláírás) ***Bíráló neve: …... …...) igen /nem
……….
(aláírás) A jelölt az értekezés nyilvános vitáján …...%-ot ért el.
Veszprém, ……….
a Bíráló Bizottság elnöke A doktori (PhD) oklevél minősítése…...
………
Az EDHT elnöke
3
Kivonat
Doktori munkám során az anaerob fermentáció, és ezáltal a biogáz illetve metánkihozatal hatékonyság-növelésének lehetőségét vizsgáltam membrántechnikák integrálásával. A kísérletsorozatok első lépéseként a biogáz hozam és gázképződési sebesség együttes meghatározására alkalmas berendezést terveztünk és alakítottunk ki, mely alkalmas az egymástól lényegesen különböző biológiailag bontható szubsztrátok biogázkihozatali vizsgálatainak reprodukálható elvégzésére.
Az anaerob lebontás intenzifikálásának egyik lehetősége a mikroorganizmusok koncentrálása a rendszerben, mely által teljesebb szerves anyag lebontás és nagyobb biogázkitermelés érhető el. A mikrobák koncentrálására, mikro- és ultraszűrő membránokkal végzett méréssorozatok során megállapítottuk, hogy ultraszűrő membrán alkalmazásával a fajlagos biogázhozam növelhető. Eredményeink alapján anaerob membrán bioreaktort építettünk ki, melynek alkalmazásával a fajlagos biogázhozamot 10 %-kal, a metánhozamot 20 %-kal növeltük a hagyományos anaerob fermentorhoz képest, 7 kg KOI/m3nap terhelés és stabil üzemállapot mellett.
A kísérleti munka befejező részeként az anaerob fermentáció során termelődő biogáz metán tartalmának dúsítását vizsgáltuk gázszeparációs membrán alkalmazásával. A kereskedelmi forgalomban kapható UBE CO5 poliimid, kapilláris membránt tartalmazó modul tesztelése során tiszta gázok és modell gázelegyek permeációs sebességét és szelektivitását mértük ki. Megállapítottuk, hogy a modell biogáz minták eredeti 20-30 % CO2 tartalma az optimális kitermelési és nyomásarányok beállításával 8-10 %-ra csökkenthető.
Eredményeink alapján megállapítottuk, hogy a membrános eljárások beiktatásával valóban javítani lehet a biogáz termelés technológiáját.
4
Abstract
The aim of my scientific work was to intensify anaerobic fermentation with application of membrane techniques to enhance biogas and biomethane production. In the first set of experiments a thermostated, anaerobic laboratory scale glass unit was designed and built to study the anaerobic degradation and biogas forming potential of various substrates.
In the second set of experiments concentration of the microorganisms in the anaerobic bulk liquid was investigated in order to intensify the anaerobic degradation, i.e. to enhance the biogas production. For this purpose different micro- and ultra-filtration membranes were tested. The results showed that the biogas production could be enhanced by using ultra- filtration membranes. Based on the former results an anaerobic membrane bioreactor was built and operated using ultra-filtration membrane module in the recirculation loop. It was found that the biogas and biomethane production could be increased with 10 % and 20 %, respectively, compared to the conventional anaerobic fermenters.
Finally purification of biogas was tested using the membrane gas separation method.
For the separation of CH4 from the other biogas components, such as CO2 and N2 the commercially available UBE CO5 membrane module was tested, containing polyimide, capillary membrane. It was found that the initial 20-30% of CO2 content of model biogas could be reduced to 8-10% by application of this membrane module.
Based on our results we found that the biogas and biomethane production could be enhanced by integration of membrane processes with anaerobic fermentation
5
Auszug
In der Doktorarbeit wurde die Möglichkeit der Wirkungsgraderhöhung der anaeroben Fermentation und dadurch die Biogas- bzw. die Methanausbeute mit Integrierung von Membrantechniken untersucht. Als erster Schritt der Versuchsserie wurde eine geeignete Anlage zur gemeinsamen Bestimmung der Biogasuasbeute und der Gasbildungsgeschwindigkeit geplant und konstruiert, die zur reproduzierbaren Durchführung der Biogasausbeute von einander sehr unterschiedlichen biologisch abbaubaren Substraten geeignet ist.
Eine Möglichkeit der Intensifizierung des anaeroben Abbaues ist die Konzentrierung der Mikroorganismen im Systhem, woduch ein vollständigerer Abbau der organischen Substanzen und grössere Biogasausbeute zu erreichen ist. In Messerien mit Konzentrierung der Mikroben durch Mikro- und Ultrafiltrationsmembranen wurde festgelegt, dass die spezifische Biogasausbeute durch Anwendung des Ultrafiltrationsmembrans zu erhöhen ist.
Aufgrund der Ergebnisse wurde ein anaerob betriebener Membranbioreaktor konstruiert.
Durch Anwendung dieses Reaktors wurde die spezifische Biogasausbeute um 10 %, die Methanausbeute um 20 % im Vergleich zu dem herkömmlichen Fermenter bei 7 kg KOI/m3Tag und stabilem Betriebszustand erhöht.
Als letzter Schritt der Forschungsarbeit wurde die Konzentrierung des Methangehaltes von bei der anaeroben Fermentation gebildete Biogas mit Anwendung von Gasseparationsmembranen untersucht. Durch Testen eines, im Handel erhältlichen UBE CO5 Kapillarmembrans aus Polyimid wurden die Permeationsgeschwindigkeit und Selektivität von reinen Gasen und Modellgasgemischen gemessen. Es wurde festgestellt, dass der originelle 20-30 % CO2 Gehalt an CO2 durch Einstellung der optimalen Ausbeute und Druckverhältnisse auf 8-10 % reduziert werden kann.
Aufgrund der Ergebnisse konnte festgestellt werden, dass die Technologie der Biogasproduktion durch Anwendung von Membranverfahren wirklich verbessert werden kann.
6
Tartalomjegyzék
1 Bevezetés ... 8
2 Irodalmi összefoglalás ... 9
2.1 Anaerob fermentáció ... 9
2.1.1 Az anaerob rothasztás folyamata ... 11
2.1.2 Anaerob rothasztók üzemeltetése ... 12
2.2 Membránszeparáció ... 17
2.2.1 Nyomáskülönbségen alapuló membrán szeparáció ... 21
2.2.2 Gázszeparáció ... 24
2.3 Anaerob membrán bioreaktorok (AnMBR) ... 29
3 Kísérleti anyagok és módszerek ... 35
3.1 Anyagok ... 35
3.2 Kísérleti berendezések ... 36
3.2.1 3DTA – nyomáskülönbségen alapuló membrán-szeparációs tesztberendezés ... 36
3.2.2 GS-MS 100 – nagynyomású gáz-szeparációs modul ... 37
3.2.3 Szakaszos üzemmódú, gáztermelés mérésére alkalmas berendezés ... 39
3.2.4 Membránmodullal összekapcsolt anaerob fermentor ... 39
3.3 Analitikai módszerek ... 40
3.3.1 Kémiai oxigénigény (KOI) mérés ... 40
3.3.2 Szárazanyag tartalom meghatározása ... 41
3.3.3 Ammónium nitrogén (NH4-N) mérés ... 41
3.3.4 Összes foszfor (TP) mérés ... 42
3.3.5 Gázkromatográfiás mérés ... 42
3.4 Fizikai paraméterek ... 42
3.4.1 A pH mérése ... 42
3.4.2 Elektromos vezetés mérése ... 42
4. Eredmények és értékelés ... 44
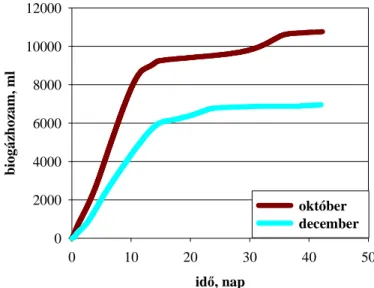
4.1 Anaerob lebontás vizsgálatára alkalmas batch reaktorok kialakítása ... 44
7
4.2 Nyomáskülönbségen alapuló membránszeparáció ... 52
4.3 Anaerob membrán bioreaktor (AnMBR) ... 59
4.4 Gázszeparációs vizsgálatok ... 65
5. Összefoglalás ... 73
Jelölésjegyzék ... 75
Irodalomjegyzék ... 76
Publikációs lista ... 83
6. Mellékletek ... 86
Új tudományos eredmények ... 89
Novel scientific results ... 90
8
1 Bevezetés
A levegő és a vizek szennyezésének növekedésével a világ minden részén egyre fontosabb kérdéssé válik a környezet védelme. A kormányok támogatják az olyan új technológiák kifejlesztését, melyek segítségével hatékonyan és gazdaságosan lehet eltávolítani a káros anyagokat a környezetből. A rendelkezésre álló megoldási lehetőségek közül, a szennyezések szerves frakciójának kezelésére alkalmas, anaerob körülmények között végzett mikrobiológiai lebontás az egyik legígéretesebb, környezetvédelmi és gazdaságossági szempontból egyaránt. Az anaerob folyamat (rothasztás) egyik fő terméke a biogáz, mely környezetvédelmi aspektusból megújuló energiaforrás. Napjainkra egyre több biogáz üzem épül világszerte, részben az egyre nagyobb mennyiségű, különböző eredetű szerves hulladékok kezelésére, részben pedig a megújuló energiaforrások iránti igény növekedése miatt.
A biogáz előállítás hatékonyságának növelésére két lehetőség kínálkozik. Egyrészről a mikroorganizmusok metabolizmusának tanulmányozása során fény derült különböző lehetséges metabolikus utakra, melyek által elősegíthető a megfelelő populációk hatékonyabb szaporodása és működése (Csáki, 2001; Hanczár, 2002). Másrészről a membránszeparációs technikák, mint környezetkímélő, hulladékszegény eljárások hatékony eszközök lehetnek az iszap-tartózkodási idő növelésében (Wang, 2009), amennyiben a mikroorganizmusokat szinte teljes mértékig visszatartják (Anderson, 1986; László, 2007; Walker, 2009) az anaerob rendszerben. Amennyiben a membránok közvetlenül kapcsolódnak az anaerob rendszerhez, a rendszer integrált anaerob membrán bioreaktorként (AnMBR) üzemel.
Munkám során célul tűztem ki egyrészt az anaerob lebontás és annak hatékonyság növelési lehetőségeinek tanulmányozását membrántechnikákkal való integrálás esetén, másrészt a termékként előállított biogáz tisztítási lehetőségét gázszeparációs membrán használatával. Vizsgálni kívántam, hogy az anaerob fermentorban visszamaradó iszap membrános koncentrálásával lehet-e biogáz többletet termelni, illetve a membrán integrálásával kialakítható membrán bioreaktor működtethető-e jobb hatékonysággal, nagyobb szerves anyag terheléssel, mint a konvencionális anaerob fermentor.
9
2 Irodalmi összefoglalás
A metán keletkezése anaerob körülmények között természetes úton több millió éve működő folyamat az olyan változatos élőhelyeken, mint a fenéklerakódások, forró források, mélytengeri árkok, mocsarak, rizsföldek vagy a szarvasmarha, disznó és az ember béltraktusában. A folyamat ipari körülmények közötti reprodukálása nem számít újdonságnak.
Az első anaerob biogáz fermentor 1859-ben Bombay-ban épült, míg Európában 1895-ben, Vesoulban (Franciaország) háztáji iszap lebontására épült. Kezdetben csak a lakossági iszap és élelmiszer hulladékok lebontására használták, míg napjainkban alkalmazása sokkal kiterjedtebb.
2.1 Anaerob fermentáció
A fermentáció szót elsőként Pasteur használta a szabad molekuláris oxigéntől mentes környezetben való sejtlégzés (respiráció) kifejezésére (Gerardi, 2003). A fermentáció akkori definíciója szerint respiráció, mely sötétben (fotoszintézis nélkül) megy végbe, és nem használ szabad oxigént, nitrát vagy nitrit iont, mint végső elektron akceptort a szerves anyagok lebontásához. Ennek alapján a respiráció számos fermentációs úton történhet, beleértve a szulfát redukciót, kevert sav előállítást és a metán előállítását. Ma a fermentáció szót jóval szélesebb körben használjuk, tulajdonképpen minden biológiai úton történő átalakításra. A fermentációt végző baktériumok lehetnek fakultatív anaerobok, aerotoleránsok vagy obligát anaerobok. A fermentáció magában foglalja a szerves anyagok átalakítását különböző szervetlen és szerves termékké. A fermentációs folyamat alatt számos oxidációs- redukciós folyamat megy végbe, melyből a baktériumok fedezik az energia szükségleteiket és számos egyszerűbb, szerves vegyületet állítanak elő.
Az iszapok és oldható hulladékok szerves anyag tartalma irányított baktérium tevékenységgel csökkenthető. Amennyiben a baktériumok tevékenysége anaerob, a szerves anyagok lebontását iszaprothasztással, míg a baktériumok aerob aktivitása esetén a lebontást iszapstabilizálással lehet elérni.
Az anaerob rothasztás jól ismert kezelési eljárás koncentrált szerves hulladékok lebontására. Előnyei közé tartozik a kis iszaphozam, a szaghatás csökkentése, az alacsony energiaigény és a stabilizált végtermék. Továbbá az anaerob rothasztás eredményeként egy speciális gázkeverék képződik, melyet biogáznak neveznek (Speece, 1996; Mata-Alvarez,
10 2000). A biogáz legnagyobb mennyiségben metánt (60-65 %) és széndioxidot (35-40 %) tartalmaz, továbbá CO, H2, N2, H2S, N2O, NH3 és H2O alkotják. Az egyetlen, gazdasági szempontból jelentős gázkomponens a biogázból a metán. Amennyiben a félfolyamatos üzemű anaerob rothasztó működése megfelelő, a naponta beadagolt nyersanyag/szubsztrát biológiailag bontható része 24 órán belül elbomlik és biogáz keletkezik belőle. A metán üzemanyagként hasznosítható, természetes, gyúlékony gáz, szagtalan és tisztán ég. A tiszta metán fűtőértéke 37,3 MJ/m3. Amennyiben a metán széndioxiddal keveredik, ahogy a biogázban is, a fűtőértéke jelentősen csökken. Az anaerob rothasztás során keletkező biogáz mennyisége általában 0,75-1,0 m3/kg szerves anyag. A biogáz fűtőértéke kb. 18,7-22,4 MJ/m3, mely a széndioxid tartalom növekedésével csökken. Amennyiben a széndioxid tartalom túl nagy, a biogáz égése nem lesz önfenntartó, adalékanyag hozzáadása válik szükségessé (Gerardi, 2003).
Az anaerob rothasztás további előnye, hogy relatív nagy üzemi hőmérsékletének és hosszú tartózkodási idejének köszönhetően szignifikánsan csökkenti a vírusok számát, a patogén baktériumokat, a gombákat és parazitákat. A patogének mennyiségi csökkentése az iszap további elhelyezése szempontjából mind a nyilvánosság, mind a jogszabályok tekintetében vonzó tulajdonság. A sok pozitív tulajdonsága mellett (2.1.1 táblázat) az anaerob rothasztásnak a hátránya, hogy instabil és nehezen szabályozható folyamat.
2.1.1 táblázat Az anaerob rothasztás előnyös tulajdonságai
• Képes lebontani a nehezen bontható természetes összetevőket, pl. lignint
• Képes lebontani a xenobiotikus összetevőket, pl. klórozott alifás szénhidrogéneket
• Javítja az iszap vízteleníthetőségét
• Metánt termel
• Iszap használata talaj adalékanyagként vagy kondicionáló szerként
• Alkalmas koncentrált ipari szennyvízhez
• Csökkenti a szaghatást, a kórokozók számát, az iszap kezelési és szállítási költségeit, az iszap illékony összetevőit
2.1.1 Az anaerob rothasztás folyamata
Az anaerob rothasztás teljes folyamata alapvet ábra) (Deublein, 2008), melybő
érkező nyersanyag többnyire szénhidrátokat, zsírokat és fehérjéket tartalmaz. Ezek polimer jellemzően vízben nem oldódó anyagok, melyek sok kisebb, egymáshoz különböz
kémiai kötéssel kapcsolódó, víz
kötések felbomlanak, így a részecskék oldatba kerülnek.
mesterségesen is elősegíthető különböz Járvás, 2010). A hidrolízist végz
keletkező oldható vegyületeket a következ
anaerob és anaerob mikroorganizmusok alakítják tovább különböz mint például a propionsav vagy etanol. Az ac
alkoholok az acetogenezis folyamata által acetáttá alakulnak, mely a következ
metánképzés szempontjából legfontosabb szubsztrát. A széndioxid és a hidrogén közvetlenül is átalakítható acetáttá vagy metá
2.1.1 ábra
A metanogenezis fázisában a metán képzése f hidrogén gázból történik. A metán el
alkoholok és szerves-nitrogén
hasznosítanak, akkumulálódnak a rothasztott iszapban. Ezek az anyagok felel Az anaerob rothasztás folyamata
Az anaerob rothasztás teljes folyamata alapvetően három szakaszra osztható ( , melyből az első a komponensek hidrolízise. Az anaerob
nyersanyag többnyire szénhidrátokat, zsírokat és fehérjéket tartalmaz. Ezek polimer nem oldódó anyagok, melyek sok kisebb, egymáshoz különböz
vízoldható részből épülnek fel. A hidrolízis során ezek a kémiai kötések felbomlanak, így a részecskék oldatba kerülnek. A kémiai kötések felbomlása segíthető különböző előkezelési eljárások beiktatásával (Beszédes, 2008;
A hidrolízist végző baktériumok fakultatív anaerobok. A hidrolízis során oldható vegyületeket a következő lépésben (acidogenezis) ugyancsak fakultatív anaerob és anaerob mikroorganizmusok alakítják tovább különböző savakká és alkoholokká,
vagy etanol. Az acidogenezis során keletkező
alkoholok az acetogenezis folyamata által acetáttá alakulnak, mely a következ
metánképzés szempontjából legfontosabb szubsztrát. A széndioxid és a hidrogén közvetlenül is átalakítható acetáttá vagy metánná.
2.1.1 ábra Biogáz képződés egyszerűsített folyamata
A metanogenezis fázisában a metán képzése főként acetátból, széndioxidból és hidrogén gázból történik. A metán előállítható néhány egyéb szerves anyagból is. A savak, nitrogén tartalom, melyet a metán-előállító baktériumok nem hasznosítanak, akkumulálódnak a rothasztott iszapban. Ezek az anyagok felel
11 en három szakaszra osztható (2.1.1 Az anaerob fermentorba nyersanyag többnyire szénhidrátokat, zsírokat és fehérjéket tartalmaz. Ezek polimer, nem oldódó anyagok, melyek sok kisebb, egymáshoz különböző erősségű olízis során ezek a kémiai A kémiai kötések felbomlása kezelési eljárások beiktatásával (Beszédes, 2008;
tatív anaerobok. A hidrolízis során lépésben (acidogenezis) ugyancsak fakultatív savakká és alkoholokká, idogenezis során keletkező szerves savak és alkoholok az acetogenezis folyamata által acetáttá alakulnak, mely a következő lépés, a metánképzés szempontjából legfontosabb szubsztrát. A széndioxid és a hidrogén közvetlenül
ként acetátból, széndioxidból és állítható néhány egyéb szerves anyagból is. A savak, állító baktériumok nem hasznosítanak, akkumulálódnak a rothasztott iszapban. Ezek az anyagok felelősek a
12 fölösiszap (az a naponta képződő iszapmennyiség, melyet a reaktor iszapkoncentrációjának illetve a hidraulikai tartózkodási idejének szabályozása érdekében az üzemeltetés során el kell távolítani) relatíve magas BOI (biológiai oxigén igény) koncentrációjáért.
Az anaerob lebontásnak hatékony működéséhez a három szakasz azonos fontosságú.
Az első lépés (hidrolizálás) inhibíciója esetén nem áll rendelkezésre elegendő szubsztrát a második és harmadik lépéshez, így a metán előállítás csökken. Amennyiben a harmadik lépés gátolt, a második lépésben keletkező savak feldúsulnak. A harmadik lépés inhibíciója áll elő, ha a savak feldúsulnak, azaz az alkalinitás és a pH is csökken. Az anaerob rothasztás folyamata általában a metanogenezis inhibíciója miatt áll le. A három folyamat szoros kapcsolatban áll egymással. Az anaerob átalakítás és szerves anyag lebontás folyamatában a sebesség meghatározó lépés az acetát előállítás. A nehezen bontható szerves anyagok esetében a sebesség meghatározó lépés a hidrolízis (Elmitwalli, 2001; Lew, 2003;
Pavlosthathis, 1991; Vavilin 1997).
2.1.2 Anaerob rothasztók üzemeltetése
Amennyiben a rendszerben nincsenek nehezen bontható szerves anyagok, az anaerob rothasztás sebesség limitáló faktora már nem a hidrolízis lesz, hanem a szerves savak konverziója metánná. A metanogén baktériumok nagyon kevés energiát hasznosítanak a szerves savak lebontásából. Az energia a metán előállítására fordítódik. A kis mennyiségű felvett energia miatt a metánképző mikroorganizmusok lassan szaporodnak. A lassú reprodukció miatt az anaerob rothasztókban optimális körülményeket kell fenntartani. A legfontosabb kontroll paraméterek a pH, alkalinitás és a hőmérséklet. Ezek mellett fontos üzemeltetési paraméterek a hidraulikus tartózkodási idő (HRT), a gázösszetétel, az illékony szerves savak mennyisége, az iszaptartózkodási idő (SRT), a toxikus anyagok jelenléte és a terhelés változás (Kárpáti, 2007; Bai, 2007).
A metánképző mikroorganizmusok elpusztulnak szabad oxigén jelenlétében. A szarvasmarha hígtrágya nagy mennyiségben tartalmaz metanogén baktériumokat, így az anaerob rothasztók beoltására és a beüzemelés ideje alatt igen hasznos lehet. A rothasztó pH- ja 6,8 és 7,2 között kell, hogy legyen. Ez a pH optimális a metanogének számára, illetve biztosítja a megfelelő puffer kapacitást. A beüzemelési időszak általában kb. egy hónapig tart, ezen idő alatt a megfelelő műveleti paraméterek biztosítása mellett stabil működést lehet elérni. A stabil működést jelzi az elégethető biogáz termelése és a stabil illékony szerves
13 sav/alkalinitás arány. A rothasztóban uralkodó magas pH ammónia toxicitást okozhat. A 7,2- es pH alatt a NH4+-ion a jellemző, ennek 1500-3000 mg/dm3 közötti értéke az optimális a megfelelő működés érdekében. Az ennél nagyobb ammónium-ion koncentráció vagy magas alkalinitás az anaerob rothasztó habzását is okozhatja. Az anaerob rothasztók terhelése 3,2-7,2 kg szerves anyag/m3nap lehet, azonban a valós terhelések 0,5-0,6 kg szerves anyag/m3nap között vannak.
Két jelentős tartózkodási idő jellegű paraméterről beszélhetünk az anaerob rothasztó esetén, az iszaptartózkodási időről (SRT – solid residence time) és a hidraulikus tartózkodási időről (HRT – hydraulic residence time). A HRT a folyadék tartózkodási ideje a reaktorban.
Alapvetően az átlagos hidraulikus tartózkodási idő határozza meg a szerves anyagok lebontásának mértékét és ezzel a rothasztó szükséges térfogatát. Az SRT az iszap (mikroorganizmusok) tartózkodási ideje a reaktorban, mely anaerob rothasztók esetén, amennyiben nincs recirkulációs áram, gyakorlatilag megegyezik a folyadék tartózkodási idejével. Recirkulációs áram alkalmazása esetén az SRT hosszabb lehet, mint a HRT. Mivel a generációs idő (az időtartam mely alatt a baktérium populáció megduplázódik) a metanogén mikroorganizmusok esetében hosszabb, mint az aerob baktériumok esetén, a jellemző SRT az anaerob rothasztókban több mint 12 nap (2.1.2 táblázat). Tíz napnál rövidebb tartózkodási idő nem javasolt, mivel ilyenkor jelentős iszapkimosódás figyelhető meg, mely főként a lassan növekvő metanogén mikroorganizmusok szempontjából hátrányos. Az SRT-re nincs hatással az iszap minősége, feltéve, hogy az nem toxikus. A HRT csökkenését okozza az iszap nagy nedvesség tartalma (94-97 %). A hidraulikus túlterhelést jelzi a hőmérséklet csökkenés, nagyobb mennyiségű és kisebb szárazanyag tartalmú fölös iszap keletkezése, metán-képződés csökkenése és a szerves anyag lebontásának csökkenése. Az anaerob rothasztók működésének egyik indikátora a metán-képződés, mely az iszap szerves anyag tartalmának lebomlását is jelzi egyben. A biogáz metántartalmának visszaesése a rendszer működésének változását mutatja, a pH csökkenésével, ezáltal savasodással jár.
14
2.1.2 táblázat A szennyvízbaktériumok fontosabb csoportjainak közelítő generációs ideje
Baktériumcsoport Funkció/szerep Közelítő generációs idő
Aerob organotrófok
Oldható szervesanyag pehelyképzése és lebontása az aktív iszapban és a csepegtető
szűrő feldolgozásban
15-30 perc
Fakultatív anaerob organotrófok
Oldható szervesanyag pehelyképzése és lebontása az aktív iszapban és a csepegtető
szűrő feldolgozásban, a szerves anyagok hidrolízise és lebontása az anaerob
rothasztásban
15-30 perc
Nitrifikáló baktérium NH4+ és NO2- oxidációja az aktív iszapban és
a csepegtető szűrő feldolgozásban 2-3 nap Metánképző baktérium Metán termelése az anaerob rothasztásban 3-30 nap
A nagy SRT előnyös az anaerob rothasztás szempontjából. Magas SRT fenntartásával maximalizálható az eltávolítási kapacitás, csökkenthető a rothasztó térfogata és puffer kapacitást biztosít a változó terhelések és toxikus hatásokkal szemben. Magas SRT kétféleképpen alakítható ki: a rothasztó térfogatának növelésével vagy a baktériumok koncentrációjának növelésével.
A szuszpendált iszappal működő anaerob rothasztókban, amelyek jellemzőinek összegzése a 2.1.3 táblázatban látható, a keverésnek igen fontos szerepe van az iszap egyenletes eloszlatásában. Ezekben a rendszerekben az SRT és a HRT azonos, a rothasztót hosszú HRT-vel tervezik. Az iszapot folyamatosan vagy szakaszosan adagolják a rendszerhez.
2.1.3 táblázat A hagyományos anaerob rothasztók előnyei és hátrányai
Előnyök Hátrányok
szemcsés, kolloid és oldható hulladékok kezelésére alkalmas
nagy rothasztótérfogat szükséges a kellő iszaptartózkodási idő (SRT) megvalósításához
a toxikus szennyvizek hígíthatók
a kezelés hatékonyságát csökkenheti a darabos és kolloid szennyvizek és a baktériumok vesztesége a rothasztó elfolyóvízébe
tápanyagok, pH, szubsztrátok és a hőmérséklet eloszlását homogénné teszi
15 A baktériumok koncentrációjának növelése érdekében, vagyis az SRT növelésére az anaerob rothasztók fix-ágyas biofilmes rendszerré alakíthatóak (Gerardi, 2003). A mikroorganizmusok a hordozó anyagra tapadnak, így megakadályozható a biomassza kimosódása a rothasztóból és magas SRT tartható fent. A fix-ágyas rendszerek nyugodt környezetet biztosítanak a növekvő mikroorganizmusoknak. Mivel a baktériumok növekedése hosszú időt vesz igénybe, a megtapadási felület (biofilm hordozó) célja a mikroorganizmusok reaktorban tartása, melynek eredményeként az SRT növekszik, míg a HRT csökkenthető.
Biofilm hordozóként kavicsot, követ vagy műanyagot használnak, mely kb. 50%-os arányban kerül a reaktorba. A fix-ágyas rothasztók átfolyó rendszerek, melyekben az iszap átáramlik a biofilmmel fedett felületek között. Az oldható szerves vegyületeket a mikroorganizmusok abszorbeálják, míg a nem oldható komponenseket adszorbeálják. Mivel a fix-ágyon a baktériumok megtapadnak, a hosszú SRT biztosított, így a metanogének akklimatizálódhatnak a különböző típusú szubsztrátokhoz. A fix-ágyas anaerob rendszereknek köszönhetően a lebontási folyamatot sokkal szélesebb körben lehet alkalmazni (lakossági és ipari hulladékok esetében is). A biofilmben a baktériumok koncentrációja nagy, így stabilabb rothasztást lehet elérni a terhelés váltakozása esetén is. Ennek köszönhetően az anaerob biotechnológia iránti érdeklődés megnövekedett, a tömény hulladékokat gyakran kezelik fix-ágyas rothasztókban.
A szerves anyagok gázzá történő átalakulása a HRT függvénye (Kárpáti, 2007;
Gerardi, 2003). A HRT függvénye a rothasztott iszap későbbi sorsa is. Amennyiben a HRT magas, a kirothasztott iszapot talajon való elhelyezésre lehet használni, míg a HRT alacsonyan tartása esetén az iszapot elégetik. A 12 napnál hosszabb tartózkodási idő nem jelenti feltétlenül a szerves anyagok teljesebb lebontását. A HRT továbbá hatással van a metántermelés sebességére és mértékére.
A hőmérsékleti körülményeknek jelentős hatása van az anaerob lebontásra. Néhány fokos hőmérséklet változás is hatással lehet a metanogén mikroorganizmusok működésére. Az anaerob rendszerek megfelelő keverése is fontos üzemeltetési szempont. A jól kevert reaktorokban nem alakulnak ki gócok, ahol a fizikai-kémiai paraméterek eltérőek lehetnek. A metán-képző baktériumok két hőmérsékleti tartományban aktívak, a mezofil (30-35°C) és termofil (50-60°C) tartományokban. 40°C és 50°C között a metanogének működése gátolt. A legtöbb metán-képző baktérium mezofil, azonban léteznek pszichrofil (5-25°C), termofil, hipertermofil (>60°C) és sztearotermofil baktériumok is. A rothasztási hőmérséklet és a rothasztás időtartama között is összefüggés figyelhető meg (2.1.2 ábra). A magasabb
16 hőmérsékleti tartományokban a szerves anyag lebontása kevesebb időt vesz igénybe, ugyanis a legtöbb kémiai reakció sebessége 10°C emelésére megduplázódik, ennek megfelelően a szerves anyag lebontása is leggyorsabban a termofil hőmérséklet-tartományban játszódik le (2.1.2 ábra) (Bai, 2007), azonban a folyamat endoterm, így ipari méretben gazdasági megfontolásból a mezofil tartományú biogáz-gyártás a jellemző.
2.1.2 ábra Az anaerob rothasztás hőmérséklet függése
A pszichrofil rendszerekben a környezeti hőmérséklettel azonos a hőmérséklet, tehát az évszakkal változik. Ezekben a rothasztókban az SRT hosszú, gyakran több, mint 12 hét. A termofil rothasztás az ipari szennyvizeknél alkalmazott folyamat, ahol a rendszer fűtése az ipari tevékenységnek köszönhetően rendelkezésre áll, nem igényel külön befektetést. A termofil rendszerek azonban nagyon érzékenyek a hőmérsékletváltozásra, kevesebb, mint 1°C hőmérsékletingadozást bírnak ki a termofil metanogének egy nap alatt, míg a mezofilek 2-3°C hőmérsékletingadozást. A legtöbb lakossági szennyvíztisztító illetve állattartási telep anaerob rothasztója, üzemeltetési és főként gazdasági megfontolásból, mezofil tartományban működik (2.1.5 táblázat).
2.1.5 táblázat A mezofil és a termofil rothasztók összehasonlítása
Tulajdonság Mezofil rothasztás Termofil rothasztás
Terhelési arány kisebb nagyobb
Patogének elpusztítása kisebb nagyobb
Mérgező anyagokra való
érzékenység kisebb nagyobb
Üzemeltetési költségek kisebb nagyobb
Hőmérséklet fenntartása kevésbé bonyolult nehézkesebb
17
2.2 Membránszeparáció
A membrán az 1985-ben nemzetközileg elfogadott definíció és nomenklatúra szerint permszelektív gát két fázis között (Bélafi-Bakó, 2007). Ez egyrészt azt jelenti, hogy a membrán egyszerre permeábilis, vagyis átjárható (bizonyos komponensek képesek átjutni rajta), és szelektív, így szeparációra alkalmas. Másrészt mindenképpen akadályt, ellenállást jelent a transzport lejátszódásánál (Bélafi-Bakó, 2002; Mulder, 1996; Staude, 1992; Noble, 1995). Membrántechnológiát az ipar számos területén használnak. Alkalmazhatóak a membránok, ha az adott elegyből az értékes komponens koncentrálása a cél, vagyis el kell távolítani az oldószert, hogy a kívánt céltermék maradjon vissza, vagy a kis mennyiségben jelenlévő szennyezőanyag/termék kinyerése a cél. Ezen túl frakcionálásra is kiválóan megfelelnek a membránok, továbbá az adott kémiai folyamat elősegítésére is alkalmasak, ha a keletkező terméket leválasztjuk a rendszerről.
A membrán szeparációs technikáknak számos előnye van. Az egyik legfontosabb, hogy energiaigényük általában kicsi, és nem termelnek veszélyes hulladékot. Működésük során semmilyen veszélyt nem jelentenek a környezetükre, rendkívül környezetbarát eljárások. Ezek mellett könnyen variálható és kombinálható más eljárásokkal, így úgynevezett
„hibrid-eljárások” jönnek létre, amelyek esetlegesen még környezetbarátabbak, és hatékonyabbak elődjeiknél. A membrántechnológiák legjelentősebb hátrányai közé tartozik a gyakran jelentkező, úgynevezett fouling probléma, vagyis eltömődés, illetve a koncentráció- polarizáció is (Ognier, 2002; Bouhahila, 2001, Ma, 2001).
A membrános műveletek a szeparáció mechanizmusa szerint is csoportosíthatóak. Az egyik legfontosabb és legelterjedtebb csoport az úgynevezett nyomáskülönbségen alapuló membrános technikák (ide tartozik a mikroszűrés (MF), ultraszűrés (UF), nanoszűrés (NF) és fordított ozmózis (RO), amelyeket összefoglaló néven membránszűrésként emlegetnek), ahol a szűrés elvén valósul meg a szeparáció. A szeparáció hajtóereje lehet még a koncentrációkülönbség (pl. dialízis, gázszeparáció vagy pervaporáció esetén), az elektromos potenciálkülönbség (elektrodialízis) és a hőmérsékletkülönbség (membrán desztilláció) is (2.2.1 táblázat).
2.2.1 táblázat A membrános műveletek csoportosítása
nyomáskülönbség koncentráció különbség mikroszűrés dialízis
ultraszűrés pervaporáció nanoszűrés gázszeparáció
fordított ozmózis ozmotikus desztilláció
A különböző típusú membráneljárások közül a leggyakrabban alkalmazottak az ultraszűrés, a nanoszűrés, elektrodialízis és a fordított ozmózis. De egyre jobban elterjedtebbé válik a gázszeparáció is, főleg nagyobb ipari méretekben.
A membránszeparációs m
szétválasztandó elegyet a membrán betáplálási oldalára vezetjük és nyomáskülönbséget hozunk létre a membrán két oldala között
hatására az elegy komponensei keres
permeátum oldalára kerülnek. Ha az elegy komponenseinek permeábilitása különböz a permeátum összetétele eltér a betáplált anyag összetételét
általános hajtóerő a komponense
függően, hogy melyik változó játssza a meghatározó szerepet a kémiai potenciálkülönbség létrehozásában.
2.2.1 ábra
Eredetüket tekintve a membránok lehetnek b
membránok. Utóbbiak között a szervetlen anyagokból készült membránok (pl. kerámia, fém, üveg, zeolit) kémiai- és hőstabilitásukat tekintve sokkal el
mint a polimer alapúak. A szilárd
különböztetünk meg. Pórusos membrán esetében az elválasztás alapja a részecskeméret
űveletek csoportosítása koncentráció-
különbség
elektromos potenciálkülönbség
hőmérséklet- különbség dialízis elektrodialízis membrán- pervaporáció (tüzelőanyagcellák) desztilláció gázszeparáció
ozmotikus desztilláció
típusú membráneljárások közül a leggyakrabban alkalmazottak az rés, elektrodialízis és a fordított ozmózis. De egyre jobban elterjedtebbé
őleg nagyobb ipari méretekben.
A membránszeparációs műveletek általános elvét az 2.2.1 ábra
szétválasztandó elegyet a membrán betáplálási oldalára vezetjük és nyomáskülönbséget két oldala között. A kémiai potenciálkülönbség
hatására az elegy komponensei keresztülhaladnak a membránon és annak átellenes ún.
permeátum oldalára kerülnek. Ha az elegy komponenseinek permeábilitása különböz
a permeátum összetétele eltér a betáplált anyag összetételétől. A membránon keresztül az a komponensek kémiai potenciálkülönbsége, de az módosulhat attól en, hogy melyik változó játssza a meghatározó szerepet a kémiai potenciálkülönbség
A membránszeparációs eljárások elvi vázlata
Eredetüket tekintve a membránok lehetnek biológiai (természetes) vagy szintetikus membránok. Utóbbiak között a szervetlen anyagokból készült membránok (pl. kerámia, fém, őstabilitásukat tekintve sokkal előnyösebb tulajdonságokkal bírnak, mint a polimer alapúak. A szilárd membránfajták között pórusos és pórusmentes típusokat különböztetünk meg. Pórusos membrán esetében az elválasztás alapja a részecskeméret
18 típusú membráneljárások közül a leggyakrabban alkalmazottak az rés, elektrodialízis és a fordított ozmózis. De egyre jobban elterjedtebbé
2.2.1 ábra mutatja be. A szétválasztandó elegyet a membrán betáplálási oldalára vezetjük és nyomáskülönbséget . A kémiai potenciálkülönbség - mint hajtóerő ztülhaladnak a membránon és annak átellenes ún.
permeátum oldalára kerülnek. Ha az elegy komponenseinek permeábilitása különböző, akkor l. A membránon keresztül az k kémiai potenciálkülönbsége, de az módosulhat attól en, hogy melyik változó játssza a meghatározó szerepet a kémiai potenciálkülönbség
A membránszeparációs eljárások elvi vázlata
iológiai (természetes) vagy szintetikus membránok. Utóbbiak között a szervetlen anyagokból készült membránok (pl. kerámia, fém, nyösebb tulajdonságokkal bírnak, membránfajták között pórusos és pórusmentes típusokat különböztetünk meg. Pórusos membrán esetében az elválasztás alapja a részecskeméret-
19 különbség (pl. MF, UF). A pórusmentes membránokat elsősorban gáz- és gőzszeparációhoz, pervaporációhoz, dialízishez, illetve fordított ozmózishoz használják (Fonyó, 1998; Bélafi- Bakó, 2002). Megjelenési formájuk szerint csoportosíthatók lapmembránokra, spirál modulokra (lapmembránból alakítva), cső- és üregszál-membránokra, mikro kapilláris membránokra, speciális membrán és modellkonstrukciókra (pl. méhsejtszerű kerámia membrán stb.) A modulokat, méretre szabhatóan, kazettává építik össze, melyeket bemerítik (szennyvíz esetében pl. bioreaktorba), és a létrehozott vákuum hatására a modul szálakon átszűrődő folyadékot (szűrlet) újrahasznosítás vagy befogadóba való bevezetés céljából elvezetik. A membrán aljában levegőztető elem van beépítve, hogy a reaktor belsejében a membrán-szálak folyamatos tisztántartása érdekében a felszálló buborékok turbulens teret alakítsanak ki.
Szerkezetük szerinti besorolásnál megkülönböztethetünk izotróp és anizotróp membránokat. Ezek a jelzők a membrán porozitására vonatkoznak: az izotróp membránok porozitása minden irányban egyforma, míg az anizotrópoknál a membrán kettő vagy több rétegből áll. Az elválasztás a legfelső, legkisebb pórusméretű rétegben történik, az alatta lévő, nagyobb pórusokat tartalmazó anyag szerepe az előző mechanikai megtámasztása, a szűrlet elvezetése. A gyakorlatban a legtöbb membrán anizotróp, az elválasztás egy vékony, gyakran csak mikrométeres vastagságú falon történik. Mivel a membránszűrés abszolút, méret szerinti elválasztás (ellentétben a tölteten vagy szűrőrétegen végbemenő mélységi, vagy statisztikus szűrésssel), a szűrőelem (azaz a membrán) vastagsága nem befolyásolja az elválasztás minőségét, tehát elegendő egy minimális vastagságú, filmszerű bevonat valamely hordozó felületén. Ha a membrán rétegei eltérő anyagból készülnek, akkor beszélünk összetett, vagy kompozit membránról. A lehetséges kombinációk köre igen széles.
A membránok teljesítményét jellemezhetjük az áteresztőképességgel vagy fluxussal. A membránszűrés megvalósítása történhet szakaszos (dead-end) vagy keresztáramú (cross-flow) módon. A szakaszos vagy nyomószűrést (2.2.2 ábra) akkor alkalmazzák, ha a kiszűrendő komponensek koncentrációja 0,1 %, vagy annál kisebb. A szűrés során a szűrendő folyadékáramot merőlegesen, megfelelő nyomással vezetik a membránra, így a pórusoknál kisebb részecskék és az oldószer áthalad a membránon, az ennél nagyobb molekulákat, ionokat visszatartja. A kiszűrt részecskék a membrán felületén szűrőlepényt képeznek. Ez a szűrési mód nagymértékben hasonlít a hagyományos szűrési eljárásokhoz, modellezése is hasonlóképpen történik.
20 2.2.2 ábra A szakaszos vagy nyomószűrés működtetése
A keresztáramú szűrés a membrántechnikában elterjedtebb megoldás (2.2.3 ábra). Itt a folyadékelegy a membrán felületével párhuzamosan, nagy sebességgel áramlik. A nyomáskülönbség hatására a folyadék egy része áthatol a membránon (szűrlet vagy permeátum), az elegy főárama tovább cirkulál, magával hordozva a visszatartott részecskéket, így a keringetett elegy (koncentrátum vagy retentátum) koncentrációja a szűrési idő előrehaladtával nő. Folytonossá tehető a folyamat, amennyiben folyamatosan történik a rátáplálás, illetve a permeátum egy részét folyamatosan elvezetjük. Az eljárás során nem képződik szűrőlepény, csak egy vékony gélréteg, ami elvileg nem okoz lényeges szűrőteljesítmény-csökkenést a szűrési idő növelésével.
2.2.3 ábra A keresztáramú szűrés működtetése
21 2.2.1 Nyomáskülönbségen alapuló membrán szeparáció
Az egyre gyarapodó szakirodalom (Öllős, 1998; Bélafi-Bakó, 2002; Hideg-Zsirai, 1990) nyomáskülönbségen alapuló membrános műveletek körébe sorolja a mikroszűrést, az ultraszűrést, a nanoszűrést és a fordított ozmózist (2.2.2 táblázat). A hagyományos szűrések esetében (nyomószűrés) a szűrő felületén lerakódott szennyező anyag is fejt ki szűrőhatást. A membránszűrés esetében a lerakódás viszont annak mértékétől függően gátolja az elválasztási folyamatot.
2.2.2 táblázat Membránszűrési eljárások csoportosítása (Bélafi-Bakó, 2002)
Membrános eljárás Mérettartomány Transzmembrán nyomás (TMP) (bar)
Mikroszűrés 0,1-10 µm 0,1-1,0
Ultraszűrés 1-500 kDa 1,0-10
Nanoszűrés >300 Da
<50 % kisebb NaCl retenció 5,0-20
Fordított ozmózis 25-99,9 % NaCl retenció 20-100
A mikroszűrés az a membrános művelet, amely a legközelebb áll a hagyományos értelemben vett szűréshez. A mikroszűrő membránok alkalmasak lebegő szennyeződések, illetve a mikroorganizmusok közül a baktériumok és gombák eltávolítására. A kiszűrendő komponensek nem oldott állapotban vannak jelen, hanem lebegő részecskék, szuszpenzió vagy emulzió formájában. A pórusméret itt a legnagyobb (0,1-2 µm), a membrán ellenállása a legkisebb, így az alkalmazandó transzmembrán-nyomás is a legkisebb (2.2.2 táblázat) (Bélafi-Bakó, 2002).
A mikroszűrő membránokon keresztüli térfogatáram-sűrűség, vagyis a fluxus, J (Darcy törvényének megfelelően) egyenesen arányos az alkalmazott ∆p nyomás-különbséggel (2.1 egyenlet).
= ∙ ∆ 2.1 egyenlet
A – permeábilitási állandó, amely tartalmazza a porozitás és a pórusméret, illetve pórusméret-eloszlás hatásait, valamint az elválasztandó folyadékelegy viszkozitását.
22 A mikroszűrés alkalmazása során a fő probléma, amivel számolni kell, a fluxus csökkenése. Ennek oka egyrészt a koncentráció-polarizáció, másrészt az eltömődés (fouling).
A mikroszűrés alkalmazható szakaszos műveletként (dead-end) és keresztáramú módban egyaránt. Bármelyiket is választjuk, egy idő után a visszatartott részecskék akkumulálódni fognak, és szűrőlepény alakul ki a membrán felületén, amely további ellenállást jelent a szűrés folyamán. A mikroszűrésnek előtisztító szerepe van ultraszűrést, nanoszűrést és fordított ozmózist alkalmazó eljárások előtt.
Az ultraszűrő membrán a szubmikron méretű kolloid részecskéket, mikroorganizmusokat, iszapot és a nagy molekulatömegű vegyületeket, pl. fehérjéket is képes visszatartani (Gerardi, 2003; Galambos, 2006). A keresztáramú szűrési mód elterjedt, az ehhez szükséges nyomáskülönbség 3-8 bar. Alkalmazható mind szakaszos, mind folyamatos módban egyaránt. Az ultraszűrő membránok pórusmérete 500 nm és 1 nm közötti, de a membránok jobban jellemezhetők a vágási értékkel. Az ultraszűrő membránok vágási értéke (MWCO, molecular weight cut off) 1-1000 kDa. A mikroszűrő membránokhoz hasonlóan az ultraszűrő membránok is pórusosak, amelyeknél a visszatartást elsősorban az oldott részecskék, anyagok mérete és alakja határozza meg, és az anyagtranszport egyenesen arányos az alkalmazott nyomás-különbséggel. Az ultraszűrést igen gyakran alkalmazzák makromolekulák oldatának koncentrálására, ahol ezen nagy molekulákat a membránnak vissza kell tartania, míg a kicsiket (és az oldószert) át kell eresztenie. Az ilyen célú, megfelelő membrán kiválasztásának megkönnyítéséhez vezették be a vágási érték (cut off) fogalmát.
A nanoszűrő membrán képes a kisebb molekulákat, mint pl. a cukrokat és a kétvegyértékű ionokat is kiszűrni a vízből. Az ultraszűréshez képest tehát kisebb vegyületek szeparációjáról van szó, amihez kisebb pórusméretű, következésképp nagyobb ellenállású membránt kell használni (Hilal, 2004). Pórusmérete 1-10 nm lehet, vágási értéke 100-1000 Da. Pórusméretét jellemzi ezen kívül a NaCl-visszatartása is, amelynek jellemző értéke 30-70
%. A megnövekedett membránellenállás miatt jóval nagyobb nyomás-különbséget kell alkalmazni a megszokott mennyiségű permeátum eléréséhez. Ráadásul a kis molekulatömegű anyagoknál az ozmózisnyomás is számottevő, amit szintén le kell győzni (Békássy-Molnár, 2000). A szűrésnél szükséges nyomáskülönbség 10-20 bar között változhat. A membránszűrési technológiák közül ez a legjobban elterjedt, és a legszélesebb körben alkalmazott módszer.
23 A nyomáskülönbségen alapuló membránszűrési technológiák közül a fordított ozmózissal lehet a legfinomabb szűrést elérni (Porter, 1990). A különböző molekulák eltérő diffúziós viselkedésén alapul ez az elválasztás. Az ozmotikus hatások jelentősek, a hajtóerőként alkalmazott nyomás is itt a legnagyobb, 20 - 100 bar. A víz fluxusa még ilyen nagy nyomáskülönbség mellett is viszonylag kicsi. Az RO membránok gyakorlatilag csak az oldószer molekulákat engedik át. NaCl-visszatartásuk elérheti a 99-99,9 % ot.
Az ultraszűréshez képest tehát kisebb vegyületek szeparációjáról van szó, amihez nagy ellenállású membránt kell használnunk. Valójában a nanoszűrő és fordított ozmózis membránok átmenetet képeznek az ultraszűrésnél alkalmazott pórusos membránok és a nem- pórusos, sűrű membránok között (ez utóbbiakat pl. pervaporációnál, gázszeparációnál használják) (Bélafi-Bakó, 2002; Rautenbach 1997). A megnövekedett membránellenállás, a membrán anyagának az MF-UF membránanyagokkal szembeni eltérése és a megnövekedett ozmózisnyomás legyőzése miatt nagyobb nyomás-különbség alkalmazására van szükség a kívánt mennyiségű permeátum eléréséhez. A kis molekulatömegű anyagoknál, mint már említettem, fellép az ozmózisnyomás jelensége, akárcsak a már említett nanoszűrésnél. A membrán az oldott anyagot (pl. só) nem engedi át, míg az oldószert (víz) átereszti. Ha az alkalmazott nyomás kisebb, mint az ozmózisnyomás, a víz a hígabb oldat (pl. tiszta víz) felől fog áramlani a töményebb felé. Ha viszont a nyomás nagyobb, mint az ozmózisnyomás az adott esetben, a víz a töményebb oldat felől áramlik a hígabb felé. Mindezeket figyelembe véve a valódi fluxus (vízáram-sűrűség – J) a 2.2 egyenlettel írható le (feltételezve, hogy oldott anyag egyáltalán nem jut át a membránon, vagyis a retenció R = 100%).
= ∙ (∆ −Π) 2.2 egyenlet
∆p – alkalmazott nyomáskülönbség, Π – ozmózisnyomás,
k – hidrodinamikai permeabilitási koefficiens.
Ha az oldott anyag retenciója nem tökéletes, a gyakorlatban ez szokott előfordulni, akkor az elméleti ozmózisnyomásnál kisebb értéket kell figyelembe venni. A hidrodinamikai permeábilitási (víz permeabilitása) koefficiens egy adott membránra nézve állandó, és értékét az oldhatóság és a diffuzivitás határozza meg. A membránok szelektivitását leginkább a retenciós, vagy visszatartási koefficienssel lehet jellemezni. A fordított ozmózist legnagyobb léptékben tengervíz sótalanításra használják a Közel-Keleten, de alkalmazzák kazántápvíz
24 előkészítésére, a gyógyszeriparban különlegesen tiszta víz előállítására, pl.
szövettenyésztéshez, oltóanyagkészítéshez.
2.2.2 Gázszeparáció
A gázszeparáció (gőzpermeáció) során gázok keverékének elválasztása a cél. A gázszeparáció hajtóereje alapvetően a koncentrációgradiens, de a nyomáskülönbségnek is fontos szerepe van a művelet kivitelezésnél. A gázszeparáció pórusmentes és pórusos membránokon keresztül egyaránt elképzelhető (Bélafi-Bakó, 2002). A pórusos és a nem- pórusos membránokon át zajló gázszeparáció mechanizmusa azonban igen eltérő [Mulder, 1996; Noble, 1995).
Gáznemű anyagok elválasztása céljából történő membrános művelet során, ha a gázok transzportja viszkózus áramlásként írható le (pl. mikroszűrő membránokon keresztül), szeparáció nem játszódhat le, mivel a gázmolekulák szabad úthossza igen rövid a membrán pórusátmérőjéhez képest (Bélafi-Bakó, 2002). A pórus méretét csökkentve elérhetjük, hogy a gázmolekulák szabad úthossza nagyobbá válik, mint a pórusátmérő. Ezt a fajta gázáramlást Knudsen-áramlásnak nevezzük és a 2.3 egyenlettel írhatjuk le.
J nr D p
RT l
= ⋅ k
⋅ π
τ
2 ∆
2.3 egyenlet J – fluxus,
l – membrán vastagsága, n – pórusok száma,
∆p – nyomáskülönbség, τ – tortuozitás,
Dk – Knudsen diffúziós koefficiens, r – pórus sugara.
A Knudsen koefficienst meghatározását a 2.4 egyenlet írja le.
D r RT
k M
w
=0 66 8⋅
, π 2.4 egyenlet
T – hőmérséklet, Mw – molekula tömege.
Az előbbi két egyenletb molekulatömeg négyzetgyökével,
áramlást egy adott membrán és nyomáskülönbség esetén. Így két gáz szeparációját a Knudsen-áramlás mechanizmusa szerint a két molekulatömeg négyzetgyökének aránya határozza meg. Ez azt jelenti, hogy meglehet
Nagyobb szeparációs faktor csak kaszkád rendszer
igazán gazdaságos. Az egyetlen alkalmazási területe mostanáig ezért a pórusos membránnal történő gáz szeparációnak az uránium hexafluorid töményítése, amely igen drága anyag.
Franciaországban működtetnek egy ilyen üzemet, ahol pórusos kerámiamembránt használnak.
A Knudsen-áramlásnak azonban van egy másik fontos vetülete is. A nem membránokkal történő gázszeparáció során, ha kompozit membránt használnak, ahol a s aktív réteget pórusos támasztóréteg tartja, a pórusos rétegben fellép
hozzájárulhat az összáramláshoz.
A nem-pórusos membránon át történ
membránon keresztül mérhető permeábilitásától függ
2.2.4 ábra Két gáz elválasztása nem
A nem-pórusos szerkezeten át történ leírását a Fick-törvény adja (2.5
J
D dc/dx
bbi két egyenletből jól látszik, hogy az áramlás fordítottan arányos a molekulatömeg négyzetgyökével, és ez az egyetlen paraméter, amely meghatározza az áramlást egy adott membrán és nyomáskülönbség esetén. Így két gáz szeparációját a mechanizmusa szerint a két molekulatömeg négyzetgyökének aránya határozza meg. Ez azt jelenti, hogy meglehetősen alacsony szeparációs faktor nyerhet Nagyobb szeparációs faktor csak kaszkád rendszerű üzemmódban érhető el, ez azonban nem
. Az egyetlen alkalmazási területe mostanáig ezért a pórusos membránnal gáz szeparációnak az uránium hexafluorid töményítése, amely igen drága anyag.
ködtetnek egy ilyen üzemet, ahol pórusos kerámiamembránt használnak.
áramlásnak azonban van egy másik fontos vetülete is. A nem gázszeparáció során, ha kompozit membránt használnak, ahol a s aktív réteget pórusos támasztóréteg tartja, a pórusos rétegben fellépő
z összáramláshoz.
pórusos membránon át történő gázszeparáció a különböző gázoknak az adott membránon keresztül mérhető permeábilitásától függ (2.2.4 ábrán).
Két gáz elválasztása nem-pórusos membránon keresztül
pórusos szerkezeten át történő egydimenziós gázdiffúzió legegyszer 2.5 egyenlet).
J Ddc
= − dx
D – diffúziós koefficiens,
dc/dx – hajtóerő: a koncentrációgradiens a membrán keresztmetszetén.
25 l jól látszik, hogy az áramlás fordítottan arányos a s ez az egyetlen paraméter, amely meghatározza az áramlást egy adott membrán és nyomáskülönbség esetén. Így két gáz szeparációját a mechanizmusa szerint a két molekulatömeg négyzetgyökének aránya sen alacsony szeparációs faktor nyerhető.
ő el, ez azonban nem . Az egyetlen alkalmazási területe mostanáig ezért a pórusos membránnal gáz szeparációnak az uránium hexafluorid töményítése, amely igen drága anyag.
ködtetnek egy ilyen üzemet, ahol pórusos kerámiamembránt használnak.
áramlásnak azonban van egy másik fontos vetülete is. A nem-pórusos gázszeparáció során, ha kompozit membránt használnak, ahol a sűrű aktív réteget pórusos támasztóréteg tartja, a pórusos rétegben fellépő Knudsen-áramlás
gázszeparáció a különböző gázoknak az adott
pórusos membránon keresztül
gázdiffúzió legegyszerűbb
2.5 egyenlet
iens a membrán
26 Állandósult körülmények között a 2.5 egyenlet kiintegrálható (2.6 egyenlet).
J D c c
i l
i i l i
= ( 0, − ,)
2.6 egyenlet co,i, cl,i – a két oldalon mérhető koncentráció,
l – membrán vastagsága.
A koncentrációkat a Henry-törvényben szereplő parciális nyomások határozzák meg (2.7 egyenlet).
= ∙ 2.7 egyenlet
Si – az i-edik komponens oldhatósági koefficiense a membránban.
A Henry-törvény főként az amorf, elasztomer polimerek esetén alkalmazható, mivel az oldhatóság gyakran sokkal komplexebb folyamat az üvegesedési hőmérséklet alatt. Az előbbi két egyenletet kombinálva kapjuk meg a gázszeparáció leírására általában használt képletet (2.8 egyenlet).
=
(,,)2.8 egyenlet
A D diffúziós koefficiens és az S oldhatósági koefficiens szorzataként kapjuk meg az úgynevezett permeábilitási koefficienst (Pm) (2.9 egyenlet)
= ∙
2.9 egyenletÍgy a 2.9 egyenlet egyszerűsíthető (2.10 egyenlet).
=
,(,,)
=
,
∆
2.10 egyenletEbből a képletből világosan kitűnik, hogy a membránon át történő áramlás-sűrűsége (fluxus) egyenesen arányos a (parciális) nyomáskülönbséggel és fordítottan arányos a membrán vastagságával. A szelektivitás (elválasztási tényező) ideális esetben megadható a permeábilitási koefficiensek (’i’ és ’j’-edik komponens) hányadosával (2.11 egyenlet).
27
/=
,, 2.11 egyenlet
Számos gázelegy esetén a valódi szeparációs faktor nem egyezik meg az ideális szelektivitási faktorral, mert nagy nyomás alkalmazásakor, amikor a gáz és a polimer között kölcsönhatás lép fel, a membrán anyaga módosulhat. Emiatt általában a permeábilitás nő, a szelektivitás viszont csökkenni szokott. A valódi szeparációs faktor függ a membrán két oldala közötti nyomások arányától is. Nagy értékek esetén érhető el a szeparációs hatékonyság maximuma. Ez megvalósítható vagy a (primer) betáplálási oldalon alkalmazott nagy nyomás alkalmazásával, és/vagy vákuum létesítésével a permeátum (szekunder) oldalon.
A permeábilitási koefficiens (Pm) igen jellemző paraméter a gázszeparációnál.
Viszonylag könnyen mérhető, ha ismert az alkalmazott membrán vastagsága. A permeábilitási koefficienst sokszor úgynevezett Barrer egységben adják meg (1 Barrer = 10-10 cm3 (STP) cm cm-2 s-1 cmHg-1 = 0,76 10-17 m3 (STP) m m-2 s-1 Pa-1, STP: normál állapot (standard temperature and pressure)). Egy adott gáz permeábilitása általában sokkal nagyobb elasztomer polimerekben, mint üveges állapotúakban, a láncok nagyobb mobilitása miatt. Az egyes gázok permeábilitása adott membrán esetén nemcsak a gáz atomok/molekulák méretétől függ, hanem a kondenzációra való hajlamától is. A gőzök permeábilitása így (standard körülmények között mérve) ugyanazon membránnál több nagyságrenddel meghaladhatja a gázokét (Bélafi-Bakó, 2002; Mulder, 1996, Staude, 1992).
Egy adott gáz permeábilitásának értéke hat nagyságrenden belül mozoghat az alkalmazott polimer membrántípusától függően. Ugyanakkor a különféle gázok és gőzök permeábilitása hasonlóan tág határok között mozoghat egy adott membrán esetén. Látható tehát, hogy a gázszeparációs műveletekhez nagyon sokféle polimer anyag felhasználható a szeparációs céltól függően. Azoknál az elválasztási problémáknál, ahol a komponensek kölcsönhatása a membránnal igen különböző (pl. gázok és gőzök szeparációja), így a permeábilitások aránya (szelektivitás) nagy, leginkább nagy áteresztőképességű anyagot szoktak választani. Ezek általában elasztomerek, mint pl. a szilikon gumi, vagy természetes gumi. Az elasztomerek szelektivitása azonban számos szeparáció során kicsiny, ilyenkor az üveges állapotú polimereket alkalmazzák, bár ezek permeábilitása jóval kisebb.
Gázszeparációs célokra főként aszimmetrikus és kompozit membránokat használnak.
Ezen membránok esetén a hidrodinamikai ellenállást tehát a vékony szelektív réteg jelenti.
28 Ennek a rétegnek hibamentesnek kell lennie, mivel a hibák erőteljesen csökkentik a szelektivitást, anélkül, hogy a fluxust jelentősen növelnék. Üveges állapotú polimerből meglehetősen nehéz hibamentes aktív réteget készíteni. Az is előfordulhat, hogy az aktív réteg molekulái behatolnak a támasztórétegbe és a membrán teljes ellenállása megnő.
A gázszeparáció alkalmazási területeit alapvetően két részre lehet osztani attól függően, hogy nagy vagy kicsi permeábilitású membránt használunk. Nagy permeábilitású anyagokat alkalmazhatunk, ha nem szükséges a nagy szelektivitás, pl. oxigénben dúsított levegő előállítása orvosi célokra, vagy égetéshez; steril levegő aerob fermentációkhoz. De ide tartozik a gőzök és a nem-kondenzálódó gázok elválasztása, pl. nitrogén szeparációja levegőből, vagy metán kinyerése hosszabb szénláncú szénhidrogének mellől. Ezeknél nagyobb szelektivitás érhető el viszonylag jó áteresztőképesség mellett. A hidrofób elasztomer anyagok permeábilitása sokkal kisebb nitrogénre vagy metánra nézve, mint szerves gőzökre, így ezekre az alkalmazási területekre igen előnyös, ha jó áteresztőképességű membránt választunk (Toshima, 1992; Whyte, 1983; Bakonyi, 2008).
Közepes szelektivitás eléréséhez kis permeábilitású membrán anyagokat célszerű választani, amelyek üveges állapotú polimerek lehetnek. A gyakorlatban a permeábilitás és a szelektivitás közötti egyensúly megteremtésével lehet hatékony membrános eljárásokat kidolgozni. Egy membrános gázszeparációs eljárás gazdaságilag akkor lesz hatékony, ha a membránnak nagy a permeabilitása és szelektivitása is az elválasztani kívánt gázkomponensekre, illetve nagy a mechanikai és hőstabilitása. Az elmúlt évtizedekben a polimer membránok gázszeparációs területen való alkalmazása egyre bővült. A rendelkezésre álló polimerek közül az aromás poliszulfon, polikarbonát, poliaril-keton, poliarilén-éter és poliimid membránok bizonyultak megfelelőnek a gázszeparációra (Mousavi, 2008).
A biogáz, mint az az első fejezetben leírtakban szerepel, főként széndioxidból és metánból áll. A biogáz jelenleg csak az előállítás helyén használható fel (Göblös, 2010). A tisztított, metánban dúsított biogáz felhasználható lenne a háztartásokban, gépjármű üzemanyagként vagy elektromos áram generálására. Ehhez a biogázból a széndioxidot és egyéb nyomgázokat el kell távolítani, és palackozva szállíthatóvá kell tenni. Az elmúlt évtizedben a kutatások a membrános gázszeparáció felé fordultak.
Az egykomponensű metán és széndioxid gázok permeációját különböző membránokon vizsgálták a kutatók. A CO2/CH4 szelektivitás értéke függ a membrán típusától (Mousavi,